DÆ°áŧi ÄÃĒy là náŧi dung PhÆ°ÆĄng phÃĄp giášĢi cÃĄc dᚥng bà i tášp chÆ°ÆĄng liÊn kášŋt hÃģa háŧc nÄm 2021 ÄÆ°áŧĢc hoc247 biÊn soᚥn và táŧng háŧĢp, váŧi náŧi dung Äᚧy Äáŧ§, chi tiášŋt cÃģ ÄÃĄp ÃĄn Äi kÃĻm sáš― giÚp cÃĄc em háŧc sinh Ãīn tášp cáŧ§ng cáŧ kiášŋn tháŧĐc, nÃĒng cao káŧđ nÄng là m bà i. Máŧi cÃĄc em cÃđng tham khášĢo!
A. KIášūN THáŧĻC CášĶN NášŪM
1. Dᚥng 1: GiášĢi thÃch sáŧą hÃŽnh thà nh liÊn kášŋt ion
+ LiÊn kášŋt ion ÄÆ°áŧĢc tᚥo thà nh táŧŦ kim loᚥi và phi kim:
Kim loᚥi â e â Cation
Phi kim + e â Anion
+ GiáŧŊa anion và cation tᚥo thà nh cÃģ láŧąc hÚt tÄĐnh Äiáŧn và tᚥo thà nh liÊn kášŋt ion
+ Hiáŧu Äáŧ ášĨm Äiáŧn giáŧŊa 2 nguyÊn táŧ liÊn kášŋt thÆ°áŧng âĨ 1,7
2. Dᚥng 2: GiášĢi thÃch sáŧą hÃŽnh thà nh cáŧ§a liÊn kášŋt cáŧng hÃģa tráŧ
+ LiÊn kášŋt cáŧng hÃģa tráŧ ÄÆ°áŧĢc hÃŽnh thà nh bášąng cáš·p electron chung
- Cáš·p e dÃđng chung phÃĒn báŧ Äáŧi xáŧĐng giáŧŊa hai hᚥt nhÃĒn nguyÊn táŧ tham gia liÊn kášŋt thÃŽ ÄÃģ là liÊn kášŋt cáŧng hÃģa tráŧ khÃīng phÃĒn cáŧąc.
- Khi cáš·p e dÃđng chung báŧ hÚt váŧ nguyÊn táŧ cÃģ Äáŧ ÃĒm Äiáŧn láŧn hÆĄn thÃŽ ÄÃģ là liÊn kášŋt cáŧng hÃģa tráŧ cÃģ cáŧąc.
+ Hiáŧu Äáŧ ÃĒm Äiáŧn trong liÊn kášŋt cáŧng hÃģa tráŧ:
- Hiáŧu Äáŧ ÃĒm Äiáŧn cáŧ§a 2 nguyÊn táŧ trong liÊn kášŋt cáŧng hÃģa tráŧ khÃīng cáŧąc: TáŧŦ 0 Äášŋn nháŧ hÆĄn 0,4
- Hiáŧu Äáŧ ÃĒm Äiáŧn cáŧ§a 2 nguyÊn táŧ trong liÊn kášŋt cáŧng hÃģa tráŧ cÃģ cáŧąc: TáŧŦ 0,4 Äášŋn nháŧ hÆĄn 1,7
3. Dᚥng 3: XÃĄc Äáŧnh trᚥng thÃĄi lai hÃģa
+ Lai hÃģa sp
- Là sáŧą táŧ háŧĢp 1 obitan s váŧi 1 obitan p tᚥo thà nh 2 obitan lai hÃģa sp.
- 2 obitan sp nà y nášąm thášģng hà ng váŧi nhau, hÆ°áŧng váŧ 2 phÃa, Äáŧi xáŧĐng nhau.
- GÃģc liÊn kášŋt bášąng 180o.
+ Lai hÃģa sp2
- Là sáŧą táŧ háŧĢp 1 obitan s váŧi 2 obitan p tᚥo thà nh 3 obitan lai hÃģa sp2.
- 3 obitan sp2nà y nášąm trong 1 máš·t phášģng, Äáŧnh hÆ°áŧng táŧŦ tÃĒm Äášŋn Äáŧnh cáŧ§a tam giÃĄc Äáŧu.
- GÃģc liÊn kášŋt bášąng 120o.
+ Lai hÃģa sp3
- Là sáŧą táŧ háŧĢp 1 obitan s váŧi 3 obitan p tᚥo thà nh 4 obitan lᚥi hÃģa sp3.
- Äáŧnh hÆ°áŧng táŧŦ tÃĒm Äášŋn 4 Äáŧnh cáŧ§a hÃŽnh táŧĐ diáŧn Äáŧu.
- CÃĄc tráŧĨc Äáŧi xáŧĐng cáŧ§a chÚng tᚥo váŧi nhau 1 gÃģc 109o28'.
4. Dᚥng 4: Viášŋt cÃīng tháŧĐc cášĨu tᚥo cáŧ§a cÃĄc phÃĒn táŧ
Viášŋt cášĨu hÃŽnh e cáŧ§a cÃĄc nguyÊn táŧ tᚥo háŧĢp chášĨt:
TÃnh nhášĐm sáŧ e máŧi nguyÊn táŧ gÃģp chung = 8 â sáŧ e láŧp nc
CÃīng tháŧĐc electron : Biáŧu diáŧ n cÃĄc e láŧp ngoà i cÃđng và cÃĄc cáš·p e chung (bášąng cÃĄc dášĨu chášĨm) lÊn xung quanh kà hiáŧu nguyÊn táŧ
CÃīng tháŧĐc cášĨu tᚥo: Thay máŧi cáš·p e chung bášąng 1 gᚥch ngang
5. Dᚥng 5: XÃĄc Äáŧnh hÃģa tráŧ và sáŧ oxi hÃģa
HÃģa tráŧ:
- HáŧĢp chášĨt ion:
+ NgÆ°áŧi ta quy Æ°áŧc , khi viášŋt Äiáŧn hÃģa tráŧ cáŧ§a nguyÊn táŧ , ghi giÃĄ tráŧ Äiáŧn tÃch trÆ°áŧc, dášĨu cáŧ§a Äiáŧn tÃch sau
+ CÃĄc nguyÊn táŧ kim loᚥi thuáŧc nhÃģm IA , IIA , IIIA cÃģ sáŧ electron áŧ láŧp ngoà i cÃđng là 1, 2, 3 cÃģ tháŧ nhÆ°áŧng nÊn cÃģ Äiáŧn hÃģa tráŧ là 1+ , 2+ , 3+
+ CÃĄc nguyÊn táŧ phi kim thuáŧc nhÃģm VIA , VIIA nÊn cÃģ 6, 7 electron láŧp ngoà i cÃđng , cÃģ tháŧ nhášn thÊm 2 hay 1 electron và o láŧp ngoà i cÃđng , nÊn cÃģ Äiáŧn hÃģa tráŧ 2â , 1â
- HáŧĢp chášĨt cáŧng hÃģa tráŧ:
+ Trong cÃĄc háŧĢp chášĨt cáŧng hÃģa tráŧ, hÃģa tráŧ cáŧ§a 1 nguyÊn táŧ ÄÆ°áŧĢc xÃĄc Äáŧnh bášąng sáŧ liÊn kášŋt cáŧng hÃģa tráŧ cáŧ§a nguyÊn táŧ nguyÊn táŧ ÄÃģ trong phÃĒn táŧ và ÄÆ°áŧĢc gáŧi là cáŧng hÃģa tráŧ cáŧ§a nguyÊn táŧ ÄÃģ
Sáŧ oxi hÃģa:
Quy tášŊc 1 : SOXH cáŧ§a cÃĄc nguyÊn táŧ trong cÃĄc ÄÆĄn chášĨt bášąng khÃīng
Quy tášŊc 2 : Trong 1 phÃĒn táŧ, táŧng sáŧ SOXH cáŧ§a cÃĄc nguyÊn táŧ bášąng 0
Quy tášŊc 3 : SOXH cáŧ§a cÃĄc ion ÄÆĄn nguyÊn táŧ bášąng Äiáŧn tÃch cáŧ§a ion ÄÃģ . Trong ion Äa nguyÊn táŧ , táŧng sáŧ SXOH cáŧ§a cÃĄc nguyÊn táŧ bášąng Äiáŧn tÃch cáŧ§a ion
Quy tášŊc 4 : Trong hᚧu hášŋt cÃĄc háŧĢp chášĨt, SOXH cáŧ§a H bášąng +1 , tráŧŦ 1 sáŧ trÆ°áŧng háŧĢp nhÆ° hidru, kim loᚥi (NaH , CaH2...). SOXH cáŧ§a O bášąng â2 tráŧŦ trÆ°áŧng háŧĢp OF2, peoxit (chášģng hᚥn H2O2,...)
LÆ°u Ã―: SOXH ÄÆ°áŧĢc viášŋt bášąng cháŧŊ sáŧ thÆ°áŧng dášĨu Äáš·t phÃa trÆ°áŧc và ÄÆ°áŧĢc Äáš·t áŧ trÊn kà hiáŧu nguyÊn táŧ
B. BÃI TᚎP MINH HáŧA
Bà i 1: HáŧĢp chášĨt trong phÃĒn táŧ cÃģ liÊn kášŋt ion là :
A. NH4Cl.
B. HCl.
C. NH3.
D. H2O.
HÆ°áŧng dášŦn giášĢi:
LiÊn kášŋt giáŧŊa cation NH4+ và anion Cl-
â ÄÃĄp ÃĄn A
Bà i 2: CÃģ 2 nguyÊn táŧ X ( Z = 19); Y (Z =17) háŧĢp chášĨt tᚥo báŧi X và Y cÃģ cÃīng tháŧĐc và kiáŧu liÊn kášŋt là :
A. XY, liÊn kášŋt ion
B. X2Y, liÊn kášŋt ion
C. XY, liÊn kášŋt cáŧng hÃģa tráŧ cÃģ cáŧąc
D. XY2, liÊn kášŋt cáŧng hÃģa tráŧ cÃģ cáŧąc
HÆ°áŧng dášŦn giášĢi:
CášĨu hÃŽnh e:
X: [Ar]4s1 â X thuáŧc nhÃģm IA
Y: [Ne]3s23p5 â Y thuáŧc nhÃģm VIIA
Ta cÃģ: X â 1e â X+
Y + 1e â Y-
â HáŧĢp chášĨt tᚥo báŧi X và Y là XY và liÊn kášŋt ion
â ÄÃĄp ÃĄn C
Bà i 3: DÃĢy nà o sau ÄÃĒy khÃīng cháŧĐa háŧĢp chášĨt ion ?
A. NH4Cl, OF2, H2S.
B. CO2, Cl2, CCl4.
C. BF3, AlF3, CH4.
D. I2, CaO, CaCl2.
HÆ°áŧng dášŦn giášĢi:
+ ÄÃĄp ÃĄn A: HáŧĢp chášĨt ion NH4Cl
+ ÄÃĄp ÃĄn C: HáŧĢp chášĨt ion BF3, AlF3
+ ÄÃĄp ÃĄn D: HáŧĢp chášĨt ion CaCl2
â ÄÃĄp ÃĄn B
Bà i 4: X, Y, Z là nháŧŊng nguyÊn táŧ cÃģ Äiáŧn tÃch hᚥt nhÃĒn lᚧn lÆ°áŧĢt là 9, 19, 8.
1. Viášŋt cášĨu hÃŽnh electron nguyÊn táŧ cáŧ§a cÃĄc nguyÊn táŧ ÄÃģ. Cho biášŋt tÃnh chášĨt hÃģa háŧc Äáš·c trÆ°ng cáŧ§a X, Y, Z.
2. Dáŧą ÄoÃĄn liÊn kášŋt hÃģa háŧc cÃģ tháŧ cÃģ giáŧŊa cÃĄc cáš·p X và Y, Y và Z, X và Z. Viášŋt cÃīng tháŧĐc phÃĒn táŧ cáŧ§a cÃĄc háŧĢp chášĨt tᚥo thà nh.
HÆ°áŧng dášŦn giášĢi:
1. CášĨu hÃŽnh electron cáŧ§a cÃĄc nguyÊn táŧ X, Y, Z:
X: (Z = 9) : 1s2 2s2 2p5
Y: (Z = 19) : 1s2 2s2 2p6 3s2 3p6 4s1
Z: (Z = 8) : 1s2 2s2 2p4
TÃnh chášĨt Äáš·c trÆ°ng cáŧ§a Y là tÃnh kim loᚥi, cáŧ§a X và Z là tÃnh phi kim.
2. LiÊn kášŋt giáŧŊa X và Y, giáŧŊa Y và Z là liÊn kášŋt ion.
- Sáŧą hÃŽnh thà nh liÊn kášŋt giáŧŊa X và Y:
X + 1e â X-
Y â Y+ + 1e
CÃĄc ion Y+ và X- hÚt nhau bášąng láŧąc hÚt tÄĐnh Äiáŧn, tᚥo thà nh háŧĢp chášĨt YX.
- Sáŧą hÃŽnh thà nh liÊn kášŋt giáŧŊa Y và Z:
Z + 2e â Z2-
2Y â 2Y+ + 21e
CÃĄc ion Y+ và Z2- hÚt nhau bášąng láŧąc hÚt tÄĐnh Äiáŧn, tᚥo thà nh háŧĢp chášĨt Y2Z.
- X và Z là cÃĄc phi kim nÊn liÊn kášŋt giáŧŊa chÚng là liÊn kášŋt cáŧng hÃģa tráŧ. Äáŧ Äᚥt ÄÆ°áŧĢc cášĨu hÃŽnh báŧn váŧŊng, máŧi nguyÊn táŧ X cᚧn gÃģp chung 1e, máŧi nguyÊn táŧ Z cᚧn gÃģp chung 2e. NhÆ° vášy 2 nguyÊn táŧ X sáš― tham gia liÊn kášŋt váŧi 1 nguyÊn táŧ Z bášąng 2 liÊn kášŋt cáŧng hÃģa tráŧ ÄÆĄn nháŧ 2 cáš·p electron gÃģp chung. Do ÄÃģ cÃīng tháŧĐc phÃĒn táŧ cáŧ§a háŧĢp chášĨt là X2Z.
Bà i 5: CÃĄc chášĨt trong dÃĢy nà o sau ÄÃĒy cháŧ cÃģ liÊn kášŋt cáŧng hoÃĄ tráŧ phÃĒn cáŧąc ?
A. HCl, KCl, HNO3, NO.
B. NH3, KHSO4, SO2, SO3.
C. N2, H2S, H2SO4, CO2.
D.CH4, C2H2, H3PO4, NO2.
HÆ°áŧng dášŦn giášĢi:
Dáŧąa và o hiáŧu Äáŧ ÃĒm Äiáŧn
â ÄÃĄp ÃĄn D
Bà i 6: Trong mᚥng tinh tháŧ kim cÆ°ÆĄng, gÃģc liÊn kášŋt tᚥo báŧi cÃĄc nguyÊn táŧ cacbon là :
A. 90o.
B. 120o.
C. 104o30'.
D. 109o28'.
HÆ°áŧng dášŦn giášĢi:
C (kim cÆ°ÆĄng) cÃģ lᚥi hÃģa sp3
â ÄÃĄp ÃĄn D
Bà i 7: R là máŧt nguyÊn táŧ phi kim. Táŧng Äᚥi sáŧ sáŧ oxi hÃģa dÆ°ÆĄng cao nhášĨt váŧi 2 lᚧn sáŧ oxi hÃģa ÃĒm thášĨp nhášĨt cáŧ§a R là +2. Táŧng sáŧ proton và nÆĄtron cáŧ§a R nháŧ hÆĄn 34.
1. XÃĄc Äáŧnh R
2. X là háŧĢp chášĨt khà cáŧ§a R váŧi hiÄro, Y là oxit cáŧ§a R cÃģ cháŧĐa 50% oxi váŧ kháŧi lÆ°áŧĢng. XÃĄc Äáŧnh cÃīng tháŧĐc phÃĒn táŧ cáŧ§a X và Y.
3. Viášŋt cÃīng tháŧĐc cášĨu tᚥo cÃĄc phÃĒn táŧ RO2; RO3; H2RO4.
HÆ°áŧng dášŦn giášĢi:
1. Gáŧi sáŧ oxi hÃģa dÆ°ÆĄng cao nhášĨt và sáŧ oxi hÃģa ÃĒm thášĨp nhášĨt cáŧ§a R lᚧn lÆ°áŧĢt là +m và -n.
Sáŧ oxi hÃģa cao nhášĨt cáŧ§a R trong oxit là +m nÊn áŧ láŧp ngoà i cÃđng nguyÊn táŧ R cÃģ m electron.
Sáŧ oxi hÃģa trong háŧĢp chášĨt cáŧ§a R váŧi hiÄro là -n nÊn Äáŧ Äᚥt ÄÆ°áŧĢc cášĨu hÃŽnh 8 electron bÃĢo hÃēa cáŧ§a khà hiášŋm, láŧp ngoà i cÃđng nguyÊn táŧ R cᚧn nhášn thÊm n electron.
Ta cÃģ: m + n = 8. Máš·t khÃĄc, theo bà i ra: +m + 2(-n) = +2 m - 2n = 2.
TáŧŦ ÄÃĒy tÃŽm ÄÆ°áŧĢc: m = 6 và n = 2. Vášy R là phi kim thuáŧc nhÃģm VI.
Sáŧ kháŧi cáŧ§a R < 34 nÊn R là O hay S. Do oxi khÃīng tᚥo ÄÆ°áŧĢc sáŧ oxi hÃģa cao nhášĨt là +6 nÊn R là lÆ°u huáŧģnh.
2. Trong háŧĢp chášĨt X, S cÃģ sáŧ oxi hÃģa thášĨp nhášĨt nÊn X cÃģ cÃīng tháŧĐc phÃĒn táŧ là H2S.
Gáŧi cÃīng tháŧĐc oxit Y là SOn.
Do %S = 50% nÊn n = 2. CÃīng tháŧĐc phÃĒn táŧ cáŧ§a Y là SO2.
3. CÃīng tháŧĐc cášĨu tᚥo cáŧ§a SO2; SO3; H2SO4:
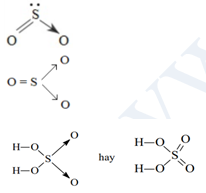
Bà i 8: Viášŋt cÃīng tháŧĐc cášĨu tᚥo cáŧ§a cÃĄc phÃĒn táŧ và ion sau: H2SO3, Na2SO4, HClO4
HÆ°áŧng dášŦn giášĢi:
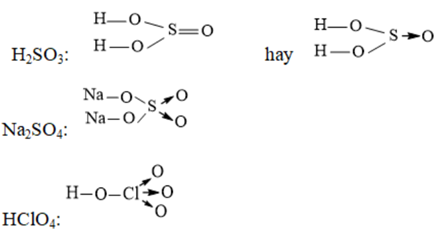
C. LUYáŧN TᚎP
CÃĒu 1 : Cháŧ ra náŧi dung sai khi nÃģi váŧ ion :
A. Ion là phᚧn táŧ mang Äiáŧn.
B. Ion ÃĒm gáŧi là cation, ion dÆ°ÆĄng gáŧi là anion.
C. Ion cÃģ tháŧ chia thà nh ion ÄÆĄn nguyÊn táŧ và ion Äa nguyÊn táŧ.
D. Ion ÄÆ°áŧĢc hÃŽnh thà nh khi nguyÊn táŧ nhÆ°áŧng hay nhášn electron.
CÃĒu 2 : Cho cÃĄc ion : Na+, Al3+, Ca2+, Clâ. Háŧi cÃģ bao nhiÊu cation ?
A. 2 B. 3 C. 4 D.5
CÃĒu 3 : Trong cÃĄc phášĢn áŧĐng hoÃĄ háŧc, nguyÊn táŧ kim loᚥi cÃģ khuynh hÆ°áŧng
A. nhášn thÊm electron.
B. Nhášn hay nhÆ°áŧng electron pháŧĨ thuáŧc và o táŧŦng phášĢn áŧĐng cáŧĨ tháŧ
C. NhÆ°áŧng báŧt electron.
D. Nhášn hay nhÆ°áŧng electron pháŧĨ thuáŧc và o táŧŦng kim loᚥi cáŧĨ tháŧ.
CÃĒu 4 : Trong phášĢn áŧĐng hoÃĄ háŧc, nguyÊn táŧ natri khÃīng hÃŽnh thà nh ÄÆ°áŧĢc
A.ion natri. B.cation natri. C.anion natri. D.ion ÄÆĄn nguyÊn táŧ natri.
CÃĒu 5 : Trong phášĢn áŧĐng : 2Na + Cl2 â 2NaCl, cÃģ sáŧą hÃŽnh thà nh
A. cation natri và clorua.
B. anion natri và clorua.
C.anion natri và cation clorua.
D. anion clorua và cation natri.
CÃĒu 6 : Hoà n thà nh náŧi dung sau : âBÃĄn kÃnh nguyÊn táŧ...(1) bÃĄn kÃnh cation tÆ°ÆĄng áŧĐng và ... (2) bÃĄn kÃnh anion tÆ°ÆĄng áŧĐngâ.
A.(1) : nháŧ hÆĄn, (2) : láŧn hÆĄn.
B. (1) : láŧn hÆĄn, (2) : nháŧ hÆĄn.
C. (1) : láŧn hÆĄn, (2) : bášąng.
D.(1) : nháŧ hÆĄn, (2) : bášąng.
CÃĒu 7 : Trong tinh tháŧ NaCl, xung quanh máŧi ion cÃģ bao nhiÊu ion ngÆ°áŧĢc dášĨu gᚧn nhášĨt ?
A.1 B.4 C.6 D.8
CÃĒu 8 : LiÊn kášŋt ion là liÊn kášŋt ÄÆ°áŧĢc hÃŽnh thà nh báŧi:
A. Sáŧą gÃģp chung cÃĄc electron Äáŧc thÃĒn.
B. sáŧą cho â nhášn cáš·p electron hoÃĄ tráŧ.
C.láŧąc hÚt tÄĐnh Äiáŧn giáŧŊa cÃĄc ion mang Äiáŧn trÃĄi dášĨu.
D. láŧąc hÚt tÄĐnh Äiáŧn giáŧŊa cÃĄc ion dÆ°ÆĄng và electron táŧą do.
CÃĒu 9 : Cháŧ ra náŧi dung sai khi nÃģi váŧ tÃnh chášĨt chung cáŧ§a háŧĢp chášĨt ion :
A. KhÃģ nÃģng chášĢy, khÃģ bay hÆĄi.
B. Táŧn tᚥi dᚥng tinh tháŧ, tan nhiáŧu trong nÆ°áŧc.
C. Trong tinh tháŧ cháŧĐa cÃĄc ion nÊn dášŦn ÄÆ°áŧĢc Äiáŧn.
D. CÃĄc háŧĢp chášĨt ion Äáŧu khÃĄ rášŊn.
CÃĒu 10 : Hoà n thà nh náŧi dung sau : âCÃĄc âĶâĶâĶ.... thÆ°áŧng tan nhiáŧu trong nÆ°áŧc. Khi nÃģng chášĢy và khi hoà tan trong nÆ°áŧc, chÚng dášŦn Äiáŧn, cÃēn áŧ trᚥng thÃĄi rášŊn thÃŽ khÃīng dášŦn Äiáŧnâ.
A. HáŧĢp chášĨt vÃī cÆĄ
B. HáŧĢp chášĨt háŧŊu cÆĄ
C. HáŧĢp chášĨt ion
D. HáŧĢp chášĨt cáŧng hoÃĄ tráŧ
CÃĒu 11 : Trong phÃĒn táŧ nà o sau ÄÃĒy cháŧ táŧn tᚥi liÊn kášŋt ÄÆĄn : N2, O2, F2, CO2 ?
A. N2 B. O2 C. F2 D.COÂÂ2
CÃĒu 12 : Cho cÃĄc phÃĒn táŧ : H2, CO2, Cl2, N2, I2, C2H4, C2H2. Bao nhiÊu phÃĒn táŧ cÃģ liÊn kášŋt ba trong phÃĒn táŧ ?
A.1 B. 2 C. 3 D.4
CÃĒu 13 : LiÊn kášŋt ÄÆ°áŧĢc tᚥo nÊn giáŧŊa hai nguyÊn táŧ bášąng máŧt hay nhiáŧu cáš·p electron chung, gáŧi là :
A.LiÊn kášŋt ion.
B.LiÊn kášŋt cáŧng hoÃĄ tráŧ.
C.LiÊn kášŋt kim loᚥi.
D.LiÊn kášŋt hiÄro.
CÃĒu 14 : Trong phÃĒn táŧ amoni clorua cÃģ bao nhiÊu liÊn kášŋt cáŧng hoÃĄ tráŧ ?
A.1 B.3. C.4. D.5
CÃĒu 15 : Trong mᚥng tinh tháŧ NaCl, cÃĄc ion Na+ và Clâ ÄÆ°áŧĢc phÃĒn báŧ luÃĒn phiÊn Äáŧu Äáš·n trÊn cÃĄc Äáŧnh cáŧ§a cÃĄc
A.HÃŽnh lášp phÆ°ÆĄng.
B.HÃŽnh táŧĐ diáŧn Äáŧu.
C.HÃŽnh chÃģp tam giÃĄc.
D.hÃŽnh lÄng tráŧĨ láŧĨc giÃĄc Äáŧu.
---(Náŧi dung Äᚧy Äáŧ§, chi tiášŋt táŧŦ cÃĒu 16 Äášŋn cÃĒu 40 cáŧ§a Äáŧ thi sáŧ 1 vui lÃēng xem tᚥi online hoáš·c ÄÄng nhášp Äáŧ tášĢi váŧ mÃĄy)---
ÄÃP ÃN PHášĶN LUYáŧN TᚎP
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
B |
C |
B |
C |
D |
B |
C |
C |
C |
C |
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
C |
B |
B |
C |
A |
A |
A |
C |
B |
C |
|
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
29 |
30 |
|
C |
A |
B |
A |
A |
B |
B |
D |
B |
B |
|
31 |
32 |
33 |
34 |
35 |
36 |
37 |
38 |
38 |
40 |
|
B |
A |
C |
B |
D |
B |
C |
A |
B |
B |
TrÊn ÄÃĒy là máŧt phᚧn trÃch dášŦn náŧi dung PhÆ°ÆĄng phÃĄp giášĢi cÃĄc dᚥng bà i tášp chÆ°ÆĄng liÊn kášŋt hÃģa háŧc nÄm 2021. Äáŧ xem toà n báŧ náŧi dung cÃĄc em ÄÄng nhášp và o trang hoc247.net Äáŧ tášĢi tà i liáŧu váŧ mÃĄy tÃnh.
Hy váŧng tà i liáŧu nà y sáš― giÚp cÃĄc em háŧc sinh Ãīn tášp táŧt và Äᚥt thà nh tÃch cao trong háŧc tášp.
ChÚc cÃĄc em háŧc táŧt!
Tà i liáŧu liÊn quan
TÆ° liáŧu náŧi bášt tuᚧn
- Xem thÊm




