Hướng dẫn giải bài tập SGK Cơ bản và sách Nâng cao chương trình Hóa học 11 Bài 13 Luyện tập Tính chất của nitơ, photpho và các hợp chất của chúng giúp các em học sinh lập phương trình hoá học; Viết phương trình hoàn thành dãy chuyển hoá và nhận biết các chất. Giải bài toán về hỗn hợp kim loại tác dụng với HNO3, tính nồng độ axit; bài tập axit photphoric tác dụng với dung dịch kiềm; bài toán về hỗn hợp kim loại, oxit tác dụng với HNO3, tính nồng độ axit; bài tập hiệu suất phản ứng phản ứng.
-
Bài tập 1 trang 61 SGK Hóa học 11
Hãy cho biết số oxi hóa của N và P trong các phân tử và ion sau đây: NH3, NH4+, NO2–, NO3–, NH4HCO3 , P2O3, PBr5, PO43–, KH2PO4, Zn3(PO4)2.
-
Bài tập 2 trang 61 SGK Hóa học 11
Trong các công thức sau đây, chọn công thức hóa học đúng của magie photphua:
A. Mg3(PO4)2
B. Mg(PO3)2
C. Mg3P2
D. Mg2P2O7
-
Bài tập 3 trang 61 SGK Hóa học 11
a) Lập các phương trình hóa học sau đây:
NH3 + Cl2 (dư) → Na + .. (1)
NH3(dư) + Cl2 → NH4Cl + …. (2)
NH3 + CH3COOH → … (3)
(NH4)3PO4 → H3PO4 + … (4)
Zn(NO3)2 → (5)
b) Lập các phương trình hóa học ở dạng phân tử và dạng ion rút gọn của phản ứng giữa các chất sau đây trong dung dịch:
K3PO4 và Ba(NO3)2 (1)
Na3PO4 và CaCl2 (2)
Ca(H2PO4)2 và Ca(OH)2 với tỉ lệ 1:1 (3)
(NH4)3PO4 + Ba(OH)2 (4)
-
Bài tập 4 trang 61 SGK Hóa học 11
Từ hiđro, clo, nitơ và các hóa chất cần thiết, hãy viết các phương trình hóa học (có ghi rõ điều kiện phản ứng) điều chế phân đạm amoni clorua.
- VIDEOYOMEDIA
-
Bài tập 5 trang 61 SGK Hóa học 11
Viết phương trình hóa học thực hiện các dãy chuyển hóa sau đây:
a)
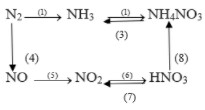
b)
.png)
-
Bài tập 6 trang 61 SGK Hóa học 11
Hãy đưa ra những phản ứng đã học có sự tham gia của đơn chất photpho, trong đó số oxi hóa của photpho.
a) Tăng
b) Giảm
-
Bài tập 7 trang 61 SGK Hóa học 12
Khi cho 3,00 g hỗn hợp Cu và Al tác dụng với dung dịch HNO3 đặc dư, đun nóng, sinh ra 4,48 lít khí duy nhất NO2 (đktc). Xác định phần trăm khối lượng của mỗi kim loại trong hỗn hợp?
-
Bài tập 8 trang 61 SGK Hóa học 12
Cho 6,00 g P2O5 vào 25,0 ml dung dịch H3PO4 6,00% (D = 1,03 g/ml). Tính nồng độ phần trăm H3PO4 trong dung dịch tạo thành?
-
Bài tập 9 trang 61 SGK Hóa học 12
Cần bón bao nhiêu kg phân đạm amoni nitrat chứa 97,5% NH4NO3 cho 10,0 hecta khoai tây, biết rằng 1,00 hecta khoai tây cần 60,0 kg nitơ?
-
Bài tập 13.1 trang 20 SBT Hóa học 11
Khí nitơ có thể được tạo thành trong các phản ứng hoá học nào sau đây ?
A. Đốt cháy NH3 trong oxi có mặt chất xúc tác platin
B. Nhiệt phân NH4NO3
C. Nhiệt phân AgNO3
D. Nhiệt phân NH4NO2
-
Bài tập 13.2 trang 20 SBT Hóa học 11
Cặp chất nào sau đây có thể tồn tại trong cùng một dung dịch ?
A. axit nitric và đồng(II) nitrat
B. đồng (II) nitrat và amoniac
C. bari hiđroxit và axit photphoric.
D. amoni hiđrophotphat và kali hiđroxit
-
Bài tập 13.3 trang 20 SBT Hóa học 11
Trong các phản ứng dưới đâu của amoniac, phản ứng nào không phải phản ứng oxi - hóa khử?
A. 4NH4 + 3O2 → 2N2 + 6H2O
B. 4NH3 + 5O2 → 4NO + 6H2O
C. 4NH3 + Cu(OH)2 → [Cu(NH3)2](OH)2
D. 2NH3 + 3Cl2 → N2 + 6HCl
-
Bài tập 13.4 trang 20 SBT Hóa học 11
Hoà tan 12,8 g kim loại hoá trị II trong một lượng vừa đủ dung dịch HNO3 60,0% (D = 1,365 g/ml), thu được 8,96 lít (đktc) một khí duy nhất màu nâu đỏ. Tên của kim loại và thể tích dung dịch HNO3 đã phản ứng là
A. đồng; 61,5 ml.
B. chì; 65,1 ml.
C. thuỷ ngân; 125,6 ml.
D. sắt; 82,3 ml.
-
Bài tập 13.5 trang 20 SBT Hóa học 11
Viết các phương trình hóa học thực hiện các dãy chuyển hóa sau:
-
Bài tập 13.6 trang 21 SBT Hóa học 11
Viết phương trình hoá học ở dạng phân tử và dạng ion rút gọn của phản ứng xảy ra trong dung dịch giữa các chất sau:
1. bari clorua và natri photphat.
2. axit photphoric và canxi hiđroxit, tạo ra muối axit ít tan.
3. axit nitric đặc, nóng và sắt kim loại.
4. natri nitrat, axit sunfuric loãng và đồng kim loại.
-
Bài tập 13.7 trang 21 SBT Hóa học 11
Có 4 lọ không dán nhãn đựng riêng biệt từng dung dịch loãng của các chất sau: H3PO4, BaCl2, Na2CO3, (NH4)2SO4. Chỉ được sử dụng dung dịch HCl, hãy nêu cách nhận biết chất đựng trong mỗi lọ. Viết phương trình hoá học của các phản ứng.
-
Bài tập 13.8 trang 21 SBT Hóa học 11
Cho các chất sau: 3Ca3(PO4)2.CaF2, H3PO4, NH4H2PO4, NaH2PO4, K3PO4, Ag3PO4. Hãy lập một dãy chuyển hoá biểu diễn mối quan hệ giữa các chất đó. Viết phương trình hoá học của các phản ứng thực hiện dãy chuyển hoá trên.
-
Bài tập 13.9 trang 21 SBT Hóa học 11
Rót dung dịch chứa 11,76 g H3PO4 vào dung dịch chứa 16,8 g KOH. Sau phản ứng cho dung dịch bay hơi đến khô. Tính khối lượng muối khan thu được.
-
Bài tập 1 trang 57 SGK Hóa học 11 nâng cao
Viết các Phương trình phản ứng hóa học để thực hiện các dãy chuyển hóa sau.
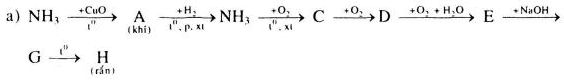
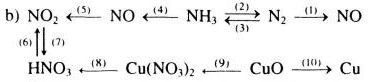
-
Bài tập 2 trang 58 SGK Hóa học 11 nâng cao
Chất khí A có mùi khai, phản ứng với khí clo theo cách khác nhau sau đây, tùy theo điều kiện phản ứng.
Trong trường hợp dư khí A thì xảy ra phản ứng:
8A + 3Cl2 → 6C + D
Chất rắn khô Chất khí
Trong trường hợp dư khí Clo xảy ra phản ứng:
2A + 3Cl2 → D(chất khí) + 6E
Chất rắn C màu trắng, khi đốt nó bị phân hủy thuận nghịch biến thành chất A và chất E. Khối lượng riêng của chất khí D là 1, 25 g/l (đktc). Hãy xác định các chất A, B, C, D, E và viết phương trình hóa học của các phản ứng.
-
Bài tập 3 trang 58 SGK Hóa học 11 nâng cao
Hãy chọn đáp án đúng trong các trường hợp sau:
a) Phản ứng giữa kim loại magie với axir nitric đặc giả thiết chỉ tạo ra đnitơ oxit. Tổng các hệ số trong phản ứng hóa học bằng.
A. 10
B. 18
C. 24
D. 20
b) Phản ứng giữa kim loại Cu với axit nitric đặc giả thiết chỉ tạo ra nito monoxit. Tổng các hệ số trong Phương trình hóa học bằng:
A. 10
B. 18
C. 24
D. 20
-
Bài tập 4 trang 58 SGK Hóa học 11 nâng cao
Bằng phản ứng hóa học, hãy nhận biết các dung dịch sau:
NH3, (NH4)2SO4, NH4Cl, Na2SO4. Viết các phương trình hóa học.
-
Bài tập 5 trang 58 SGK Hóa học 11 nâng cao
Trong quá trình tổng hợp ammoniac, áp suất trong bình phản ứng giảm đi 10,0% so với áp suất lúc ban đầu. biết nhịệt độ của phản ứng được giữa không đổi trước và sau phản ứng. Hãy xác định thành phần phần trăm thể tích của hỗn hợp khí thu được sau phản ứng, nếu trong hỗn hợp ban đầu lượng nitơ và hiđro được lấy đúng theo hệ số tỉ lượng.
-
Bài tập 1 trang 72 SGK Hóa học 11 nâng cao
Nêu những điểm khác biệt trong cấu tạo nguyên tử giữa nitơ và photpho
-
Bài tập 2 trang 72 SGK Hóa học 11 nâng cao
Lập các phương trình hóa học ở dạng phân tử và dạng ion rút gọn của các phản ứng xảy ra trong dung dịch của các chất.
a) Kali photphat và bari nitrat
b) natri photphat và nhôm sunfat
c) kali phot phat và canxi clorua
d) natri hiđrophotphat và natri hiđroxit.
e) canxi điphotphat (1) mol và canxi hiđroxit (1 mol)
g) canxi đihiđrophotphat (1mol) và canxi hiđroxit (2 mol)
-
Bài tập 3 trang 72 SGK Hóa học 11 nâng cao
Chọn công thức của apatit:
A. Ca3(PO4)2
B. Ca(PO3)2
C. 3Ca3(PO4)2CaF2
D. CaP2O7
-
Bài tập 4 trang 72 SGK Hóa học 11 nâng cao
Cho 44 gam NaOH vào dung dịch chứa 39,2 gam H3PO4, sau khi phản ứng xảy ra hoàn toàn, đem cô cạn dung dịch thu được đến cô cạn. Hỏi những muối nào được tạo nên và khối lượng muối khan thu được là bao nhiêu?
A. Na3PO4 và 50 gam.
B. Na2HPO4 và 15 gam.
C. NaH2PO4 và 49,2 gam, Na2HPO4 và 14,2 gam.
D. Na2HPO4 và 14,2 gam; Na3PO4 và 49,2 gam.
-
Bài tập 5 trang 72 SGK Hóa học 11 nâng cao
Thêm 10 gam dung dịch bão hòa bari hiđroxit (đo tan là 3,89 gam trong 100 gam nước) vào 0,5 ml dung dịch axit phot phoric nồng độ 6 mol/lít. Tính lượng các hợp chất của bari được tạo thành.