Học247 đã biên soạn và tổng hợp tư liệu Bộ 5 đề thi thử vào lớp 10 môn Hóa học năm 2021 Trường THPT Amsterdam. Hi vọng với bộ tư liệu này, các thí sinh sẽ dễ dàng đối chiếu đáp án bài làm của mình. Đồng thời, đây cũng là tư liệu bổ ích cho những thí sinh sẽ thi vào các năm học sau. Chúc các em đạt kết quả cao!
|
TRƯỜNG THPT CHUYÊN AMSTERDAM |
ĐỀ THI THỬ TUYỂN SINH VÀO LỚP 10 NĂM 2021 MÔN HÓA HỌC THỜI GIAN 50 PHÚ |
ĐỀ SỐ 1
Câu I.
1) Viết các phương trình phản ứng cho các thí nghiệm sau: đun nóng hỗn hợp benzen với brom có bột sắt làm xúc tác; đun nóng chất béo trong dung dịch NaOH (dư); điện phân dung dịch muối ăn có màng ngăn; cho khí H2S phản ứng với dung dịch FeCl3.
2) Ba chất A, B, C là những hợp chất hữu cơ có công thức phân tử: C5H8O2; C2H6O; C3H4O2. Chất A, C tác dụng được với Na. Chất A, B tác dụng được với NaOH. Chất A tác dụng với chất C thu được chất B. Xác định các chất A, B, C và viết phương trình phản ứng xảy ra.
Câu II.
1) Chỉ được dùng thêm giấy quỳ tím, hãy nhận biết các lọ đựng dung dịch hoá chất sau đã mất nhãn (viết các phương trình phản ứng xảy ra): BaCl2, NaCl, NaHSO4, NaAlO2, Na2CO3.
2) Chất A là muối của kim loại canxi; chất B là oxit; chất C và D là kim loại. Hãy chọn các chất thích hợp A, B, C, D và hoàn thành các phương trình phản ứng:
a) A + NaOH→ 2 muối + H2O
b) B + HCl → 2 muối + H2O
c) C + muối → 1 muối
d) D + muối → 2 muối
3) Cho khí etan (C2H6) đi qua chất xúc tác ở nhiệt độ cao thu được hỗn hợp khí X gồm 4 khí etilen, axetilen, hiđro, etan. Tỉ khối của X đối với khí etan là 0,4. Nếu cho 8,96 lít khí X (đktc) qua dung dịch brom (dư). Viết các phương trình phản ứng và tính khối lượng brom đã tham gia phản ứng.
Câu III.
1) Đốt cháy hoàn toàn 11,0 gam hỗn hợp X gồm: metan, etilen, axetilen thu được 12,6 gam nước. Mặt khác 20,16 dm3 (đktc) hỗn hợp X trên phản ứng tối đa với 176 gam Br2. Viết các phương trình phản ứng và tính thành phần phần trăm thể tích của mỗi chất trong hỗn hợp X.
2) Đun nóng m gam tinh bột trong dung dịch axit loãng thu được dung dịch X. Trung hòa lượng axit dư trong dung dịch X rồi chia thành 2 phần:
- Phần một đem thực hiện phản ứng tráng gương hoàn toàn thu được 21,6 gam Ag.
- Phần hai đem thực hiện phản ứng lên men rượu; toàn bộ lượng rượu thu được pha chế thành 12,5 ml rượu 46o. Cho kim loại Na (dư) tác dụng với 10 ml rượu này thu được V lít khí H2 (đktc). Viết các phương trình hóa học của các phản ứng đã xảy ra và tính m, V.
(Biết hiệu suất phản ứng thủy phân và phản ứng lên men đều đạt 80%; khối lượng riêng của rượu etylic là 0,8 g/ml, khối lượng riêng của nước là 1,0 g/ml).
Câu IV.
1) Nung hỗn hợp gồm a gam bột sắt và b gam bột S trong điều kiện không có không khí thu được chất rắn A. Cho A tác dụng với axit H2SO4 loãng (dư) thu được khí B có tỷ khối so với H2 bằng 10,6; dung dịch C còn lại 1,6 gam chất rắn không tan. Sục toàn bộ khí B vào dung dịch Pb(NO3)2 dư thu được 43,02 gam kết tủa. Viết phương trình phản ứng xảy ra và tính các giá trị a, b.
2) Cho m gam hỗn hợp X gồm 3 kim loại Al, Fe, Cu vào dung dịch CuSO4 (dư), sau khi các phản ứng xảy ra hoàn toàn thu được 17,6 gam kim loại. Nếu cũng hòa tan m gam hỗn hợp X vào 500 ml dung dịch HCl 1M đến khi phản ứng xảy ra hoàn toàn thu được 4,48 lít (đktc) khí H2, dung dịch Y và a gam chất rắn.
a) Viết các phương trình phản ứng xảy ra và tìm giá trị của a.
b) Cho từ từ dung dịch NaOH 1M vào dung dịch Y và khuấy đều đến khi bắt đầu kết tủa thì dùng hết V ml, cho tiếp dung dịch NaOH vào đến khi lượng kết tủa không đổi thì tổng thể tích NaOH 1M đã dùng là 600 ml. Tìm các giá trị m và V.
ĐÁP ÁN ĐỀ SỐ 1
Câu 1:
C6H6 + Br2 → C6H5Br + HBr
(RCOO)3C3H5 + 3NaOH → C3H5(OH)3 + 3RCOONa
2NaCl + 2H2O → Cl2 + 2NaOH + H2
2FeCl3 + H2S → 2FeCl2 + S + 2HCl
- Chất A tác dụng với Na và NaOH A là C3H4O2. Cấu tạo CH2=CHCOOH. Chất C tác dụng được với Na công thức chỉ có C2H6O. Cấu tạo CH3CH2OH. Chất B là C5H8O2, cấu tạo CH2=CHCOOC2H5
2CH2=CHCOOH + 2Na → 2CH2=CHCOONa + H2
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2
CH2=CHCOOH + NaOH → CH2=CHCOONa + H2O
CH2=CHCOOC2H5 + NaOH → CH2=CHCOONa + C2H5OH
Câu 2:
- Mẫu làm giấy quỳ chuyển màu đỏ là NaHSO4. Mẫu làm giấy quỳ chuyển màu xanh NaAlO2 và Na2CO3. Dung dịch không đổi màu BaCl2 và NaCl.
- Cho vài giọt dung dịch NaHSO4 vào 2 mẫu làm giấy quỳ có màu xanh. Nếu có khí bay ra là Na2CO3 ; có kết tủa là NaAlO2.
2NaHSO4 + Na2CO3 → 2Na2SO4 + CO2 + H2O
NaHSO4 + NaAlO2 + H2O→ Al(OH)3â + Na2SO4
- Lấy mẫu Na2CO3 vừa nhận được cho vào hai lọ còn lại nếu lọ nào có kết tủa là BaCl2 còn lại là NaCl
Na2CO3 + BaCl2 → BaCO3â + 2 NaCl
Ca(HCO3)2 + 2NaOH → CaCO3 + Na2CO3 + 2H2O
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
Fe + 2FeCl3 → 3FeCl2
Cu + 2FeCl3 → CuCl2 + 2FeCl2
C2H6 → C2H4 + H2 (1)
C2H6 → C2H2 + 2H2 (2)
C2H4 + Br2 → C2H4Br2 (3)
C2H2 + 2Br2 → C2H2Br4 (4)
dA/C2H6 = 0,4. Suy ra khối lượng hỗn hợp khí A là: MA = 0,4.30 =12 gam
Vì khối lượng không đổi nên: nC2H6 bđ.MC2H6 bđ = nA.MA
Ta có nA = 0,4 mol. Suy ra nC2H6 bđ = (0,4.12):30 = 0,16 mol
Từ (1), (2) nH2 tăng = 0,4 - 0,16 = 0,24 mol. Vậy ta có nBr2 = nH2 = 0,24 mol
Khối lượng Br2 = 0,24.160 = 38,4 gam
Câu 3:
CH4 + 2O2 → CO2 + 2H2O
C2H4 + 3O2 → 2CO2 + 2H2O
2C2H2 + 5O2 → 4CO2 + 2H2O
C2H4 + Br2 → C2H4Br2
C2H2 + 2Br2 → C2H2Br4
Gọi x, y, z lần lượt số mol của CH4, C2H4, C2H2 trong 11 gam hỗn hợp
Ta có hệ: 16x + 28y + 26 z = 11; 2x+ 2y + z = 0,7; 11x + 2y – 7z = 0
x = 0,1; y = 0,15; z = 0,2 mol
%VCH4= (0,1:0,45).100 = 22,22%; %VC2H4= 33,34%; %VC2H2= 44,44%
+ Phương trình: (-C6H10O5-)n + nH2O → nC6H12O6 (1)
Phần một: C6H12O6 + Ag2O → C6H12O7 + 2Ag (2)
Phần hai: C6H12O6 → 2C2H5OH + 2CO2 (3)
2Na + 2H2O → 2NaOH + 2H2 (4)
2Na + 2C2H5OH → 2C2H5ONa + 2H2 (5)
+ Tính m: Từ (2) nC6H12O6 = 1/2nAg = 0,1 mol → mC6H12O6 ở (2) = 18,0 gam
Theo bài ra VC2H5OH nguyên chất = 12,5.46/100 = 5,75 ml
Suy ra mC2H5OH = 5,75.0,8 gam/lit = 4,6 gam.
Suy ra mC6H12O6 ở (3) tham gia thuỷ phân = 9.100/80 = 11,25 gam
Tổng khối lượng glucozơ ở (1) = 18 + 11,25 = 29,25 gam.
Khối lượng m = 26,325 x100/80 = 32,90625 gam
+ Tính V: nH2 = ½(nH2O + nC2H5OH) = 0,2375 mol
Thể tích khí H2 ở 12,5 ml: V = 0,2375x22,4 = 5,32 lít
Cho vào 10 ml thì VH2 giải phóng là: (10.5,32):12,5 = 4,256 lít
Câu 4:
1. Fe + S → FeS (1)
FeS + H2SO4 FeSO4 + H2S (2)
MB = 2.10,6 = 21,2
B có M < 21,2 là H2. Chất rắn A là Fe (dư)
Fe + H2SO4 → Fe SO4 + H2 (3)
H2S + Pb(NO3)2 → PbS + 2HNO3 (4)
Theo (4) nH2S = nPbS = 43,02: 239 = 0,18(mol)
Số mol H2 trong B là x . Ta có: \(\frac{{2x + 34.0,18}}{{x + 0,18}}\) = 21,2 x = 0,12
a = (0,12 + 0,18).56 = 16,8 (gam)
b = 1,6 + 0,18.32 = 7,36 (gam)
2. a)
2Al + 3CuSO4 →Al2(SO4)3 + 3Cu (1)
Fe + CuSO4 → FeSO4 + Cu (2)
2Al + 6HCl → 2AlCl3 + 3H2 (3)
Fe + 2HCl → FeCl2 + H2 (4)
Ta có nH2 = 0,2 mol. Suy ra số mol HCl đã phản ứng 0,4 mol ; HCl còn dư, Al, Fe phản ứng hết.
Theo các phương trình phản ứng :
n H2 (3,4) = n Cu sinh ra (1, 2) = 0,2 mol
Khối lượng Cu trong hỗn hợp ban đầu = 17,6 - 64.0,2 = 4,8 gam.
b) Trong dung dịch có 0,1 mol HCl dư
NaOH + HCl → NaCl + H2O (5)
FẹCl2 + 2NaOH → Fe(OH)2 + 2NaCl (6)
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl (7)
NaOH + Al(OH)3 → Na AlO2 + 2H2O (8)
V = 0,1 : 1 = 0,1 lít = 100 ml
Tổng số mol NaOH đã dùng = 1.0,6 = 0,6 mol
Từ phương trình (3,4,5,6,7). nNaOH đã dùng = Số mol HCl = 0,5 mol.
Số mol NaOH (5,6,7) = Số mol HCl = 0,5 mol
Số mol NaOH ở (8) = 0,6 - 0,5 = 0,1 mol
Ta có nAl = n Al(OH)3 = n NaOH(8) = 0,1 mol
Theo (3), (4). Số mol của Fe = nH2(4) = 0,2 - 1,5.nAl = 0,2 - 0,15 = 0,05 mol.
Vậy m = 0,1.27 + 0,05.56 + 4,8 = 10,3 gam
ĐỀ SỐ 2
Câu 1: Nêu hiện tượng và viết phương trình hóa học xảy ra(nếu có)khi tiến hành các thí nghiệm sau:
a. Cho mẫu kim loại Na vào dung dịch CuCl2.
b. Cho mẫu đá vôi vào dung dịch KHSO4
c. Cho từ từ dung dịch NaOH đến dư vào dung dịch AlCl3
d. Cho canxicacbua vào nước
e. Đun nóng tinh bột trong dung dịch axit H2SO4 loãng, thu được dung dịch X. Cho X vào dung dịch AgNO3 trong NH3 dư, đun nóng nhẹ.
g. Cho lòng trắng trứng vào rượu etylic.
Câu 2:
a. Từ quặng pirit sắt, natri clorua, oxi, nước, hãy viết các phương trình hóa học điều chế các chất: FeSO4,FeCl2, FeCl3, sắt III hiđroxit, Na2SO3, NaHSO4.
b. Hòa tan 0,8 gam hỗn hợp gồm một kim loại hóa trị II và một kim loại hóa trị III cần dùng 34 ml dung dịch HCl 2M.
+ Cô cạn dung dịch sau phản ứng thì thu được bao nhiêu gam muối khan.
+ nếu kim loại hóa trị III là Al và có số mol bằng 5 lần số mol của kim loại hóa trị II thì kim loại hóa trị II là kim loại nào?
Câu 3: Nhiệt phân hoàn toàn một lượng MgCO3 sau một thời gian thu được chất rắn A và khí B. Hấp thụ hết khí B bằng dung dịch NaOH thu được dung dịch C. Dung dịch C vừa tác dụng được với BaCl2, vừa tác dụng được với KOH. Hòa tan chất rắn A bằng dung dịch axit sunfuric loãng, dư thu được khí B và dung dịch D.Xác định thành phần của A, B, C, D và viết các phương trình hóa học
Câu 4: Nung 93,9 gam hỗn hợp X gồm Fe3O4 và Al trong môi trường chân không. Sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp Y. chia Y làm 2 phần:
- Phần 1: cho tác dụng với dung dịch NaOH dư thu được 1.344 lít H2
- Phần 2: cho tác dụng với dung dịch HCl dư thu được 14.112 lít H2 biết các khí đo ở đktc. Tính khối lượng các chất trong hỗn hợp X.
Câu 5:
a. Cho 20 ml rượu etylic 230 tác dụng vừa đủ với kim loại Na. Tính khối lượng chất rắn thu được sau phản ứng. Biết khối lượng riêng của rượu là 0.8g/ml, của nước là 1g/ml.
b. Đốt cháy hoàn toàn chất hữu cơ X (Mx<78) chứa C, H, O, N thu được CO2, H2O và N2. Biết số mol H2O bằng 1,75 lần số mol CO2; tổng số mol CO2 và H2O bằng 2 lần số mol O2 tham gia phản ứng. Xác định công thức phân tử và đề nghị một công thức cấu tạo của X.
---(Nội dung đầy đủ, chi tiết phần đáp án của đề thi số 2 vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐỀ SỐ 3
Câu I:
1. Cho lần lượt từng chất: Fe, BaO, Al2O3 và KOH vào lần lượt các dung dịch: NaHSO4, CuSO4. Hãy viết các phương trình phản ứng xảy ra.
2. Một hỗn hợp gồm Al, Fe, Cu và Ag. Bằng phương pháp hoá học hãy tách rời hoàn toàn các kim loại ra khỏi hỗn hợp trên.
3. Có 5 lọ mất nhãn đựng 5 dung dịch: NaOH, KCl, MgCl2, CuCl2, AlCl3. Hãy nhận biết từng dung dịch trên mà không dùng thêm hoá chất khác. Viết các phương trình phản ứng xảy ra.
Câu II:
1. Hiđrocacbon X là chất khí (ở nhiệt độ phòng, 250C). Nhiệt phân hoàn toàn X (trong điều kiện không có oxi) thu được sản phẩm C và H2, trong đó thể tích khí H2 thu được gấp đôi thể tích khí X (đo ở cùng điều kiện). Xác định các công thức phân tử thỏa mãn X.
2. Ba chất hữu cơ mạch hở A, B, C có công thức phân tử tương ứng là: C3H6O, C3H4O2, C6H8O2. Chúng có những tính chất sau:
- Chỉ A và B tác dụng với Na giải phóng khí H2.
- Chỉ B và C tác dụng được với dung dịch NaOH.
- A tác dụng với B (trong điều kiện xúc tác, nhiệt độ thích hợp) thu được sản phẩm là chất C.
Hãy cho biết công thức cấu tạo của A, B, C. Viết các phương trình phản ứng xảy ra.
3. Metan bị lẫn một ít tạp chất là CO2, C2H4, C2H2. Trình bày phương pháp hoá học để loại hết tạp chất khỏi metan.
Câu III:
1. Hòa tan hoàn toàn 0,297 gam hỗn hợp Natri và một kim loại thuộc nhóm IIA trong bảng tuần hoàn các nguyên tố hóa học vào nước. Ta được dung dịch X và 56 ml khí Y (đktc). Xác định kim loại thuộc nhóm IIA và khối lượng của mỗi kim loại trong hỗn hợp.
2. Hỗn hợp X gồm ba kim loại Al, Fe, Cu.
Cho m gam hỗn hợp X vào dung dịch CuSO4 (dư) sau khi phản ứng xảy ra hoàn toàn thu được 35,2 gam kim loại. Nếu cũng hòa tan m gam hỗn hợp X vào 500 ml dung dịch HCl 2M đến khi phản ứng xảy ra hoàn toàn thu được 8,96 lít khí H2 (đktc), dung dịch Y và a gam chất rắn.
a. Viết các phương trình phản ứng xảy ra và tìm giá trị của a.
b. Cho từ từ dung dịch NaOH 2M vào dung dịch Y và khuấy đều đến khi thấy bắt đầu xuất hiện kết tủa thì dùng hết V1 lít dung dịch NaOH 2M, tiếp tục cho tiếp dung dịch NaOH vào đến khi lượng kết tủa không có sự thay đổi nữa thì lượng dung dịch NaOH 2M đã dùng hết 600 ml. Tìm các giá trị m và V1.
Câu IV:
1. Từ tinh bột, các hóa chất vô cơ và điều kiện cần thiết khác có đủ. Viết phương trình hóa học điều chế Etyl axetat ( ghi rõ điều kiện nếu có).
2. Có a gam hỗn hợp X gồm một axit no đơn chức A và một este B. B tạo ra bởi một axit no đơn chức A1 và một rượu no đơn chức C (A1 là đồng đẳng kế tiếp của A). Cho a gam hỗn hợp X tác dụng với lượng vừa đủ NaHCO3, thu được 1,92 gam muối. Nếu cho a gam hỗn hợp X tác dụng với một lượng vừa đủ NaOH đun nóng thu được 4,38 gam hỗn hợp hai muối của 2 axit A, A1 và 1,38 gam rượu C, tỷ khối hơi của C so với hiđro là 23. Đốt cháy hoàn toàn 4,38 gam hỗn hợp hai muối của A, A1 bằng một lượng oxi dư thì thu được Na2CO3, hơi nước và 2,128 lit CO2 (đktc). Giả thiết phản ứng xảy ra hoàn toàn.
a. Tìm công thức phân tử, công thức cấu tạo của A, A1, C, B.
b. Tính a.
---(Nội dung đầy đủ, chi tiết phần đáp án của đề thi số 3 vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐỀ SỐ 4
Câu 1:
1. Thế nào là độ tan ? Nêu ảnh hưởng của nhiệt độ đến độ tan của chất rắn và chất khí. Lập biểu thức liên hệ giữa độ tan và nồng độ phần trăm của dung dịch bão hòa.
2. Pha chế 35,8 gam dung dịch CuSO4 bão hòa ở 100oC . Đun nóng dung dịch này cho đến khi có 17,86 gam nước bay hơi, sau đó để nguội đến 20oC. Tính số gam tinh thể CuSO4.5H2O kết tinh. Biết rằng độ tan của CuSO4 ở 20oC và 100oC lần lượt là 20,7g và 75,4 g.
Câu 2: Các công thức C2H6O, C3H8O và C3H6O2 là công thức phân tử của 5 chất hữu cơ đơn chức, mạch hở A, B, C, D, E trong đó :
- Tác dụng với Na chỉ có A và E.
- Tác dụng với dung dịch NaOH có B, D và E.
- D tác dụng với dung dịch NaOH thì thu được F mà F tác dụng với A lại tạo C.
1. Xác định CTPT của A, B, C, D và E. Viết các CTCT của chúng .
2. Viết các phương trình phản ứng xảy ra.
Câu 3:
1. Dẫn hỗn hợp khí gồm C2H2, CO2 và SO2 cho qua dung dịch X chữa một chất tan thấy có Y duy nhất thoát ra. Hỏi chất tan trong dung dịch X có tính chất gì ? Dùng hai chất có tính chất khác nhau để viết ptpư minh họa.
2. Hỗn hợp Z gồm hai hiđrocacbon điều kiện thường ở thể khí và có số nguyên tử cacbon bằng nhau. Đốt cháy hoàn toàn Z thu được 3,52 gam CO2 và 1,62 gam H2O . Tìm CTPT của hai hiđrocacbon biết trong hỗn hợp Z chúng có số mol bằng nhau.
Câu 4: Dung dịch A chứa H2SO4, FeSO4 và MSO4, dung dịch B chứa NaOH 0,5M và BaCl2. Để trung hòa 200ml dung dịch A cần dùng vừa đủ 40ml dung dịch B. Mặt khác khi cho 200ml dung dịch A tác dụng với 300ml dung dịch B thì thu được dung dịch C và 21,07g kết tủa D gồm một muối và hai hiđroxit. Để trung hòa dung dịch C cần 40ml dung dịch HCl 0,25M . Cho biết trong dung dịch C vẫn còn BaCl2 dư.
1. Xác định kim loại M biết rằng nguyên tử khối của M lớn hơn nguyên tử khối của Na.
2. Tính CM của từng chất trong dung dịch A.
Câu 5: Chất hữu cơ X có công thức RCOOH và Y có công thức R'(OH)2 trong đó R và R' là các gốc hiđrocacbon mạch hở. Hỗn hợp A vừa trộn gồm X và Y, chia A thành hai phần bằng nhau, mỗi phần chứa tổng số mol hai chất là 0,05 mol.
- Phần 1: Cho tác dụng với Na dư được 0,08 gam khí.
- Phần 2: Đốt cháy hoàn toàn được 3,136 lít khí CO2 (đktc) và 2,7 gam nước .
1. Tìm CTPT của X, Y.
2. Viết CTCT của X và Y, gọi tên chúng.
---(Nội dung đầy đủ, chi tiết phần đáp án của đề thi số 4 vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐỀ SỐ 5
Câu 1:
1. Cho hỗn hợp A gồm Al, Cu, Fe3O4 vào dung dịch H2SO4 đặc, nóng dư, thu được dung dịch B, khí SO2 thoát ra. Nếu cho hỗn hợp A vào dung dịch HCl dư thu được dung dịch C, chất rắn không tan D và khí E. Cho dung dịch NaOH dư vào dung dịch C thu được kết tủa F. Nung F ngoài không khí đến khối lượng không đổi thu được chất rắn G, cho khí CO dư qua G nung nóng đến khối lượng không đổi thu được chất rắn H.
Xác định các chất có trong B, C, D, E, F, G, H và viết các phương trình phản ứng xảy ra.
2. Cho 5 dung dịch không màu đựng trong 5 bình mất nhãn gồm: NaHSO4, NaCl, Mg(HCO3)2, Na2CO3, Ba(HCO3)2. Không được dùng thêm hoá chất nào khác, hãy nêu phương pháp nhận biết các dung dịch trên.
Câu 2:
1. Viết các phương trình phản ứng thực hiện sơ đồ chuyển hoá sau (ghi rõ điều kiện phản ứng nếu có).
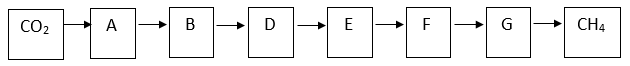
2. Từ than đá, đá vôi và các chất vô cơ cần thiết, viết phương trình phản ứng điều chế các chất PVC (Polivinylclorua), PE (Polietilen).
3. X, Y là hai chất hữu cơ đơn chức, mạch hở (trong phân tử chỉ chứa C, H, O) có khối lượng mol phân tử bằng 74 g/mol. X tác dụng được với cả Na, NaOH; Y chỉ tác dụng với dung dịch NaOH, không tác dụng với Na. Viết công thức cấu tạo có thể có của X, Y và viết các phương trình phản ứng xảy ra ở trên.
Câu 3:
1. Cho 122,4g hỗn hợp X gồm Cu, Fe3O4 vào dung dịch H2SO4 đặc, nóng thu được 10,08 lít SO2 (đktc), dung dịch Y và còn lại 4,8g kim loại. Cô cạn dung dịch Y thu được m gam muối khan. Tính m.
2. Để điều chế 100 lít rượu etylic 460 cần dùng m kg gạo. Biết rằng, trong gạo chứa 80% tinh bột; khối lượng riêng C2H5OH bằng 0,8 g/ml và hiệu suất toàn bộ quá trình điều chế đạt 75%. Tính m.
Câu 4:
1. Cho 16g hỗn hợp X gồm bột Mg, Fe vào 600 ml dung dịch AgNO3 có nồng độ C (mol/l), khuấy đều hỗn hợp để phản ứng xảy ra hoàn toàn, thu được dung dịch Y và 70,4g chất rắn Z. Cho dung dịch NaOH dư vào dung dịch Y thu được kết tủa, nung kết tủa trong không khí ở nhiệt cao đến khối lượng không đổi thu được 16g chất rắn T. Viết các phương trình phản ứng xảy ra, tính khối lượng từng kim loại trong hỗn hợp X và tính giá trị C.
2. Tiến hành hai thí nghiệm:
- Thí nghiệm 1: Cho 650ml dung dịch NaOH 2M vào 400ml dung dịch AlCl3 a(M) thì thu được 3b gam kết tủa.
- Thí nghiệm 2: Cho 700ml dung dịch NaOH 2M vào 400ml dung dịch AlCl3 a(M) thì thu được 2b gam kết tủa.
Tìm a, b.
Câu 5: Hỗn hợp X gồm 2 este có tỉ lệ số mol trong hỗn hợp là 1:3. Cho a gam hỗn hợp X vào dung dịch NaOH dư, sau phản ứng thu được 4,92g muối của một axit hữu cơ đơn chức và 3,18g hỗn hợp 2 rượu no, đơn chức, mạch thẳng (có số nguyên tử C < 5). Nếu đốt cháy hết 3,18g hỗn hợp 2 rượu thu được 3,36 lít CO2 (đktc). Biết các phản ứng xảy ra hoàn toàn.
1. Xác định công thức cấu tạo 2 este, viết các phương trình phản ứng xảy ra.
2. Tính a.
---(Nội dung đầy đủ, chi tiết phần đáp án của đề thi số 5 vui lòng xem tại online hoặc đăng nhập để tải về máy)---
Trên đây là phần trích dẫn nội dung Bộ 5 đề thi thử vào lớp 10 môn Hóa học năm 2021 có đáp án Trường THPT Amsterdam, để xem nội dung đềy đủ, chi tiết vuii lòng truy cập vào hệ thống hoc247.net!
Ngoài ra các em học sinh có thể tham khảo thêm một số tài liệu cùng chuyên mục khác tại đây:
- Bộ 5 đề thi thử vào lớp 10 môn Hóa học năm 2021 có đáp án Trường THPT Tiểu La
- Bộ 5 đề thi thử vào lớp 10 môn Hóa học năm 2021 có đáp án Trường THPT Lý Thường Kiệt
- Bộ 5 đề thi thử vào lớp 10 môn Hóa học năm 2021 có đáp án Trường THPT Phan Đình Phùng
Chúc các em học tập tốt!
Tài liệu liên quan
Tư liệu nổi bật tuần
-
Đề thi minh họa môn Hóa học tốt nghiệp THPT năm 2025
22/10/20242065 -
Đề thi minh họa môn Tin học tốt nghiệp THPT năm 2025
22/10/2024761 -
Đề thi minh họa môn Toán tốt nghiệp THPT năm 2025
22/10/20241478 - Xem thêm




