─Éß║┐n vß╗øi nß╗Öi dung t├│m tß║»t l├¢ thuyß║┐t v├á b├ái tß║¡p minh hoß║í B├ái 11: Muß╗æi m├┤n Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t nß╗æi tri thß╗®c ─æã░ß╗úc ─æß╗Öi ng┼® bi├¬n tß║¡p cß╗ºa HOC247 tß╗òng hß╗úp v├á r├║t gß╗ìn, c├íc em sß║¢ ─æã░ß╗úc t├¼m hiß╗âu vß╗ü kh├íi niß╗çm, t├¡nh tan, t├¡nh chß║Ñt ho├í hß╗ìc v├á ─æiß╗üu chß║┐ muß╗æi. Mß╗Øi c├íc em c├╣ng tham khß║úo.
Tóm tắt lÛ thuyết
1.1. Khái niệm
| Phß║ún ß╗®ng tß║ío muß╗æi l├á qu├í tr├¼nh tß║ío ra muß╗æi tß╗½ sß╗▒ kß║┐t hß╗úp giß╗»a cation kim loß║íi v├á anion gß╗æc acid th├┤ng qua phß║ún ß╗®ng giß╗»a acid v├á kim loß║íi hoß║Àc oxide base. |
- C├íc phß║ún ß╗®ng tß║ío muß╗æi trong bß║úng 11.1 ─æß╗üu c├│ th├ánh phß║ºn ph├ón tß╗¡ gß╗ôm cation kim loß║íi v├á anion gß╗æc acid.
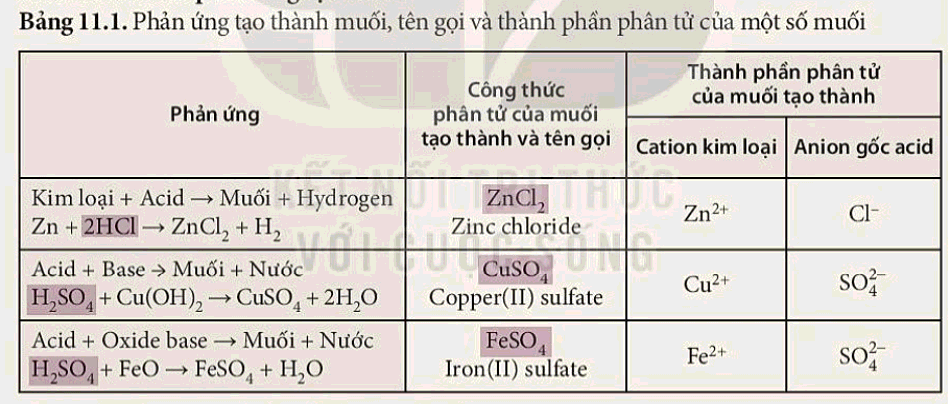
- Nhß║¡n x├®t vß╗ü c├ích gß╗ìi t├¬n muß╗æi
+ Muß╗æi ─æã░ß╗úc ─æß║Àt t├¬n theo quy tß║»c:
|
T├¬n kim loß║íi (ho├í trß╗ï, ─æß╗æi vß╗øi kim loß║íi nhiß╗üu ho├í trß╗ï) + t├¬n gß╗æc acid. |
- Thành phần phân tử của muối gồm cation kim loại và anion gốc acid.
1.2. Tính tan của muối
- ─Éa sß╗æ c├íc muß╗æi l├á chß║Ñt rß║»n, c├│ muß╗æi kh├┤ng tan hoß║Àc tan ├¡t trong nã░ß╗øc. C├íc bß║úng t├¡nh tan ─æã░ß╗úc x├óy dß╗▒ng ─æß╗â tiß╗çn sß╗¡ dß╗Ñng.
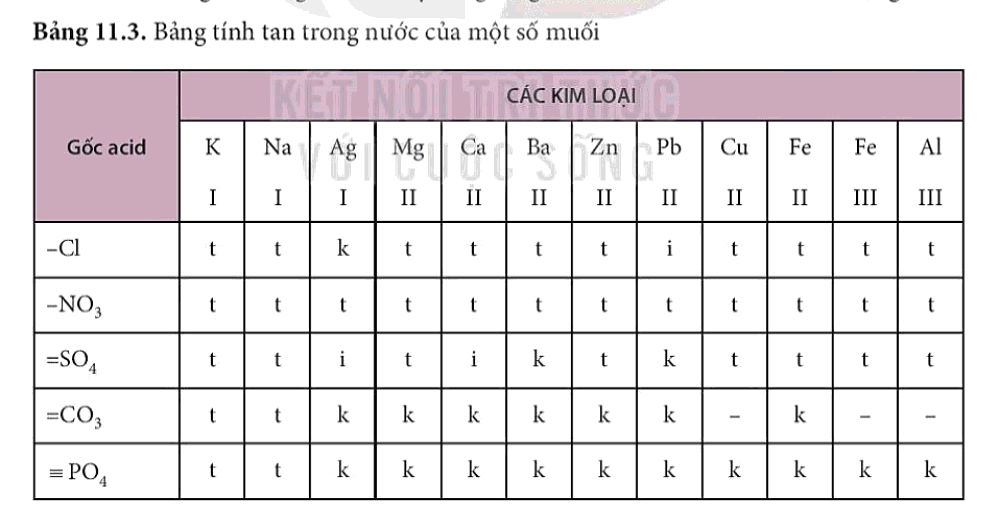
1.3. Tính chất hoá học
- Dung dß╗ïch muß╗æi c├│ thß╗â t├íc dß╗Ñng vß╗øi mß╗Öt sß╗æ kim loß║íi tß║ío th├ánh muß╗æi mß╗øi v├á kim loß║íi mß╗øi.
- Muß╗æi c├│ thß╗â t├íc dß╗Ñng vß╗øi mß╗Öt sß╗æ dung dß╗ïch acid tß║ío th├ánh muß╗æi mß╗øi v├á acid mß╗øi, sß║ún phß║®m cß╗ºa phß║ún ß╗®ng c├│ thß╗â l├á chß║Ñt ├¡t tan hoß║Àc kh├┤ng tan.
- Dung dß╗ïch muß╗æi t├íc dß╗Ñng vß╗øi dung dß╗ïch base.
- Dung dß╗ïch muß╗æi t├íc dß╗Ñng vß╗øi dung dß╗ïch base tß║ío th├ánh muß╗æi mß╗øi v├á base mß╗øi, trong ─æ├│ c├│ ├¡t nhß║Ñt mß╗Öt sß║ún phß║®m l├á chß║Ñt khi/chß║Ñt ├¡t tan/kh├┤ng tan.
- Dung dß╗ïch muß╗æi t├íc dß╗Ñng vß╗øi dung dß╗ïch muß╗æi.
- Hai dung dß╗ïch muß╗æi t├íc dß╗Ñng vß╗øi nhau tß║ío th├ánh hai muß╗æi mß╗øi, trong ─æ├│ ├¡t nhß║Ñt c├│ mß╗Öt muß╗æi kh├┤ng tan hoß║Àc ├¡t tan.
1.4. Điều chế
- Muß╗æi c├│ thß╗â ─æiß╗üu chß║┐ bß║▒ng mß╗Öt sß╗æ phã░ãíng ph├íp nhã░ sau:
+ Dung dß╗ïch acid t├íc dß╗Ñng vß╗øi base.
+ Dung dß╗ïch acid t├íc dß╗Ñng vß╗øi muß╗æi.
+ Oxide acid t├íc dß╗Ñng vß╗øi dung dß╗ïch base.
Bài tập minh họa
Bài 1. Hãy kể tên một số tính chất hoá học của muối.
Hã░ß╗øng dß║½n giß║úi
- Dung dß╗ïch muß╗æi c├│ thß╗â t├íc dß╗Ñng vß╗øi mß╗Öt sß╗æ kim loß║íi tß║ío th├ánh muß╗æi mß╗øi v├á kim loß║íi mß╗øi.
- Muß╗æi c├│ thß╗â t├íc dß╗Ñng vß╗øi mß╗Öt sß╗æ dung dß╗ïch acid tß║ío th├ánh muß╗æi mß╗øi v├á acid mß╗øi, sß║ún phß║®m cß╗ºa phß║ún ß╗®ng c├│ thß╗â l├á chß║Ñt ├¡t tan hoß║Àc kh├┤ng tan.
- Dung dß╗ïch muß╗æi t├íc dß╗Ñng vß╗øi dung dß╗ïch base.
- Dung dß╗ïch muß╗æi t├íc dß╗Ñng vß╗øi dung dß╗ïch base tß║ío th├ánh muß╗æi mß╗øi v├á base mß╗øi, trong ─æ├│ c├│ ├¡t nhß║Ñt mß╗Öt sß║ún phß║®m l├á chß║Ñt khi/chß║Ñt ├¡t tan/kh├┤ng tan.
- Dung dß╗ïch muß╗æi t├íc dß╗Ñng vß╗øi dung dß╗ïch muß╗æi.
- Hai dung dß╗ïch muß╗æi t├íc dß╗Ñng vß╗øi nhau tß║ío th├ánh hai muß╗æi mß╗øi, trong ─æ├│ ├¡t nhß║Ñt c├│ mß╗Öt muß╗æi kh├┤ng tan hoß║Àc ├¡t tan.
B├ái 2. Nß║┐u chß╗ë d├╣ng dung dß╗ïch NaOH th├¼ c├│ thß╗â ph├ón biß╗çt ─æã░ß╗úc 2 dung dß╗ïch muß╗æi trong mß╗ùi cß║Àp chß║Ñt sau:
A. Na2SO4 và Fe2(SO4)3
B. Na2SO4 và K2SO4
C. Na2SO4 và BaCl2
D. Na2CO3 và K3PO4
Hã░ß╗øng dß║½n giß║úi
Chß╗ë d├╣ng dung dß╗ïch NaOH th├¼ c├│ thß╗â ph├ón biß╗çt ─æã░ß╗úc 2 dung dß╗ïch muß╗æi Na2SO4 v├á Fe2(SO4)3 do mß╗Öt ß╗æng nghiß╗çm xuß║Ñt hiß╗çn kß║┐t tß╗ºa n├óu ─æß╗Å (─æß╗Å n├óu) Fe(OH)3 c├▓n lß║íi Na2SO4 kh├┤ng c├│ hiß╗çn tã░ß╗úng g├¼.
3NaOH + FeCl3  Fe(OH)3 + 3NaCl
Luyß╗çn tß║¡p B├ái 11 Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t Nß╗æi Tri Thß╗®c
Học xong bài học này, em có thể:
- N├¬u ─æã░ß╗úc kh├íi niß╗çm vß╗ü muß╗æi; mß╗Öt sß╗æ phã░ãíng ph├íp ─æiß╗üu chß║┐ muß╗æi; mß╗æi quan hß╗ç giß╗»a acid, base, oxide v├á muß╗æi.
- Chß╗ë ra ─æã░ß╗úc mß╗Öt sß╗æ muß╗æi tan v├á muß╗æi kh├┤ng tan tß╗½ bß║úng t├¡nh tan.
- ─Éß╗ìc ─æã░ß╗úc t├¬n mß╗Öt sß╗æ loß║íi muß╗æi th├┤ng dß╗Ñng.
- Quan s├ít qua video th├¡ nghiß╗çm muß╗æi phß║ún ß╗®ng vß╗øi kim loß║íi, vß╗øi acid, vß╗øi base, vß╗øi muß╗æi; n├¬u v├á giß║úi th├¡ch ─æã░ß╗úc hiß╗çn tã░ß╗úng xß║úy ra trong th├¡ nghiß╗çm (viß║┐t phã░ãíng tr├¼nh ho├í hß╗ìc) v├á r├║t ra kß║┐t luß║¡n vß╗ü t├¡nh chß║Ñt ho├í hß╗ìc cß╗ºa muß╗æi.
3.1. Trß║»c nghiß╗çm B├ái 11 Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t Nß╗æi Tri Thß╗®c
C├íc em c├│ thß╗â hß╗ç thß╗æng lß║íi nß╗Öi dung kiß║┐n thß╗®c ─æ├ú hß╗ìc ─æã░ß╗úc th├┤ng qua b├ái kiß╗âm tra Trß║»c nghiß╗çm KHTN 8 Kß║┐t nß╗æi tri thß╗®c B├ái 11 cß╗▒c hay c├│ ─æ├íp ├ín v├á lß╗Øi giß║úi chi tiß║┐t.
-
- A. 1
- B. 2
- C. 3
- D. 4
-
- A. Na2SO4.
- B. Na2CO3.
- C. NaCl.
- D. Na2S
-
- A. Có kết tủa trắng xanh.
- B. Có khí thoát ra.
- C. Có kết tủa đỏ nâu.
- D. Kết tủa màu trắng.
C├óu 4-10: Mß╗Øi c├íc em ─æ─âng nhß║¡p xem tiß║┐p nß╗Öi dung v├á thi thß╗¡ Online ─æß╗â cß╗ºng cß╗æ kiß║┐n thß╗®c vß╗ü b├ái hß╗ìc n├áy nh├®!
3.2. B├ái tß║¡p SGK B├ái 11 Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t Nß╗æi Tri Thß╗®c
C├íc em c├│ thß╗â xem th├¬m phß║ºn hã░ß╗øng dß║½n Giß║úi b├ái tß║¡p KHTN 8 Kß║┐t nß╗æi tri thß╗®c B├ái 11 ─æß╗â gi├║p c├íc em nß║»m vß╗»ng b├ái hß╗ìc v├á c├íc phã░ãíng ph├íp giß║úi b├ái tß║¡p.
Mß╗ƒ ─æß║ºu trang 48 SGK Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t nß╗æi tri thß╗®c ÔÇô KNTT
Hoß║ít ─æß╗Öng trang 48 SGK Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t nß╗æi tri thß╗®c ÔÇô KNTT
Giß║úi C├óu hß╗Åi 1 trang 49 SGK Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t nß╗æi tri thß╗®c ÔÇô KNTT
Giß║úi C├óu hß╗Åi 2 trang 49 SGK Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t nß╗æi tri thß╗®c ÔÇô KNTT
Giß║úi C├óu hß╗Åi 3 trang 49 SGK Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t nß╗æi tri thß╗®c ÔÇô KNTT
Hoß║ít ─æß╗Öng trang 50 SGK Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t nß╗æi tri thß╗®c ÔÇô KNTT
Giß║úi C├óu hß╗Åi trang 51 SGK Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t nß╗æi tri thß╗®c ÔÇô KNTT
Giß║úi C├óu hß╗Åi trang 52 SGK Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t nß╗æi tri thß╗®c ÔÇô KNTT
Hß╗Åi ─æ├íp B├ái 11 Khoa hß╗ìc tß╗▒ nhi├¬n 8 Kß║┐t Nß╗æi Tri Thß╗®c
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Khoa học tự nhiên HOC247 sẛ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!








