V·ªõi mong mu·ªën ƒëem ƒë·∫øn cho c√°c em h·ªçc sinh nhi·ªÅu t√Ýi li·ªáu √¥n t·∫≠p, HOC247 xin g·ª≠i ƒë·∫øn B·ªô 5 ƒë·ªÅ thi th·ª≠ THPT QG m√¥n H√≥a h·ªçc nƒÉm 2021 c√≥ ƒë√°p √°n Tr∆∞·ªùng THPT An L∆∞∆°ng. Hi v·ªçng t√Ýi li·ªáu s·∫Ω gi√∫p c√°c em h·ªçc t·∫≠p th·∫≠t t·ªët.
|
TR∆Ø·ªúNG THPT AN L∆Ø∆ÝNG |
ĐỀ THI THỬ THPT QG NĂM 2021 MÔN HÓA HỌC THỜI GIAN 50 PHÚT |
ĐỀ SỐ 1
Câu 1. Dung dịch A có \(\left[ {{H^ + }} \right] = {10^{ - 3}}\)M sẽ có môi trường
A. Trung tính.
B. Axit.
C. Baz∆°.
D. Không xác định.
C√¢u 2. Cho d√£y c√°c ch·∫•t sau: \(NaOH,{\rm{ }}HN{O_3}\),\({\rm{ }}Ba{\left( {OH} \right)_2}\),\({\rm{ }}HCl{O_4},{\rm{ }}C{H_3}COOH\),\({\rm{ }}N{H_3}\). S·ªë axit, baz∆° l·∫ßn l∆∞·ª£t l√Ý
A. 3 v√Ý 3.
B. 5 v√Ý 2.
C. 4 v√Ý 3.
D. 3 v√Ý 4.
C√¢u 3. Kh√≠ \({N_2}\) kh√° tr∆° ·ªü nhi·ªát ƒë·ªô th∆∞·ªùng l√Ý do
A. N có bán kính nguyên tử nhỏ, phân tử \({N_2}\) không phân cựC.
B. Nguyên tử N có độ âm điện lớn nhất trong nhóm VA.
C. Trong phân tử \({N_2}\), mỗi nguyên tử còn 1 cặp electron chưa liên kết.
D. Trong phân tử \({N_2}\) chứa liên kết ba rất bền.
C√¢u 4. Trong c√°c ph·∫£n ·ª©ng sau, ph·∫£n ·ª©ng n√Ýo \(N{H_3}\) kh√¥ng th·ªÉ hi·ªán t√≠nh kh·ª≠?
A. \(4N{H_3} + 5{O_2} \to 4NO + 6{H_2}O\).
B. \(N{H_3} + HCl \to N{H_4}Cl\).
C. \(8N{H_3} + 3C{l_2} \to 6N{H_4}Cl + {N_2}\).
D. \(2N{H_3} + 3CuO \to 3Cu + 3{H_2}O + {N_2}\).
C√¢u 5. Nung n√≥ng m gam b·ªôt s·∫Øt ngo√Ýi kh√¥ng kh√≠, sau ph·∫£n ·ª©ng thu ƒë∆∞·ª£c 36 gam h·ªón h·ª£p X g·ªìm \(Fe,{\rm{ }}FeO\),\({\rm{ }}F{e_2}{O_3} v√Ý F{e_3}{O_4}\). H√≤a tan h·∫øt X trong dung d·ªãch \(HN{O_3}\) lo√£ng thu ƒë∆∞·ª£c 5,6 l√≠t h·ªón h·ª£p kh√≠ Y g·ªìm \(NO v√Ý N{O_2}\) c√≥ t·ªâ kh·ªëi so v·ªõi \({H_2}\) l√Ý 19. Gi√° tr·ªã m l√Ý
A. 16.
B. 32.
C. 28.
D. 20.
C√¢u 6. Cacbon v√¥ ƒë·ªãnh h√¨nh v√Ý than ch√¨ l√Ý hai d·∫°ng th√π h√¨nh c·ªßa nhau v√¨
A. Có tính chất vật lí tương tự nhau.
B. Đều do nguyên tố cacbon tạo nên.
C. Có cấu tạo mạng tinh thể giống nhau.
D. Chúng có tính chất hoá học không giống nhau.
Câu 7. Dẫn hơi nước qua than nóng đỏ thì thu được V lít (đktc) hỗn hợp khí X gồm \(C{O_2}, CO, {H_2}\); tỉ khối hơi của X so với \({H_2}\)
l√Ý 7,8. Cho to√Ýn b·ªô V l√≠t h·ª£p kh√≠ X ·ªü tr√™n kh·ª≠ v·ª´a ƒë·ªß 24 gam h·ªón h·ª£p \(CuO, F{e_2}{O_3}\) nung n√≥ng, thu ƒë∆∞·ª£c r·∫Øn Y ch·ªâ c√≥ 2 kim lo·∫°i. Cho to√Ýn b·ªô Y v√Ýo dung d·ªãch HCl d∆∞ th·∫•y c√≥ 4,48 l√≠t \({H_2}\) bay ra (ƒëktc). Gi√° tr·ªã c·ªßa V l√Ý
A. 10,08.
B. 11,20.
C. 13,44.
D. 8,96.
Câu 8. Ankan Y phản ứng với clo tạo ra 2 dẫn xuất monoclo có tỉ khối hơi so với \({H_2}\) bằng 39,25.
T√™n c·ªßa Y l√Ý
A. Butan.
B. Propan.
C. iso-butan.
D. 2-metylbutan.
C√¢u 9. ƒê·ªët ch√°y ho√Ýn to√Ýn m·ªôt h·ª£p ch·∫•t h·ªØu c∆° X (C, H, N) b·∫±ng l∆∞·ª£ng kh√¥ng kh√≠ v·ª´a ƒë·ªß (g·ªìm 1/5 th·ªÉ t√≠ch \({O_2}\), c√≤n l·∫°i l√Ý \({N_2}\)) ƒë∆∞·ª£c kh√≠ \(C{O_2}, {H_2}O v√Ý {N_2}\). Cho to√Ýn b·ªô s·∫£n ph·∫©m ch√°y qua b√¨nh ƒë·ª±ng dung d·ªãch \(Ba{\left( {OH} \right)_2}\) d∆∞ th·∫•y c√≥ 39,4 gam k·∫øt t·ªßa, kh·ªëi l∆∞·ª£ng dung d·ªãch gi·∫£m ƒëi 24,3 gam. Kh√≠ tho√°t ra kh·ªèi b√¨nh c√≥ th·ªÉ t√≠ch 34,72 l√≠t (ƒëktc). Bi·∫øt \({d_{X/{O_2}}} < 2\). C√¥ng th·ª©c ph√¢n t·ª≠ c·ªßa X l√Ý
A. \({C_2}{H_7}N.\)
B. \({C_2}{H_8}N\).
C. \({C_2}{H_7}{N_2}\).
D. \({C_2}{H_4}{N_2}\).
C√¢u 10. Nung n√≥ng 100 gam h·ªón h·ª£p g·ªìm \(N{a_2}C{O_3}\) v√Ý \(NaHC{O_3}\) cho ƒë·∫øn kh·ªëi l∆∞·ª£ng kh√¥ng ƒë·ªïi c√≤n l·∫°i 69 gam ch·∫•t r·∫Øn. Th√Ýnh ph·∫ßn % kh·ªëi l∆∞·ª£ng m·ªói ch·∫•t trong h·ªón h·ª£p ban ƒë·∫ßu l√Ý
A. 63% v√Ý 37%.
B. 84% v√Ý 16%.
C. 42% v√Ý 58%.
D. 21% v√Ý 79%.
C√¢u 11. D·∫´n lu·ªìng kh√≠ CO qua h·ªón h·ª£p \(A{l_2}{O_3},{\rm{ }}CuO\),\({\rm{ }}MgO,{\rm{ }}F{e_2}{O_3}\) (n√≥ng) sau khi ph·∫£n ·ª©ng x·∫£y ra ho√Ýn to√Ýn thu ƒë∆∞·ª£c ch·∫•t r·∫Øn g·ªìm
A. \(A{l_2}{O_3},{\rm{ }}Cu,{\rm{ }}Mg,{\rm{ }}Fe.\)
B. \(Al,{\rm{ Fe,}}Cu,{\rm{ }}Mg.\)
C. \(A{l_2}{O_3},{\rm{ }}Cu,MgO,Fe\) .
D. \(A{l_2}{O_3},{\rm{ }}F{e_2}{O_3},{\rm{ }}Cu,{\rm{ }}MgO.\)
C√¢u 12. C√≥ hai dung d·ªãch, m·ªói dung d·ªãch ƒë·ªÅu ch·ª©a hai cation v√Ý hai anion kh√¥ng tr√πng nhau trong c√°c ion sau:
\({K^ + }:0,15{\rm{ }}mol\), \(M{g^{2 + }}{\rm{: 0,1 mol, }}\)\(NH_4^ + :0,25{\rm{ }}mol;{\rm{ }}{H^ + }:0,2{\rm{ }}mol\);\({\rm{ }}C{l^ - }:0,1{\rm{ }}mol;{\rm{ }}SO_4^{2 - }:0,075{\rm{ }}mol\);\({\rm{ }}NO_3^ - :0,25{\rm{ }}mol\) v√Ý \(CO_3^{2 - }:0,15{\rm{ }}mol\). M·ªôt trong hai dung d·ªãch tr√™n ch·ª©a
A. \({K^ + },{\rm{ }}M{g^{2 + }}\),\({\rm{ }}SO_4^{2 - },{\rm{ }}C{l^ - }\).
B. \({K^ + },{\rm{ }}NH_4^ + \),\({\rm{ C}}O_3^{2 - },{\rm{ }}C{l^ - }\).
C. \(NH_4^ + ,{\rm{ }}{H^ + }\),\({\rm{ }}NO_3^ - ,{\rm{ }}SO_4^{2 - }\).
D. \(M{g^{2 + }},{\rm{ }}{{\rm{H}}^ + }\),\({\rm{ }}SO_4^{2 - },{\rm{ }}C{l^ - }\).
C√¢u 13. Lo·∫°i thu·ª∑ tinh kh√≥ n√≥ng ch·∫£y ch·ª©a 18,43% \({K_2}O\); 10,98% \(CaO\) v√Ý 70,59% \(Si{O_2}\) c√≥ c√¥ng th·ª©c d∆∞·ªõi d·∫°ng c√°c oxit l√Ý
A. \({K_2}O.CaO.4Si{O_2}\).
B. \({K_2}O.2CaO.6Si{O_2}\).
C. \({K_2}O.CaO.6Si{O_2}\).
D. \({K_2}O.3CaO.8Si{O_2}\).
C√¢u 14. Trong c√°c ph·∫£n ·ª©ng c·ªßa Si v·ªõi \(C{l_2},{\rm{ }}{F_2},{\rm{ }}{O_2},{\rm{ }}HN{O_3}\) ƒë·∫∑c n√≥ng, dung d·ªãch NaOH, Mg. S·ªë ph·∫£n ·ª©ng m√Ý trong ƒë√≥ Si th·ªÉ hi·ªán t√≠nh oxi h√≥a l√Ý
A. 5.
B. 4.
C. 3.
D. 1.
C√¢u 15. Oxi ho√° h·∫øt 2,2 gam h·ªón h·ª£p hai ancol ƒë∆°n ch·ª©c th√Ýnh anƒëehit c·∫ßn v·ª´a ƒë·ªß 4,8 gam CuO. Cho to√Ýn b·ªô l∆∞·ª£ng anƒëehit tr√™n t√°c d·ª•ng v·ªõi l∆∞·ª£ng d∆∞ dung d·ªãch \(AgN{O_3}\) trong \(N{H_3}\), thu ƒë∆∞·ª£c 23,76 gam Ag. Hai ancol l·∫ßn l∆∞·ª£t l√Ý :
A. \(C{H_3}OH,{\rm{ }}{C_2}{H_5}C{H_2}OH.\)
B. \(C{H_3}OH,{\rm{ }}{C_2}{H_5}OH.\)
C. \({C_2}{H_5}OH,{\rm{ }}{C_3}{H_7}C{H_2}OH.\)
D. \({C_2}{H_5}OH,{\rm{ }}{C_2}{H_5}C{H_2}OH.\)
Câu 16. Thực hiện các thí nghiệm sau đây:
(1) S·ª•c kh√≠ \({C_2}{H_4}\) v√Ýo dung d·ªãch \(KMn{O_4}\).
(2) Cho \(NaHC{O_3}\) v√Ýo dung d·ªãch \(C{H_3}COOH\).
(3) Chi·∫øu s√°ng h·ªón h·ª£p kh√≠ metan v√Ý clo.
(4) Cho glucozơ tác dụng với \(Cu{\left( {OH} \right)_2}\) ở điều kiện thường. 
(5) Đun etanol với \({H_2}S{O_4}\) đặc ở \(140^\circ C\).
(6) ƒêun n√≥ng h·ªón h·ª£p triolein v√Ý hiƒëro (v·ªõi x√∫c t√°c Ni).
(7) Cho phenol tác dụng với dung dịch NaOH.
(8) Cho anilin tác dụng với dung dịch brom.
(9) Cho metyl amin tác dụng với dung dịch \(FeC{l_3}\).
(10) Cho glixerol tác dụng với NA.
Nh·ªØng th√≠ nghi·ªám x·∫£y ra ph·∫£n ·ª©ng oxi ho√° - kh·ª≠ l√Ý
A. 5.
B. 3.
C. 4.
D. 6.
C√¢u 17. Este X ƒë∆°n ch·ª©c t√°c d·ª•ng v·ªõi NaOH ƒëun n√≥ng thu ƒë∆∞·ª£c mu·ªëi Y c√≥ c√¥ng th·ª©c ph√¢n t·ª≠ l√Ý \({C_3}{H_5}{O_2}Na\) v√Ý r∆∞·ª£u \({Y_1}\). Oxi h√≥a \({Y_1}\) b·∫±ng CuO nung n√≥ng thu ƒë∆∞·ª£c anƒëehit \({Y_2}\). \({Y_2}\) t√°c d·ª•ng v·ªõi \(A{g_2}O\) d∆∞, ƒëun n√≥ng thu ƒë∆∞·ª£c s·ªë mol Ag g·∫•p 4 l·∫ßn s·ªë mol \({Y_2}\). V·∫≠y t√™n g·ªçi c·ªßa X l√Ý
A. etyl propionat
B. metyl propionat.
C. metyl axetat.
D. propyl propionat.
C√¢u 18. Dung d·ªãch X ch·ª©a 0,01 mol \(Cl{H_3}N - C{H_2} - COOH\); 0,02 mol \(C{H_3} - CH\left( {N{H_2}} \right) - COOH\); 0,05 mol \(HCOO{C_6}{H_5}\). Cho dung d·ªãch X t√°c d·ª•ng v·ªõi 160 ml dung d·ªãch KOH 1M ƒëun n√≥ng ƒë·ªÉ ph·∫£n ·ª©ng x·∫£y ra ho√Ýn to√Ýn. C√¥ c·∫°n dung d·ªãch sau ph·∫£n ·ª©ng thu ƒë∆∞·ª£c m gam ch·∫•t r·∫Øn khan. Gi√° tr·ªã c·ªßa m l√Ý
A. 16,335 gam.
B. 8,615 gam.
C. 12,535 gam.
D. 14,515 gam.
C√¢u 19. Trung ho√Ý ho√Ýn to√Ýn 8,88 gam m·ªôt amin (b·∫≠c m·ªôt, m·∫°ch cacbon kh√¥ng ph√¢n nh√°nh) b·∫±ng axit HCl, t·∫°o ra 17,64 gam mu·ªëi. Amin c√≥ c√¥ng th·ª©c l√Ý
A. \({H_2}NC{H_2}C{H_2}C{H_2}C{H_2}N{H_2}\).
B. \(C{H_3}C{H_2}C{H_2}N{H_2}\).
C. \({H_2}NC{H_2}C{H_2}N{H_2}\).
D. \({H_2}NC{H_2}C{H_2}C{H_2}N{H_2}\).
C√¢u 20. Ph√°t bi·ªÉu n√Ýo sau ƒë√¢y kh√¥ng ƒë√∫ng?
A. Tinh b·ªôt l√Ý polime c√≥ c·∫•u tr√∫c d·∫°ng m·∫°ch ph√¢n nh√°nh v√Ý kh√¥ng ph√¢n nh√°nh.
B. Tinh b·ªôt kh√¥ng tan trong n∆∞·ªõc l·∫°nh. Trong n∆∞·ªõc n√≥ng t·ª´ \(65^\circ C\) tr·ªü l√™n, tinh b·ªôt chuy·ªÉn th√Ýnh dung d·ªãch keo nh·ªõt.
C. Tinh bột không phản ứng với dung dịch \({H_2}S{O_4}\) loãng, đun nóng.
D. Etanol có thể được sản xuất bằng phương pháp lên men các nông sản chứa nhiều tinh bột.
C√¢u 21. Th·ªßy ph√¢n ho√Ýn to√Ýn 7,02 gam h·ªón h·ª£p X g·ªìm glucoz∆° v√Ý saccaroz∆° trong dung d·ªãch \({H_2}S{O_4}\) thu ƒë∆∞·ª£c dung d·ªãch Y. Trung h√≤a h·∫øt l∆∞·ª£ng axit d∆∞ trong dung d·ªãch Y r·ªìi cho ph·∫£n ·ª©ng ·ª©ng ho√Ýn to√Ýn v·ªõi l∆∞·ª£ng d∆∞ dung d·ªãch \(AgN{O_3}\) trong \(N{H_3}\) th√¨ thu ƒë∆∞·ª£c 8,64 gam Ag. Th√Ýnh ph·∫ßn % v·ªÅ kh·ªëi l∆∞·ª£ng c·ªßa saccaroz∆° trong h·ªón h·ª£p X l√Ý
A. 97,14%.
B. 24,35%.
C. 12,17%.
D. 48,71%.
C√¢u 22. Ti·∫øn h√Ýnh hai th√≠ nghi·ªám sau:
- Thí nghiệm 1:
B∆∞·ªõc 1: Cho v√Ýo ·ªëng nghi·ªám 1 gi·ªçt dung d·ªãch \(CuS{O_4}\) b√£o h√≤a + 2 ml dung d·ªãch NaOH 30%.‚ÄÉ
Bước 2: Lắc nhẹ, gạn lớp dung dịch để giữ kết tủA.
B∆∞·ªõc 3: Th√™m kho·∫£ng 4 ml l√≤ng tr·∫Øng tr·ª©ng v√Ýo ·ªëng nghi·ªám, d√πng ƒë≈©a th·ªßy tinh khu·∫•y ƒë·ªÅu.
- Thí nghiệm 2:
B∆∞·ªõc 1: L·∫•y kho·∫£ng 4 ml l√≤ng tr·∫Øng tr·ª©ng cho v√Ýo ·ªëng nghi·ªám.
Bước 2: Nhỏ từng giọt khoảng 3 ml dung dịch \(CuS{O_4}\) bão hòA.
B∆∞·ªõc 3: Th√™m kho·∫£ng 5 ml dung d·ªãch NaOH 30% v√Ý khu·∫•y ƒë·ªÅu.
Ph√°t bi·ªÉu n√Ýo sau ƒë√¢y sai?
A. Các phản ứng ở các bước 3 xảy ra nhanh hơn khi các ống nghiệm được đun nóng.
B. Sau b∆∞·ªõc 3 ·ªü c·∫£ hai th√≠ nghi·ªám, h·ªón h·ª£p thu ƒë∆∞·ª£c sau khi khu·∫•y xu·∫•t hi·ªán m√Ýu t√≠m.
C. Sau b∆∞·ªõc 2 ·ªü th√≠ nghi·ªám 2, xu·∫•t hi·ªán k·∫øt t·ªßa m√Ýu xanh.
D. Sau b∆∞·ªõc 1 ·ªü th√≠ nghi·ªám 1, trong ·ªëng nghi·ªám xu·∫•t hi·ªán k·∫øt t·ªßa m√Ýu xanh.
C√¢u 23. Cho c√°c polime sau: T∆° t·∫±m, t∆° visco, t∆° axetat, t∆° nitron, cao su buna-S, poli vinylclorua, poli vinylaxetat, nh·ª±a novolac. S·ªë polime c√≥ ch·ª©a nguy√™n t·ªë oxi trong ph√¢n t·ª≠ l√Ý
A. 4.
B. 5.
C. 3.
D. 6.
C√¢u 24. Cho m gam h·ªón h·ª£p X g·ªìm Na v√Ý K (t·ªâ l·ªá mol 1:1) v√Ýo 500 ml dung d·ªãch ch·ª©a h·ªón h·ª£p g·ªìm \(A{l_2}{\left( {S{O_4}} \right)_3} 0,5M\) v√Ý \({H_2}S{O_4} 1M\) sau khi ph·∫£n ·ª©ng x·∫£y ra ho√Ýn to√Ýn thu ƒë∆∞·ª£c dung d·ªãch Y. Cho dung d·ªãch Y t√°c d·ª•ng v·ªõi 1,5 l√≠t dung d·ªãch HCl 1M, sau khi ph·∫£n ·ª©ng x·∫£y ra ho√Ýn to√Ýn thu ƒë∆∞·ª£c 23,4 gam k·∫øt t·ªßa. Gi√° tr·ªã nh·ªè nh·∫•t c·ªßa m l√Ý
A. 130,2 gam.
B. 27,9 gam.
C. 105,4 gam.
D. 74,4 gam.
C√¢u 25. Nh√∫ng m·ªôt thanh Al n·∫∑ng 20 gam v√Ýo 400 ml dung d·ªãch \(CuC{l_2}\) 0,5M. Khi n·ªìng ƒë·ªô dung d·ªãch \(CuC{l_2}\) gi·∫£m 25% th√¨ l·∫•y thanh Al ra kh·ªèi dung d·ªãch, gi·∫£ s·ª≠ t·∫•t c·∫£ Cu tho√°t ra b√°m v√Ýo thanh Al. Kh·ªëi l∆∞·ª£ng thanh Al sau ph·∫£n ·ª©ng l√Ý
A. 21,15 gam.
B. 21,88 gam.
C. 22,02 gam.
D. 22,3 gam.
C√¢u 26. ƒêi·ªán ph√¢n 100 ml dung d·ªãch \(CuS{O_4} 0,2M\) v·ªõi c∆∞·ªùng ƒë·ªô d√≤ng ƒëi·ªán 9,65A. Bi·∫øt hi·ªáu su·∫•t ƒëi·ªán ph√¢n l√Ý 100%. Kh·ªëi l∆∞·ª£ng Cu b√°m v√Ýo catot khi th·ªùi gian ƒëi·ªán ph√¢n \({t_1} = 200\left( s \right) v√Ý {t_2} = 500\left( s \right)\) l√Ý
A. 0,32 gam v√Ý 0,64 gam.
B. 0,64 gam v√Ý 1,62 gam.
C. 0,64 gam v√Ý 1,28 gam.
D. 0,64 gam v√Ý 3,25 gam.
Câu 27. Cho 2 phản ứng sau:
(1) \(Cu + 2Fe{{Cl}_3} \rightarrow Cu{{Cl}_2} + 2Fe{{Cl_2}}\)
(2) \(Fe + Cu{{Cl}_2} \rightarrow Fe{{Cl}_2} + Cu\)
K·∫øt lu·∫≠n n√Ýo d∆∞·ªõi ƒë√¢y l√Ý ƒë√∫ng?
A. Tính oxi hoá của \(C{u^{2 + }} > F{e^{3 + }} > F{e^{2 + }}\).
B. Tính oxi hoá của \(F{e^{3 + }} > C{u^{2 + }} > F{e^{2 + }}\).
C. Tính khử của \(Cu > F{e^{2 + }} > Fe\).
D. Tính khử của \(F{e^{2 + }} > Fe > Cu\).
C√¢u 28. Ho√Ý tan m·ªôt l∆∞·ª£ng Fe v√Ýo dung d·ªãch \({H_2}S{O_4}\) lo√£ng th·∫•y tho√°t ra \({V_1}\) , l√≠t kh√≠ \({H_2}\). M·∫∑t kh√°c n·∫øu ho√Ý tan c√πng m·ªôt l∆∞·ª£ng Fe tr√™n v√Ýo dung d·ªãch \({H_2}S{O_4}\) ƒë·∫∑c n√≥ng th·∫•y tho√°t ra \({V_2}\) l√≠t kh√≠ \(S{O_2}\) (c√°c th·ªÉ t√≠ch ƒëo ·ªü c√πng ƒëi·ªÅu ki·ªán). M·ªëi quan h·ªá gi·ªØa \({V_1}\) v√Ý \({V_2} \)l√Ý
A. \({V_1} = 2{V_2}\).
B. \(2{V_1} = {V_2}\).
C. \({V_1} = {V_2}\).
D. \(3{V_1} = 2{V_2}\).
C√¢u 29. Nung m gam b·ªôt s·∫Øt trong oxi, thu ƒë∆∞·ª£c 4,5 gam h·ªón h·ª£p ch·∫•t r·∫Øn X. H√≤a tan h·∫øt h·ªón h·ª£p X trong dung d·ªãch \({H_2}S{O_4}\) ƒë·∫∑c n√≥ng (d∆∞) tho√°t ra 1,26 l√≠t (ƒëktc) \(S{O_2}\) (l√Ý s·∫£n ph·∫©m kh·ª≠ duy nh·∫•t).
Gi√° tr·ªã c·ªßa m l√Ý
A. 3,78.
B. 2,22.
C. 2,52.
D. 2,32.
C√¢u 30. Cho m gam h·ªón h·ª£p b·ªôt X g·ªìm \(F{e_x}{O_y}, CuO v√Ý Cu\) (x, y nguy√™n d∆∞∆°ng) v√Ýo 600 ml dung d·ªãch HCl 1M, thu ƒë∆∞·ª£c dung d·ªãch Y (kh√¥ng ch·ª©a HCl) v√Ý c√≤n l·∫°i 6,4 gam kim lo·∫°i kh√¥ng tan. Cho Y t√°c d·ª•ng v·ªõi l∆∞·ª£ng d∆∞ dung d·ªãch \(AgN{O_3}\), thu ƒë∆∞·ª£c 102,3 gam k·∫øt t·ªßA. Bi·∫øt c√°c ph·∫£n ·ª©ng ƒë·ªÅu x·∫£y ra ho√Ýn to√Ýn. Gi√° tr·ªã c·ªßa m g·∫ßn nh·∫•t v·ªõi gi√° tr·ªã n√Ýo sau ƒë√¢y?
A. 22,7.
B. 34,1.
C. 29,1.
D. 27,5.
Câu 31. Cho hình sau:
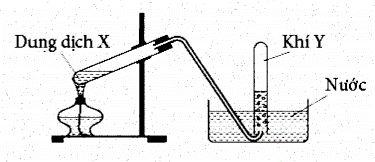
H√¨nh v·∫Ω tr√™n m√¥ t·∫£ th√≠ nghi·ªám ƒëi·ªÅu ch·∫ø kh√≠ n√Ýo sau ƒë√¢y
A. \({C_2}{H_2}.\)
B. \(C{H_4}\).
C. \({C_2}{H_4}\).
D. \(N{H_3}\).
C√¢u 32. Trong khi l√Ým c√°c th√≠ nghi·ªám ·ªü l·ªõp ho·∫∑c trong c√°c gi·ªù th·ª±c h√Ýnh h√≥a h·ªçc c√≥ m·ªôt s·ªë kh√≠ th·∫£i: \(C{l_2},{\rm{ }}{H_2}S\),\({\rm{ }}S{O_2}\),\({\rm{ }}N{O_2},{\rm{ }}HCl\). Bi·ªán ph√°p ƒë√∫ng d√πng ƒë·ªÉ kh·ª≠ c√°c kh√≠ tr√™n l√Ý
A. Dùng bông tẩm giấm ăn nút ngay ống nghiệm sau khi đã quan sát hiện tượng.
B. S·ª•c kh√≠ v√Ýo c·ªëc ƒë·ª±ng thu·ªëc t√≠m ho·∫∑c b√¥ng t·∫©m thu·ªëc t√≠m n√∫t ngay ·ªëng nghi·ªám sau khi ƒë√£ quan s√°t hi·ªán t∆∞·ª£ng.
C. Dùng bông tẩm xút hoặc nước vôi trong nút ngay ống nghiệm sau khi đã quan sát hiện tượng.
D. S·ª•c kh√≠ v√Ýo c·ªëc ƒë·ª±ng n∆∞·ªõc.
C√¢u 33. Ti·∫øn h√Ýnh ƒëi·ªán ph√¢n 100g dung d·ªãch ch·ª©a \(AlC{l_3}\) (7x mol) v√Ý \(FeC{l_2}\) (10x mol) (c√≥ m√Ýng ngƒÉn) v·ªõi c∆∞·ªùng ƒë·ªô d√≤ng ƒëi·ªán 5A, kh·ªëi l∆∞·ª£ng dung d·ªãch trong qu√° tr√¨nh ƒëi·ªán ph√¢n thay ƒë·ªïi theo th·ªùi gian ƒë∆∞·ª£c bi·ªÉu di·ªÖn b·∫±ng ƒë·ªì th·ªã sau:
Khi ƒëi·ªán ph√¢n t·ªõi th·ªùi ƒëi·ªÉm \(2,5{t_1}\) gi√¢y khi kh√≠ b·∫Øt ƒë·∫ßu tho√°t ra t·∫°i catot th√¨ t·∫°m d·ª´ng ƒëi·ªán ph√¢n, sau th√™m m·ªôt l∆∞·ª£ng dung d·ªãch \(N{a_2}S{O_4}\) v√Ýo r·ªìi ƒëi·ªán ph√¢n ti·∫øp t·ªõi th·ªùi ƒëi·ªÉm 17370 gi√¢y th√¨ k·∫øt th√∫c qu√° tr√¨nh ƒëi·ªán ph√¢n, l·∫•y m√Ýng ngƒÉn ra; ƒë·ªÉ y√™n dung d·ªãch m·ªôt th·ªùi gian th√¨ kh·ªëi l∆∞·ª£ng dung d·ªãch c√≤n l·∫°i m gam.
.png)
Gi√° tr·ªã c·ªßa m l√Ý
A. 47,63 gam.
B. 28,56 gam.
C. 33,37 gam.
D. 44,75 gam.
C√¢u 34. Cho 31,15 gam h·ªón h·ª£p b·ªôt Zn v√Ý Mg (t·ª∑ l·ªá mol 1 : 1) tan h·∫øt trong dung d·ªãch h·ªón h·ª£p g·ªìm \(NaN{O_3}\) v√Ý \(NaHS{O_4}\) thu ƒë∆∞·ª£c dung d·ªãch A ch·ªâ ch·ª©a m gam h·ªón h·ª£p c√°c mu·ªëi v√Ý 4,48 l√≠t (ƒëktc) h·ªón h·ª£p kh√≠ B g·ªìm \({N_2}O\) v√Ý \({H_2}\). Kh√≠ B c√≥ t·ª∑ kh·ªëi so v·ªõi \({H_2}\) b·∫±ng 11,5. m g·∫ßn gi√° tr·ªã n√Ýo nh·∫•t?
A. 240.
B. 255.
C. 132.
D. 252.
Câu 35. Cho các phát biểu sau:
(a) Khi n·∫•u canh cua th√¨ th·∫•y c√°c m·∫£ng ‚Äúri√™u cua‚Äù n·ªïi l√™n l√Ý do s·ª± ƒë√¥ng t·ª• c·ªßa protein do nhi·ªát ƒë·ªô.
(b) D·∫ßu ƒÉn v√Ý m·ª° b√¥i tr∆°n c√≥ c√πng th√Ýnh ph·∫ßn nguy√™n t·ªë.
(c) Cao su c√≥ t√≠nh ƒë√Ýn h·ªìi, kh√¥ng d·∫´n ƒëi·ªán, kh√¥ng d·∫´n nhi·ªát.
(d) Mu·ªëi mono natri c·ªßa axit glutamic ƒë∆∞·ª£c d√πng l√Ým m√¨ ch√≠nh.
(e) Khi ƒÉn c∆°m, n·∫øu nhai kƒ© s·∫Ω th·∫•y c√≥ v·ªã ng·ªçt l√Ý do tinh b·ªôt trong c∆°m b·ªã th·ªßy ph√¢n th√Ýnh glucoz∆°.
(g) Khi b·ªã ong ƒë·ªët, ƒë·ªÉ gi·∫£m ƒëau nh·ª©c c√≥ th·ªÉ b√¥i v√¥i t√¥i v√Ýo v·∫øt ƒë·ªët.
S·ªë ph√°t bi·ªÉu ƒë√∫ng l√Ý
A. 2.
B. 3.
C. 4.
D. 5.
C√¢u 36. Ti·∫øn h√Ýnh c√°c th√≠ nghi·ªám sau:
(a) Cho dung d·ªãch HCl v√Ýo dung d·ªãch \(Fe{\left( {N{O_3}} \right)_2}\).
(b) Cho kim lo·∫°i Be v√Ýo \({H_2}O\).
(c) Cho kim lo·∫°i Al v√Ýo dung d·ªãch \(HN{O_3}\) lo√£ng ngu·ªôi.
(d) \(N{O_2}\) tác dụng với nước có mặt oxi.
(e) Clo tác dụng sữa vôi \((30^\circ C)\).
(g) L·∫•y thanh Fe ng√¢m trong dung d·ªãch \({H_2}S{O_4}\) ƒë·∫∑c ngu·ªôi, r·ªìi l·∫•y ra cho ti·∫øp v√Ýo dung d·ªãch HCl lo√£ng.
S·ªë th√≠ nghi·ªám c√≥ ph·∫£n ·ª©ng oxi h√≥a - kh·ª≠ x·∫£y ra l√Ý
A. 4.
B. 3.
C. 5.
D. 6.
C√¢u 37. Cho X, Y l√Ý hai axit cacboxylic ƒë∆°n ch·ª©c m·∫°ch h·ªü \(\left( {{M_X} < {M_Y}} \right)\); T l√Ý este hai ch·ª©c t·∫°o b·ªüi X, Y v√Ý m·ªôt ancol no m·∫°ch h·ªü Z. ƒê·ªët ch√°y ho√Ýn to√Ýn 6,88 gam h·ªón h·ª£p E g·ªìm X, Y, T b·∫±ng m·ªôt l∆∞·ª£ng v·ª´a ƒë·ªß \({O_2}\), thu ƒë∆∞·ª£c 5,6 l√≠t \(C{O_2}\) (ƒëktc) v√Ý 3,24 gam n∆∞·ªõc. M·∫∑t kh√°c 6,88 gam E t√°c d·ª•ng v·ªõi dung d·ªãch \(AgN{O_3}{\rm{/ }}N{H_3}\) d∆∞ thu ƒë∆∞·ª£c 12,96 gam Ag. Kh·ªëi l∆∞·ª£ng r·∫Øn khan thu ƒë∆∞·ª£c khi cho c√πng l∆∞·ª£ng E tr√™n t√°c d·ª•ng v·ªõi 150 ml dung d·ªãch KOH 1M l√Ý
A. 10,54 gam.
B. 14,04 gam.
C. 12,78 gam.
D. 13,66 gam.
C√¢u 38. Cho h·ªón h·ª£p X g·ªìm 3 este ƒë∆°n ch·ª©c. ƒêem ƒë·ªët ch√°y m gam X th√¨ c·∫ßn v·ª´a ƒë·ªß 0,465 mol \({O_2}\) s·∫£n ph·∫©m ch√°y thu ƒë∆∞·ª£c ch·ª©a x mol \(C{O_2}\). Th·ªßy ph√¢n m gam X trong 90 ml dung d·ªãch NaOH 1M (v·ª´a ƒë·ªß) th√¨ thu ƒë∆∞·ª£c ƒë∆∞·ª£c 8,86 gam h·ªón h·ª£p mu·ªëi Y v√Ý m·ªôt ancol Z no ƒë∆°n ch·ª©c, m·∫°ch h·ªü. ƒêem ƒë·ªët ch√°y ho√Ýn to√Ýn h·ªón h·ª£p mu·ªëi Y th√¨ c·∫ßn d√πng 7,392 l√≠t (ƒëktc) kh√≠ \({O_2}\). Gi√° tr·ªã x l√Ý
A. 0,38.
B. 0,14.
C. 0,34.
D. 0,46.
Câu 39. Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi ở bảng sau:
|
Mẫu thử |
Thuốc thử |
Hiện tượng |
|
X |
Qùy tím |
Quỳ tím hóa đỏ |
|
Y |
\(Cu{\left( {OH} \right)_2}\) |
Dung dịch xanh lam |
|
X,Z |
Dung dịch \(AgN{O_3}\) trong \(N{H_3}\) dư, đun nóng |
Kết tủa Ag trắng sáng |
|
T |
N∆∞·ªõc \(B{r_2}\) |
Kết tủa trắng |
C√°c dung d·ªãch X, Y, Z, T l·∫ßn l∆∞·ª£t l√Ý:
A. Phenol, etylen glicol, anđehit axetic , axit focmic.
B. Axit axetic, etylen glicol, anđehit axetic, phenol.
C. Axit focmic, glixerol, anđehit axetic, phenol.
D. Axit axetic, etylen glicol, anđehit axetic, phenol.
C√¢u 40. Cho h·ªón h·ª£p X g·ªìm hai ch·∫•t h·ªØu c∆° c√≥ c√πng c√¥ng th·ª©c ph√¢n t·ª≠ \({C_2}{H_7}N{O_2}\) t√°c d·ª•ng v·ª´a ƒë·ªß v·ªõi dung d·ªãch NaOH ƒëun n√≥ng, thu ƒë∆∞·ª£c dung d·ªãch Y v√Ý 4,48 l√≠t h·ªón h·ª£p Z (·ªü ƒëktc) g·ªìm hai kh√≠ (ƒë·ªÅu l√Ým xanh gi·∫•y qu·ª≥ ·∫©m). T·ªâ kh·ªëi h∆°i c·ªßa Z ƒë·ªëi v·ªõi \({H_2}\) b·∫±ng 13,75. C√¥ c·∫°n dung d·ªãch Y thu ƒë∆∞·ª£c kh·ªëi l∆∞·ª£ng mu·ªëi khan l√Ý
A. 16,5 gam.
B. 14,3 gam.
C. 8,9 gam.
D. 15,7 gam.
ĐÁP ÁN ĐỀ SỐ 1
|
1-B |
2-A |
3-D |
4-B |
5-C |
6-B |
7-B |
8-B |
9-A |
10-B |
|
11-C |
12-B |
13-C |
14-D |
15-A |
16-A |
17-B |
18-A |
19-D |
20-C |
|
21-D |
22-C |
23-B |
24-C |
25-D |
26-C |
27-B |
28-D |
29-A |
30-C |
|
31-C |
32-C |
33-A |
34-A |
35-C |
36-A |
37-C |
38-A |
39-C |
40-B |
ĐỀ SỐ 2
C√¢u 1: C·∫•u h√¨nh electron c·ªßa nguy√™n t·ª≠ S (Z=16) l√Ý
A. \(1{s^2}2{s^2}2{p^6}3{s^2}3{p^6}. \)
B. \(1{s^2}2{s^2}2{p^6}3{p^6}.\)
C. \(1{s^2}2{s^2}2{p^5}3{s^2}3{p^5}.\)
D. \(1{s^2}2{s^2}2{p^6}3{s^2}3{p^4}.\)
C√¢u 2: Lo·∫°i ph·∫£n ·ª©ng n√Ýo lu√¥n lu√¥n l√Ý ph·∫£n ·ª©ng oxi h√≥a ‚Äì kh·ª≠?
A. Phản ứng hóa hợp.
B. Phản ứng phân hủy.
C. Phản ứng thế trong hóa học vô cơ.
D. Phản ứng trao đổi.
C√¢u 3: Oxi c√≥ th·ªÉ thu ƒë∆∞·ª£c t·ª´ ph·∫£n ·ª©ng nhi·ªát ph√¢n ch·∫•t n√Ýo sau ƒë√¢y?
A. \(CaC{O_3}\).
B. \(KMn{O_4}.\)
C. \({(N{H_4})_2}S{O_4}.\)
D. \(NaHC{O_3}.\)
C√¢u 4: .Cho phenolphtalein v√Ýo dung d·ªãch n√Ýo sau ƒë√¢y s·∫Ω h√≥a h·ªìng ?
A. dung dịch \(NaN{O_3}.\)
B. dung dịch \(HN{O_3}.\)
C. dung dịch \(KOH.\)
D. dung dịch \({H_2}S{O_4}.\)
C√¢u 5: C√¥ng th·ª©c ph√¢n t·ª≠ kh√≠ metan l√Ý
A. \(C{H_4}.\)
B. \({C_2}{H_4}. \)
C. \({C_2}{H_2}.\)
D. \({C_2}{H_6}.\)
C√¢u 6: H·ª£p ch·∫•t n√Ýo sau ƒë√¢y l√Ý ancol?
A. \(HCH=O\).
B. \({C_2}{H_5}OH.\)
C. \({C_6}{H_5}OH.\)
D. \(C{H_3}COOH.\)
C√¢u 7: Cho s∆° ƒë·ªì th·ª≠ t√≠nh d·∫´n ƒëi·ªán c·ªßa c√°c ch·∫•t nh∆∞ h√¨nh v·∫Ω. B√≥ng ƒë√®n kh√¥ng s√°ng khi X l√Ý
.png)
A. dung dịch saccarozo (đường).
B. dung dịch \(NaOH.\)
C. dung dịch \(Ca{{Cl}_2}\).
D. dung dịch \(HCl\).
C√¢u 8: Este \({C_2}{H_5}COOC{H_3}\) c√≥ t√™n l√Ý
A. metyl propionat.
B. etylmetyl este.
C. metyletyl este.
D. etyl propionat.
C√¢u 9: C·∫•u h√¨nh electron l·ªõp ngo√Ýi c√πng c·ªßa nguy√™n t·ª≠ kim lo·∫°i ki·ªÅm l√Ý
A. \(n{s^2} \)
B. \(n{s^1}\)
C. \(n{s^2} n{p^1}\)
D. \(n{s^2} n{p^3}\)
C√¢u 10: Ch·∫•t n√Ýo sau ƒë√¢y thu·ªôc lo·∫°i ƒëisaccarit ?
A. Tinh b·ªôt.
B. Xenluloz∆°.
C. Glucoz∆°.
D. Saccaroz∆°.
---(Nội dung đầy đủ, chi tiết từ câu 11 đến câu 40 của đề thi số 2 vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 2
1-D 2-C 3-B 4-C 5-A 6-B 7-A 8-D 9-B 10-D
11-C 12-D 13-B 14-C 15-A 16-D 17-A 18-A 19-C 20-B
21-D 22-A 23-A 24-D 25-B 26-D 27-C 28-C 29-C 30-B
31-C 32-B 33-D 34-B 35-D 36-A 37-A 38-A 39-B 40-B.
ĐỀ SỐ 3
C√¢u 1. Ion kim lo·∫°i n√Ýo sau ƒë√¢y c√≥ t√≠nh oxi h√≥a y·∫øu nh·∫•t?
A. Fe3+. B. Mg2+. C. Ag+. D. Cu2+.
C√¢u 2. Trong s·ªë c√°c ph∆∞∆°ng ph√°p l√Ým m·ªÅm n∆∞·ªõc c·ª©ng, ph∆∞∆°ng ph√°p n√Ýo ch·ªâ kh·ª≠ ƒë∆∞·ª£c ƒë·ªô c·ª©ng t·∫°m th·ªùi?
A. Phương pháp cất nước. B. Phương pháp trao đổi ion.
C. Phương pháp hóa học. D. Phương pháp đun sôi nước.
C√¢u 3. M·ªôt ch·∫•t c√≥ ch·ª©a nguy√™n t·ªë oxi, d√πng ƒë·ªÉ l√Ým s·∫°ch n∆∞·ªõc v√Ý c√≥ t√°c d·ª•ng b·∫£o v·ªá c√°c sinh v·∫≠t tr√™n Tr√°i ƒê·∫•t kh√¥ng b·ªã b·ª©c x·∫° c·ª±c t√≠m. Ch·∫•t kh√≠ n√Ýy l√Ý
A. Ozon.
B. Oxi.
C. Lưu huỳnh đioxit.
D. Cacbon đioxit.
C√¢u 4. Este n√Ýo sau ƒë√¢y t√°c d·ª•ng v·ªõi dung d·ªãch ki·ªÅm cho 2 mu·ªëi v√Ý n∆∞·ªõc?
A. HCOOC6H5.
B. C6H5COOCH3.
C. CH3COOCH2C6H5.
D. CH3COOCH3.
C√¢u 5. Ch·∫•t n√Ýo sau t√°c d·ª•ng ƒë∆∞·ª£c v·ªõi dung d·ªãch HCl nh∆∞ng kh√¥ng t√°c d·ª•ng v·ªõi dung d·ªãch NaOH?
A. Al.
B. NaHCO3.
C. Al2O3.
D. NaAlO2.
Câu 6. Phần trăm khối lượng của nguyên tố cacbon trong trong phân tử anilin (C6H5NH2)?
A. 83,72%
B. 75,00%
C. 78,26%
D. 77,42%
C√¢u 7. Ch·∫•t n√Ýo sau ƒë√¢y kh√¥ng b·ªã oxi ho√° b·ªüi H2SO4 ƒë·∫∑c, n√≥ng l√Ý (
A. Al. B. Fe3O4. C. FeCl2. D. CuO.
C√¢u 8. Cho v√Ýi gi·ªçt dung d·ªãch NaOH v√Ýo dung d·ªãch FeCl3 hi·ªán t∆∞·ª£ng x·∫£y ra l√Ý
A. kh√¥ng hi·ªán t∆∞·ª£ng g√¨. B. c√≥ k·∫øt t·ªßa m√Ýu n√¢u ƒë·ªè xu·∫•t hi·ªán.
C. c√≥ k·∫øt t·ªßa ƒëen xu·∫•t hi·ªán. D. c√≥ k·∫øt t·ªßa v√Ýng xu·∫•t hi·ªán.
C√¢u 9. Polime n√Ýo sau ƒë√¢y kh√¥ng ch·ª©a nguy√™n t·ªë nit∆° trong ph√¢n t·ª≠?
A. T∆° t·∫±m.
B. Poliacrilonitrin.
C. Polietilen.
D. T∆° nilon-6.
C√¢u 10. Ch·∫•t X l√Ý m·ªôt baz∆° m·∫°nh, ƒë∆∞·ª£c s·ª≠ d·ª•ng r·ªông r√£i trong nhi·ªÅu ng√Ýnh c√¥ng nghi·ªáp nh∆∞ s·∫£n xu·∫•t n∆∞·ªõc gia-ven, n·∫•u x√Ý ph√≤ng,‚Ķ C√¥ng th·ª©c c·ªßa X l√Ý
A. Ca(OH)2. B. Ba(OH)2. C. NaOH. D. KOH.
---(Nội dung đầy đủ, chi tiết từ câu 11 đến câu 40 của đề thi số 3 vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 3
|
1B |
2D |
3A |
4A |
5D |
6D |
7D |
8B |
9C |
10C |
|
11C |
12D |
13C |
14A |
15B |
16A |
17A |
18A |
19C |
20A |
|
21D |
22A |
23B |
24B |
25C |
26C |
27D |
28D |
29C |
30A |
|
31D |
32A |
33C |
34D |
35C |
36B |
37B |
38B |
39C |
40B |
ĐỀ SỐ 4
C√¢u 1. ·ªû ƒëi·ªÅu ki·ªán th∆∞·ªùng, kim lo·∫°i n√Ýo sau ƒë√¢y c√≥ nhi·ªát ƒë·ªô n√≥ng ch·∫£y th·∫•p nh·∫•t?
A. Zn. B. Hg. C. Ag. D. Cu.
C√¢u 2. Kim lo·∫°i n√Ýo sau ƒë√¢y l√Ý kim lo·∫°i ki·ªÅm th·ªï?
A. Na. B. Ca. C. Al. D. Fe.
C√¢u 3. Ch·∫•t b·ªôt X m√Ýu ƒëen, c√≥ kh·∫£ nƒÉng h·∫•p ph·ª• c√°c kh√≠ ƒë·ªôc n√™n ƒë∆∞·ª£c d√πng trong trong c√°c m√°y l·ªçc n∆∞·ªõc, kh·∫©u trang y t·∫ø, m·∫∑t n·∫° ph√≤ng ƒë·ªôc. Ch·∫•t X l√Ý
A. cacbon oxit. B. lưu huỳnh. C. than hoạt tính. D. thạch cao.
C√¢u 4. Metyl propionat c√≥ c√¥ng th·ª©c c·∫•u t·∫°o l√Ý
A. HCOOC2H5. B. C2H5COOC2H5. C. C2H5COOCH3. D. CH3COOCH3.
C√¢u 5. Cho dung d·ªãch NaOH v√Ýo dung d·ªãch ch·∫•t X, thu ƒë∆∞·ª£c k·∫øt t·ªßa m√Ýu xanh lam. Ch·∫•t X l√Ý
A. FeCl3. B. MgCl2. C. CuCl2. D. FeCl2.
C√¢u 6. Dung d·ªãch Ala-Gly kh√¥ng ph·∫£n ·ª©ng ƒë∆∞·ª£c v·ªõi dung d·ªãch n√Ýo sau ƒë√¢y?
A. HCl. B. H2SO4. C. NaCl. D. KOH.
C√¢u 7. Al2O3 kh√¥ng tan ƒë∆∞·ª£c trong dung d·ªãch n√Ýo sau ƒë√¢y?
A. NaOH. B. BaCl2. C. HCl. D. Ba(OH)2.
C√¢u 8. Crom (VI) oxit c√≥ c√¥ng th·ª©c ho√° h·ªçc l√Ý
A. Cr(OH)3. B. CrO3. C. K2CrO4. D. Cr2O3.
C√¢u 9. Monome n√Ýo sau ƒë√¢y kh√¥ng c√≥ ph·∫£n ·ª©ng tr√πng h·ª£p?
A. CH2=CH2. B. CH2=CH-CH3. C. CH2=CHCl. D. CH3-CH3.
C√¢u 10. Kim lo·∫°i n√Ýo sau ƒë√¢y ƒë∆∞·ª£c ƒëi·ªÅu ch·∫ø b·∫±ng ph∆∞∆°ng ph√°p nhi·ªát luy·ªán?
A. Na. B. Al. C. Ca. D. Fe.
---(Nội dung đầy đủ, chi tiết từ câu 11 đến câu 40 của đề thi số 4 vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 4
|
1B |
2B |
3C |
4C |
5C |
6C |
7B |
8B |
9D |
10D |
|
11A |
12C |
13D |
14B |
15B |
16A |
17A |
18A |
19B |
20D |
|
21A |
22D |
23D |
24A |
25B |
26D |
27C |
28B |
29A |
30D |
|
31B |
32D |
33A |
34C |
35B |
36C |
37D |
38C |
39D |
40A |
ĐỀ SỐ 5
C√¢u 41. Ch·∫•t n√Ýo d∆∞·ªõi ƒë√¢y ch·ªâ ph√π h·ª£p ƒë·ªÉ l√Ým m·ªÅm n∆∞·ªõc c√≥ ƒë·ªô c·ª©ng t·∫°m th·ªùi?
A. Ca(OH)2.
B. Na2CO3.
C. HCl.
D. Na3PO4.
C√¢u 42. Ph√°t bi·ªÉu n√Ýo sau ƒë√¢y ƒë√∫ng?
A. Dung d·ªãch HNO3 ƒë·∫∑c, ngu·ªôi ho√Ý tan ƒë∆∞·ª£c nh√¥m.
B. Dung d·ªãch NH3 l√Ým qu·ª≥ t√≠m chuy·ªÉn sang m√Ýu h·ªìng.
C. Nhiệt phân NaNO3 thu được khí NO2.
D. Cu tan ƒë∆∞·ª£c trong dung d·ªãch ch·ª©a h·ªón h·ª£p HCl v√Ý NaNO3.
C√¢u 43. S·ªë ƒë·ªìng ph√¢n este c√≥ c√¥ng th·ª©c ph√¢n t·ª≠ C4H8O2 l√Ý
A. 4.
B. 3.
C. 5.
D. 2.
C√¢u 44. Anilin ph·∫£n ·ª©ng v·ªõi dung d·ªãch ch·∫•t n√Ýo sau ƒë√¢y?
A. NaOH.
B. HCl.
C. Na2CO3.
D. NaCl.
C√¢u 45. Trong c√°c mu·ªëi: CaCO3, NaCl, KBr v√Ý NaHCO3 mu·ªëi d·ªÖ b·ªã nhi·ªát ph√¢n nh·∫•t l√Ý
A. NaCl.
B. KBr.
C. CaCO3.
D. NaHCO3.
C√¢u 46. D√£y g·ªìm c√°c kim lo·∫°i n√Ýo sau ƒë√¢y th∆∞·ªùng ƒë∆∞·ª£c s·∫£n xu·∫•t b·∫±ng ph∆∞∆°ng ph√°p th·ªßy luy·ªán ?
A. Al, Fe, Pb, Hg.
B. Mg, Fe, Ag, Cu.
C. Na, Cu, Pb, Zn.
D. Cu, Ag, Hg, Au.
C√¢u 47. Este n√Ýo sau ƒë√¢y ph·∫£n ·ª©ng v·ªõi dung d·ªãch NaOH theo t·ªâ l·ªá mol 1 : 2?
A. Benzyl fomat.
B. Phenyl axetat.
C. Metyl fomat.
D. Etyl fomat.
C√¢u 48. Ph√°t bi·ªÉu n√Ýo sau ƒë√¢y kh√¥ng ƒë√∫ng?
A. Phenol tham gia phản ứng thế brom dễ hơn so với benzen,
B. Phenol phản ứng với dung dịch NaOH, lấy muối vừa tạo ra cho tác dụng với dung dịch HCl lại thu được phenol.
C. Dung d·ªãch phenol trong n∆∞·ªõc l√Ým qu·ª≥ t√≠m ho√° ƒë·ªè.
D. Dung dịch natriphenolat phản ứng với khí CO2, lấy kết tủa vừa tạo ra cho tác dụng với dung dịch NaOH lại thu được natriphenolat.
C√¢u 49. Ph·∫£n ·ª©ng n√Ýo sau ƒë√¢y t·∫°o ra h·ª£p ch·∫•t crom (III)?
A. Cr(OH)2 + Br2 + NaOH ‚Üí
B. K2Cr2O7 + FeSO4 + H2SO4 ‚Üí
C. CrO3 + H2O ‚Üí
D. Cr + HCl ‚Üí
C√¢u 50. Cacbohiƒërat l√Ý h·ª£p ch·∫•t t·∫°p ch·ª©c, trong ph√¢n t·ª≠ c√≥ nhi·ªÅu nh√≥m hiƒëroxi v√Ý c√≥ nh√≥m
A. amin.
B. cacbonyl.
C. andehit.
D. cacboxyl.
---(Nội dung đầy đủ, chi tiết từ câu 51 đến câu 80 của đề thi số 5 vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 5
|
41 |
A |
42 |
D |
43 |
A |
44 |
B |
45 |
D |
|
46 |
D |
47 |
B |
48 |
C |
49 |
B |
50 |
B |
|
51 |
A |
52 |
C |
53 |
C |
54 |
A |
55 |
A |
|
56 |
B |
57 |
A |
58 |
A |
59 |
A |
60 |
D |
|
61 |
A |
62 |
B |
63 |
B |
64 |
A |
65 |
D |
|
66 |
C |
67 |
D |
68 |
B |
69 |
D |
70 |
B |
|
71 |
B |
72 |
D |
73 |
B |
74 |
D |
75 |
B |
|
76 |
A |
77 |
A |
78 |
B |
79 |
D |
80 |
C |
Tr√™n ƒë√¢y l√Ý m·ªôt ph·∫ßn tr√≠ch d·∫´n n·ªôi dung B·ªô 5 ƒë·ªÅ thi th·ª≠ THPT QG m√¥n H√≥a h·ªçc nƒÉm 2021 c√≥ ƒë√°p √°n Tr∆∞·ªùng THPT An L∆∞∆°ng. ƒê·ªÉ xem to√Ýn b·ªô n·ªôi dung c√°c em ƒëƒÉng nh·∫≠p v√Ýo trang hoc247.net ƒë·ªÉ t·∫£i t√Ýi li·ªáu v·ªÅ m√°y t√≠nh.
Hy v·ªçng t√Ýi li·ªáu n√Ýy s·∫Ω gi√∫p c√°c em h·ªçc sinh √¥n t·∫≠p t·ªët v√Ý ƒë·∫°t th√Ýnh t√≠ch cao trong h·ªçc t·∫≠p.
Ngo√Ýi ra c√°c em c√≥ th·ªÉ tham kh·∫£o th√™m m·ªôt s·ªë t∆∞ li·ªáu c√πng chuy√™n m·ª•c t·∫°i ƒë√¢y:
- Bộ 5 đề thi thử THPT QG môn Hóa học năm 2021 có đáp án Trường THPT Kim Động
- Bộ 5 đề thi thử THPT QG môn Hóa học năm 2021 có đáp án Trường THPT Đức Hợp
Chúc các em học tốt!
T√Ýi li·ªáu li√™n quan
Tư liệu nổi bật tuần
- Xem thêm


