Hướng dẫn Giải bài tập Hóa học 10 KNTT Bài 9 Bài 9: Ôn tập chương 2 môn Hóa học lớp 10 KNTT giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức.
-
Giải câu hỏi 1 trang 46 SGK Hóa học 10 Kết nối tri thức - KNTT
Cho vị trí của các nguyên tố E, T, Q, X, Y, Z trong bảng tuần hoàn rút gọn (chỉ biểu diễn các nguyên tố nhóm A) như sau:
.jpg)
Có các nhận xét sau:
(1) Thứ tự giảm dần tính kim loại Y, E, X.
(2) Thứ tự tăng dần độ âm điện là Y, X, Z, T.
(3) Thứ tự giảm dần tính phi kim là T, Z, Q.
(4) Thứ tự giảm dần bán kính nguyên tử là Y, E, X, T.
Số nhận xét đúng là
A. 1.
B. 2.
C. 3.
D. 4.
-
Giải câu hỏi 2 trang 47 SGK Hóa học 10 Kết nối tri thức - KNTT
Sulfur (S) là nguyên tố thuộc nhóm VIA, chu kì 3 của bảng tuần hoàn. Trong các biểu thức sau:
(1) Nguyên tử S có 3 lớp electron và có 10 electron p.
(2) Nguyên tử S có 5 electron hóa trị và 6 electron s.
(3) Công thức oxide cao nhất của S có dạng SO3 và là acidic oxide.
(4) Nguyên tố S có tính phi kim mạnh hơn so với nguyên tố có số hiệu nguyên tử là 8.
(5) Hydroxide cao nhất của S có dạng H2SO4 và có tính acid.
Số phát biểu đúng là
A. 2.
B. 3.
C. 4.
D. 5.
-
Giải câu hỏi 3 trang 47 SGK Hóa học 10 Kết nối tri thức - KNTT
X và Y là hai nguyên tố thuộc nhóm A, trong cùng một chu kì của bảng tuần hoàn. Oxide cao nhất của X và Y có dạng XO và YO3. Trong các phát biểu sau:
(1) X và Y thuộc 2 nhóm A kế tiếp nhau.
(2) X là kim loại, Y là phi kim
(3) X2O3 là basic oxide và YO3 là acidic oxid.
(4) Hydroxide cao nhất của Y có dạng Y(OH)6 và có tính baso.
Số phát biểu đúng là:
A. 2.
B. 3.
C. 4.
D. 1.
-
Giải câu hỏi 4 trang 47 SGK Hóa học 10 Kết nối tri thức - KNTT
Borax (Na2B4O7.10H2O), còn gọi là hàn the, là khoáng chất dạng tinh thể. Nhờ có khả năng hòa tan oxide của kim loại, borax được dùng để làm sạch bề mặt kim loại trước khi hàn, chế tạo thủy tinh quang học, men đồ sứ,… Một lượng lớn borax được dùng để sản xuất bột giặt.
a) Nêu vị trí trong bảng tuần hoàn của mỗi nguyên tố có trong thành phần của borax và viết cấu hình electron của nguyên tử các nguyên tố đó.
b) Sắp xếp các nguyên tố trên theo chiều bán kính nguyên tử tăng dần.
c) Sắp xếp các nguyên tố trên theo chiều độ âm điện giảm dần.
Giải thích dựa vào quy luật biến thiên trong bảng tuần hoàn.
- VIDEOYOMEDIA
-
Giải câu hỏi 5 trang 47 SGK Hóa học 10 Kết nối tri thức - KNTT
Công thức cấu tạo của phân tử cafein, một chất gây đắng tìm thấy nhiều trong cafe và trà được biểu diễn ở hình bên
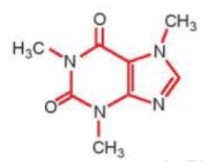
a) Nêu vị trí của các nguyên tố tạo nên cafein trong bảng tuần hoàn.
b) So sánh tính phi kim, bán kính nguyên tử và độ âm điện của các nguyên tố đó và giải thích.
-
Giải câu hỏi 6 trang 47 SGK Hóa học 10 Kết nối tri thức - KNTT
Một loại hợp kim nhẹ, bền được sử dụng rộng rãi trong kĩ thuật hàng không chứa hai nguyên tố A, B đứng kế tiếp nhau trong cùng một chu kì của bảng tuần hoàn và có tổng số đơn vị điện tích hạt nhân là 25.
a) Viết cấu hình electron, từ đó xác định vị trí của hai nguyên tố A và B trong bảng tuần hoàn.
b) So sánh tính chất hóa học của A với B và giải thích.
-
Giải bài 9.1 trang 24 SBT Hóa học 10 Kết nối tri thức - KNTT
Nguyên tử X có Z = 15. Trong bảng tuần hoàn, nguyên tố X thuộc chu kì
A. 4.
B. 2.
C. 5.
D. 3.
-
Giải bài 9.2 trang 24 SBT Hóa học 10 Kết nối tri thức - KNTT
Nguyên tố X thuộc nhóm IA, còn nguyên tố Z thuộc nhóm VIIA của bảng tuần hoàn. Cấu hình electron hoá trị của nguyên tử các nguyên tố X, Z lần lượt là
A. ns1 và ns2np5.
B. ns1 và ns2np7.
C. ns1 và ns2np3.
D. ns2 và ns2np5.
-
Giải bài 9.3 trang 24 SBT Hóa học 10 Kết nối tri thức - KNTT
Cho các nguyên tố sau: 11Na, 13Al và 17Cl. Các giá trị bán kính nguyên tử (pm) tương ứng trong trường hợp nào sau đây là đúng?
A. Na (157); Al (125); Cl (99).
B. Na (99); Al (125); Cl (157).
C. Na (157); Al (99); Cl (125).
D. Na (125); Al (157); Cl (99).
-
Giải bài 9.4 trang 24 SBT Hóa học 10 Kết nối tri thức - KNTT
Cho các nguyên tố sau: 14Si, 15P và 16S.
Các giá trị độ âm điện tương ứng trong trường hợp nào sau đây là đúng?
A. 14Si (2,19); 15p (1,90); 16S (2,58).
B. 14Si (2,58); 15P (2,19); 16S (1,90)
C. 14Si (1,90); 15P (2,19); 16S (2,58)
D. 14Si (1,90); 15P (2,58); 16S (2,19)
-
Giải bài 9.5 trang 24 SBT Hóa học 10 Kết nối tri thức - KNTT
Dãy nào sau đây được xếp theo thứ tự tăng dần tính acid?
A. NaOH; Al(OH)3; Mg(OH)2; H2SiO3.
B. H2SiO3, Al(OH)3; H3PO4; H2SO4.
C. Al(OH)3, H2SiO3; H3PO4, H2SO4.
D. H2SiO3, Al(OH)3, Mg(OH)2, H2SO4.
-
Giải bài 9.6 trang 24 SBT Hóa học 10 Kết nối tri thức - KNTT
Dãy nào sau đây được xếp theo thứ tự tăng dần tính base?
A. K2O, Al2O3, MgO, CaO.
B. Al2O3, MgO, CaO, K2O.
C MgO, CaO, Al2O3, K2O.
D. CaO, Al2O3, K2O, MgO.
-
Giải bài 9.7 trang 25 SBT Hóa học 10 Kết nối tri thức - KNTT
Nêu mối quan hệ giữa xu hướng biến đổi bán kính nguyên tử với độ âm điện của các nguyên tố trong bảng tuần hoàn và giải thích.
-
Giải bài 9.8 trang 25 SBT Hóa học 10 Kết nối tri thức - KNTT
Dựa vào xu hướng biển đổi tính kim loại và phi kim của các nguyên tố trong bảng tuần hoàn, cho biết:
a) Nguyên tố nào có tính kim loại mạnh nhất. Nguyên tố nào có tính phi kim mạnh nhất.
b) Các nguyên tố kim loại và phi kim được phân bố ở khu vực nào trong bảng tuần hoàn.
c) Những nhóm nào gồm các kim loại mạnh nhất và phi kim mạnh nhất.
-
Giải bài 9.9 trang 25 SBT Hóa học 10 Kết nối tri thức - KNTT
Methadone (C21H27NO), thưởng được sử dụng để giảm đau và được xem như là chất thay thế cho heroin (thuốc chữa cai nghiện).
a) Nêu vị trí các nguyên tố tạo nên methadone trong bảng tuần hoàn.
b) So sánh bán kính nguyên tử, độ âm điện và tính phi kim của các nguyên tố đó. Giải thích.
-
Giải bài 9.10 trang 25 SBT Hóa học 10 Kết nối tri thức - KNTT
Nguyên tử X có kí hiệu \[{}_{16}^{32}X\].
a) Xác định các giá trị số proton, số electron, số neutron, số đơn vị điện tích hạt nhân và số khối của X.
b) Viết cấu hình electron nguyên tử X và nêu vị trí của X trong bảng tuần hoàn.
c) X là kim loại, phi kim hay khí hiếm? Giải thích.
d) Xác định công thức oxide ứng với hoá trị cao nhất, hydroxide tương ứng của X và nêu tính acid - base của chúng.
-
Giải bài 9.11 trang 25 SBT Hóa học 10 Kết nối tri thức - KNTT
Cho hai nguyên tố có số hiệu nguyên tử Z = 15 và Z = 62.
a) Xác định vị trí của hai nguyên tố đó trong bảng tuần hoàn.
b) Viết cấu hình electron nguyên tử của hai nguyên tố đó và cho biết chúng là nguyên tố s, p, d hay f.
c) Viết công thức oxide ứng với hóa trị cao nhất và hydroxide tương ứng của mỗi nguyên tố.
d) Nêu tính chất đơn chất và tính chất mỗi hợp chất trên
-
Giải bài 9.12 trang 26 SBT Hóa học 10 Kết nối tri thức - KNTT
Hãy so sánh và giải thích kích thước tương đối của:
a) nguyên tử lithium và nguyên tử fluorine.
b) nguyên tử lithium và ion của nó (Li+).
c) nguyên tử oxygen và ion của nó (O2-).
d) ion nitride (N3-) và ion fluoride (F-).
-
Giải bài 9.13 trang 26 SBT Hóa học 10 Kết nối tri thức - KNTT
Ba nguyên tố X, Y, Z thuộc cùng một chu kì và có tổng số hiệu nguyên tử là 39. Số hiệu của nguyên tử Y bằng trung bình cộng số hiệu của nguyên tử X và Z. Nguyên tử của ba nguyên tố này hầu như không phản ứng với H2O ở điều kiện thường.
a) Hãy xác định vị trí của X, Y, Z trong bảng tuần hoàn. Viết cấu hình electron nguyên tử và tên từng nguyên tố.
b) So sánh độ âm điện, bán kính nguyên tử của X, Y, Z.
c) So sánh tính base của các hydroxide của X, Y, Z.
-
Giải bài 9.14 trang 26 SBT Hóa học 10 Kết nối tri thức - KNTT
Quá trình sản xuất aluminium từ quặng bauxite gồm tinh chế bauxite và trộn Al2O3 thu được với cryolite (Na3AlF6) rồi điện phân nóng chảy. Trường hợp bể điện phân chưa đúng tiêu chuẩn, sản phẩm là Al có lẫn Na. Cho 1,0 g hỗn hợp sản phẩm phản ứng với dung dịch sulfuric acid loãng, dư, thoát ra 1336,7 mL khí hydrogen (25 °C và 1 bar).
a) Xác định độ tinh khiết của aluminium trong sản phẩm.
b) Viết công thức oxide ứng với hoá trị cao nhất, hydroxide tương ứng của các kim loại trên.
c) So sánh tính acid - base giữa các oxide, hydroxide tương ứng đó. Giải thích.
-
Giải bài 9.15 trang 26 SBT Hóa học 10 Kết nối tri thức - KNTT
Oxide ứng với hoá trị cao nhất của một nguyên tố có công thức thực nghiệm là R2O5. Oxide này là một chất hút nước mạnh, được sử dụng trong tổng hợp chất hữu cơ. Khả năng hút ẩm của nó đủ mạnh để chuyển nhiều acid vô cơ thành các alhydrite (oxide tương ứng) của chúng. Hợp chất khí của R với hydrogen có chứa 8,82% khối lượng hydrogen và là chất khí không màu, rất độc, kém bền sinh ra trong quá trình phân huỷ xác động thực vật.
a) Nêu vị trí của R trong bảng tuần hoàn.
b) Viết cấu hình electron theo ô orbital của nguyên tử R.
c) Nêu một số tính chất hoá học cơ bản của R và hợp chất.
-
Giải bài 9.16 trang 27 SBT Hóa học 10 Kết nối tri thức - KNTT
Hoà tan hết 2,3 g hỗn hợp có chứa kim loại barium và hai kim loại kiềm kế tiếp nhau trong nhóm IA của bảng tuần hoàn vào nước, thu được dung dịch X và 611 mL khi (25 °C và 1 bar). Nếu thêm 1,278 g Na2SO4 vào dung dịch X và khuấy đều thì sau khi phản ứng kết thúc, nước lọc vẫn còn ion Ba2+. Nếu thêm 1,491 g Na2SO4 vào dung dịch X và khuấy đều thì sau khi phản ứng kết thúc, nước lọc có mặt ion SO42-. Dựa vào bảng tuần hoàn, hãy xác định tên hai kim loại kiềm ở trên





