Mß╗Öt sß╗æ oxide phß╗ò biß║┐n tß║ío n├¬n c├íc kho├íng chß║Ñt nhã░ ─æ├í granite v├á thß║ích anh (oxide cß╗ºa silicon), gß╗ë sß║»t (oxide cß╗ºa sß║»t) v├á ─æ├í v├┤i (oxide cß╗ºa calcium v├á carbon). ─É├í ruby tß╗▒ nhi├¬n c├│ dß║úi m├áu tß╗½ hß╗ông ─æß║¡m tß╗øi ─æß╗Å sß║½m do th├ánh phß║ºn c├íc oxide cß╗ºa aluminium, chromium, ... tß║ío n├¬n. Oxide l├á g├¼? C├│ nhß╗»ng loß║íi oxide n├áo? Ch├║ng c├│ sß║Án trong tß╗▒ nhi├¬n hay phß║úi ─æiß╗üu chß║┐? Ch├║ng ta h├úy c├╣ng t├¼m hiß╗âu qua b├ái hß╗ìc dã░ß╗øi ─æ├óy B├ái 12: Oxide trong chã░ãíng tr├¼nh Khoa hß╗ìc tß╗▒ nhi├¬n 8 Ch├ón trß╗Øi s├íng tß║ío.
Tóm tắt lÛ thuyết
1.1. Kh├íi niß╗çm Oxide - Phã░ãíng tr├¼nh h├│a hß╗ìc tß║ío oxide
a. Tìm hiểu khái niệm Oxide
H├¼nh 12.1. Mß╗Öt sß╗æ hß╗úp chß║Ñt c├│ chã░a nguy├¬n tß╗æ oxygen
- Oxide là hợp chất gồm 2 nguyên tố, trong đó có nguyên tố oxygen.
- C├┤ng thß╗®c ho├í hß╗ìc chung cß╗ºa oxide l├á MXOY
b. T├¼m hiß╗âu phß║ún ß╗®ng tß║ío Oxide
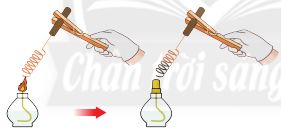
Hình 12.2. Đốt dây đồng
Hình 12.3. Đốt than gỗ trong không khí
C├íc phß║ún ß╗®ng ho├í hß╗ìc tß║ío oxide:
- Kim loß║íi phß║ún ß╗®ng vß╗øi oxygen
Kim loại + O2 \(\xrightarrow{t^0}\) Oxide kim loại
Phß║ún ß╗®ng tr├¬n xß║úy ra vß╗øi hß║ºu hß║┐t c├íc kim loß║íi (trß╗½ Au, Pt, Ag).
- Phi kim phß║ún ß╗®ng vß╗øi oxygen
Phi kim + O2 \(\xrightarrow{t^0}\) Oxide phi kim
C├íc phi kim thã░ß╗Øng gß║Àp: C, S, B ...
1.2. Phân loại Oxide
H├¼nh 12.4. D├╣ng giß║Ñm ─ân ─æß╗â tß║®y gß╗ë s├®t tr├¬n bß╗ü mß║Àt ─æß╗ô d├╣ng l├ám bß║▒ng sß║»t - th├®p
- Có 4 loại oxide:
+ Oxide acid l├á oxide phß║ún ß╗®ng ─æã░ß╗úc vß╗øi dung dß╗ïch base tß║ío ra muß╗æi v├á nã░ß╗øc.
+ Oxide base l├á oxide phß║ún ß╗®ng ─æã░ß╗úc vß╗øi dung dß╗ïch acid tß║ío ra muß╗æi v├á nã░ß╗øc.
+ Oxide lã░ß╗íng t├¡nh (amphoteric oxide) l├á c├íc oxide vß╗½a phß║ún ß╗®ng ─æã░ß╗úc vß╗øi dung dß╗ïch acid vß╗½a phß║ún ß╗®ng ─æã░ß╗úc vß╗øi dung dß╗ïch base ─æß╗üu tß║ío ra muß╗æi v├á nã░ß╗øc.
+ Oxide trung t├¡nh (neutral oxide) l├á c├íc oxide kh├┤ng phß║ún ß╗®ng ─æã░ß╗úc vß╗øi dung dß╗ïch acid v├á dung dß╗ïch base.
1.3. Tính chất hóa học của Oxide
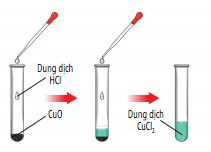
H├¼nh 12.5. CuO phß║ún ß╗®ng vß╗øi dung dß╗ïch HCl
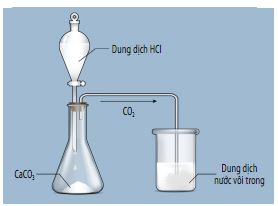
Hình 12.6. Thí nghiệm điều chế CO2 và thử tính chất của CO2
- Oxide base phß║ún ß╗®ng vß╗øi dung dß╗ïch acid tß║ío ra muß╗æi cß╗ºa acid tã░ãíng ß╗®ng v├á nã░ß╗øc.
- Oxide acid phß║ún ß╗®ng vß╗øi dung dß╗ïch base tß║ío ra muß╗æi cß╗ºa acid tã░ãíng ß╗®ng v├á nã░ß╗øc.
Bài tập minh họa
V├¡ dß╗Ñ 1: Lß║¡p CTHH cß╗ºa hß╗úp chß║Ñt: Nh├┤m oxit ─æã░ß╗úc tß║ío n├¬n tß╗¡ 2 nguy├¬n tß╗æ nh├┤m v├á oxi.
Hã░ß╗øng dß║½n giß║úi
Theo quy tắc hóa trị:
x . III = y . II
=> x = 2; y = 3
Vậy CTHH: Al2­O3
Ví dụ 2: CaO là oxide:
A. Oxide acid
B. Oxit base
C. Oxit trung tính
D. Oxit lã░ß╗íng t├¡nh
Hã░ß╗øng dß║½n giß║úi
CaO là Oxit base
Đáp án B
Luyß╗çn tß║¡p B├ái 12 Khoa hß╗ìc tß╗▒ nhi├¬n 8 Ch├ón trß╗Øi s├íng tß║ío
Học xong bài này các em cần biết:
ÔÇô N├¬u ─æã░ß╗úc kh├íi niß╗çm oxide.
ÔÇô Viß║┐t ─æã░ß╗úc phã░ãíng tr├¼nh ho├í hß╗ìc tß║ío oxide tß╗½ kim loß║íi/phi kim vß╗øi oxygen.
ÔÇô Ph├ón loß║íi oxide (theo khß║ú n─âng phß║ún ß╗®ng vß╗øi dung dß╗ïch acid/base).
ÔÇô Tiß║┐n h├ánh ─æã░ß╗úc th├¡ nghiß╗çm oxide kim loß║íi phß║ún ß╗®ng vß╗øi dung dß╗ïch acid; oxide phi kim phß║ún ß╗®ng vß╗øi dung dß╗ïch base; n├¬u v├á giß║úi th├¡ch ─æã░ß╗úc hiß╗çn tã░ß╗úng xß║úy ra trong th├¡ nghiß╗çm (viß║┐t phã░ãíng tr├¼nh ho├í hß╗ìc) v├á r├║t ra nhß║¡n x├®t vß╗ü t├¡nh chß║Ñt ho├í hß╗ìc cß╗ºa oxide.
3.1. Trß║»c nghiß╗çm B├ái 12 Khoa hß╗ìc tß╗▒ nhi├¬n 8 Ch├ón trß╗Øi s├íng tß║ío
C├íc em c├│ thß╗â hß╗ç thß╗æng lß║íi nß╗Öi dung kiß║┐n thß╗®c ─æ├ú hß╗ìc ─æã░ß╗úc th├┤ng qua b├ái kiß╗âm tra Trß║»c nghiß╗çm KHTN 8 Ch├ón trß╗Øi s├íng tß║ío B├ái 12 cß╗▒c hay c├│ ─æ├íp ├ín v├á lß╗Øi giß║úi chi tiß║┐t.
-
- A. Muối.
- B. Acid.
- C. Base.
- D. Oxide.
-
- A. t├íc dß╗Ñng vß╗øi dung dß╗ïch acid tß║ío th├ánh muß╗æi v├á nã░ß╗øc.
- B. t├íc dß╗Ñng vß╗øi dung dß╗ïch base tß║ío th├ánh muß╗æi v├á nã░ß╗øc.
- C. kh├┤ng t├íc dß╗Ñng vß╗øi dung dß╗ïch base v├á dung dß╗ïch acid.
- D. chß╗ë t├íc dß╗Ñng ─æã░ß╗úc vß╗øi muß╗æi.
-
- A. CO2.
- B. CO.
- C. C2O.
- D. H2CO3.
C├óu 4-10: Mß╗Øi c├íc em ─æ─âng nhß║¡p xem tiß║┐p nß╗Öi dung v├á thi thß╗¡ Online ─æß╗â cß╗ºng cß╗æ kiß║┐n thß╗®c vß╗ü b├ái hß╗ìc n├áy nh├®!
3.2. B├ái tß║¡p SGK B├ái 12 Khoa hß╗ìc tß╗▒ nhi├¬n 8 Ch├ón trß╗Øi s├íng tß║ío
C├íc em c├│ thß╗â xem th├¬m phß║ºn hã░ß╗øng dß║½n Giß║úi b├ái tß║¡p KHTN 8 Ch├ón trß╗Øi s├íng tß║ío B├ái 12 ─æß╗â gi├║p c├íc em nß║»m vß╗»ng b├ái hß╗ìc v├á c├íc phã░ãíng ph├íp giß║úi b├ái tß║¡p.
Đang cập nhật câu hỏi và gợi Û làm bài.
Hß╗Åi ─æ├íp B├ái 12 Khoa hß╗ìc tß╗▒ nhi├¬n 8 Ch├ón trß╗Øi s├íng tß║ío
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Khoa học tự nhiên HOC247 sẛ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!




.JPG)

.JPG)