Hướng dẫn Giải bài tập Khoa học tự nhiên 7 Kết nối tri thức Chương 1 Bài 2 Nguyên tử sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức.
-
Giải câu hỏi trang 14 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Theo Đê – mô – crit và Đan – tơn, nguyên tử được quan niệm như thế nào?
-
Hoạt động trang 16 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Làm mô hình nguyên tử carbon theo Bo
Chuẩn bị: bìa carton, giấy màu vàng, các viên bi nhựa to màu đỏ và các viên bi nhỏ màu xanh.
Tiến hành:
Gắn viên bi đỏ vào bìa carton làm hạt nhân nguyên tử carbon. Cắt giấy màu vàng thành hai đường tròn có bán kính khác nhau và mỗi vòng tròn có độ dày khoảng 1 cm (Hình 2.3).
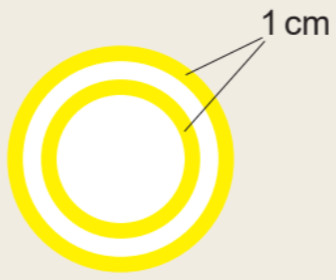
Hình 2.3
Dán các đường tròn lên bìa carton sao cho tâm của hai đường tròn là viên bi đỏ. Gắn các viên bi màu xanh lên hai đường tròn màu vàng như Hình 2.2b
a) Nguyên tử hydrogen b) Nguyên tử carbon
Hình 2.2. Mô hình nguyên tử của hydrogen và carbon theo Bo
Thảo luận nhóm và trả lời câu hỏi:
1. Các đường tròn bằng giấy màu vàng biểu diễn gì?
2. Em hãy cho biết số electron có trong lớp electron thứ nhất và thứ hai của nguyên tử carbon và chỉ ra lớp electron đã chứa tối đa electron
-
Giải câu hỏi 1 trang 16 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
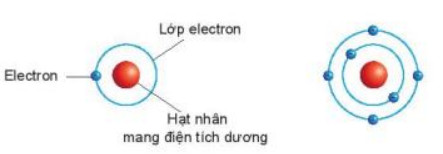
Quan sát Hình 2.1 và cho biết các thành phần cấu tạo nên nguyên tử.
.jpg)
Hình 2.1. Mô hình hành tinh nguyên tử Rơ-dơ-pho
-
Giải câu hỏi 2 trang 16 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Quan sát Hình 2.2, áp dụng mô hình nguyên tử của Bo, mô tả cấu tạo của nguyên tử hydrogen và nguyên tử carbon

a) Nguyên tử hydrogen b) Nguyên tử carbon
Hình 2.2. Mô hình nguyên tử của hydrogen và carbon theo Bo
- VIDEOYOMEDIA
-
Giải câu hỏi 3 trang 16 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Quan sát Hình 2.4 và cho biết:
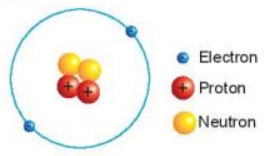
Hình 2.4. Mô hình nguyên tử Helium
1. Hạt nhân nguyên tử có một hay nhiều hạt? Các hạt đó thuộc cùng một loại hạt hay nhiều loại hạt?
2. Số đơn vị điện tích hạt nhân của helium bằng bao nhiêu?
-
Hoạt động trang 17 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Tìm hiểu cấu tạo một số nguyên tử
Chuẩn bị: Mô hình nguyên tử của các nguyên tử carbon, nitrogen, oxygen theo Hình 2.5.
.jpg)
Hinh 2.5. Mô hình nguyên tử của carbon, nitrogen và oxygen
Quan sát các mô hình nguyên tử đã chuẩn bị, thảo luận nhóm, hoàn thành bảng theo mẫu sau và trả lời câu hỏi:
.jpg)
1. So sánh số electron trên từng lớp electron tương ứng trong các nguyên tử trên.
2. Số electron ở lớp electron ngoài cùng của vỏ mỗi nguyên tử trên đã được điền tối đa chưa? Cần thêm bao nhiêu electron để lớp electron ngoài cùng của mỗi nguyên tử trên có số electron tối đa?
-
Giải câu hỏi 1 trang 18 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Quan sát Hình 2.6 và cho biết:
1. Thứ tự sắp xếp các electron ở vỏ nguyên tử chlorine
2. Số electron trên từng lớp ở vỏ nguyên tử chlorine
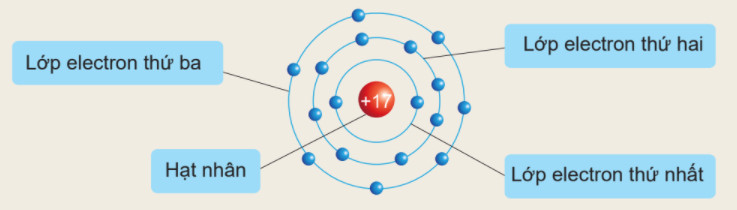
Hình 2.6. Sơ đồ các lớp electron của nguyên tử chlorine
-
Giải câu hỏi 2 trang 18 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Em hãy cho biết vì sao khối lượng hạt nhân nguyên tử có thể coi là khối lượng của nguyên tử.
-
Giải câu hỏi 3 trang 18 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Hãy so sánh khối lượng của nguyên tử nhôm (13p, 14n) và nguyên tử đồng (29p, 36n).
-
Giải bài 2.1 trang 7 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Phát biểu nào sau đây không mô tả đúng mô hình nguyên tử của Rơ-dơ-pho – Bo?
A. Nguyên tử có cấu tạo rỗng, gồm hạt nhân ở tâm nguyên tử và các electron ở vỏ nguyên tử.
B. Nguyên tử có cấu tạo đặc khít, gồm hạt nhân nguyên tử và các electron.
C. Electron chuyển động xung quanh hạt nhân theo những quỹ đạo xác định tạo thành các lớp electron.
D. Hạt nhân nguyên tử mang điện tích dương, electron mang điện tích âm.
-
Giải bài 2.2 trang 7 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Phát biểu nào sau đây không mô tả đúng vỏ nguyên tử theo mô hình nguyên tử của Rơ-dơ-pho – Bo?
A. Electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau tạo thành các lớp electron.
B. Lớp electron trong cùng gần hạt nhân nhất có tối đa 2 electron, các lớp electron khác có chứa tối đa 8 electron hoặc nhiều hơn.
C. Lớp electron trong cùng gần hạt nhân nhất có tối đa 8 electron, các lớp electron khác có chứa tối đa nhiều hơn 8 electron.
D. Các electron sắp xếp vào các lớp theo thứ tự từ trong ra ngoài cho đến hết.
-
Giải bài 2.3 trang 7 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Trừ hạt nhân của nguyên tử hydrogen, hạt nhân các nguyên tử còn lại được tạo thành từ hạt
A. electron và proton.
B. electron, proton và neutron.
C. neutron và electron.
D. proton và neutron.
-
Giải bài 2.4 trang 7 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Cho các phát biểu:
(1) Nguyên tử trung hòa về điện.
(2) Khối lượng của nguyên tử tập trung chủ yếu ở hạt nhân.
(3) Trong nguyên tử, số hạt mang điện tích dương bằng số hạt mang điện tích âm nên số hạt electron bằng số hạt neutron.
(4) Vỏ nguyên tử, gồm các lớp electron có khoảng cách khác nhau đối với hạt nhân.
Trong các phát biểu trên, số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
-
Giải bài 2.5 trang 8 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Hãy viết tên, điện tích và khối lượng của các hạt cấu tạo nên nguyên tử vào chỗ trống để hoàn thiện bảng dưới đây.

-
Giải bài 2.6 trang 8 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Từ Hình 2.1 mô phỏng một nguyên tử carbon, hãy cho biết trong một nguyên tử carbon có bao nhiêu hạt electron, proton, neutron.
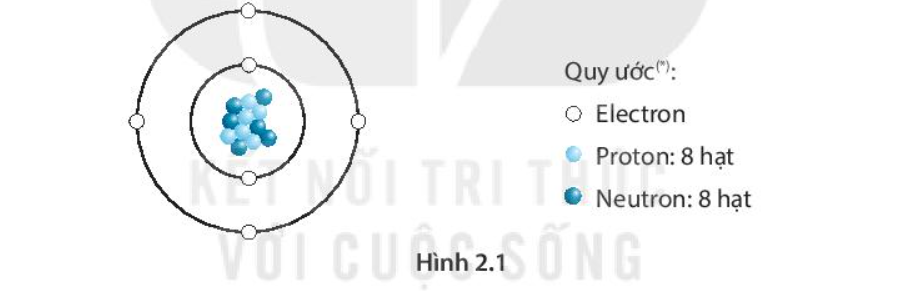
-
Giải bài 2.7 trang 8 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Mặt Trời chứa chủ yếu hai nguyên tố hóa học là hydrogen (H) và helium (He). Hình biểu diễn một nguyên tử hydrogen và một nguyên tử helium.
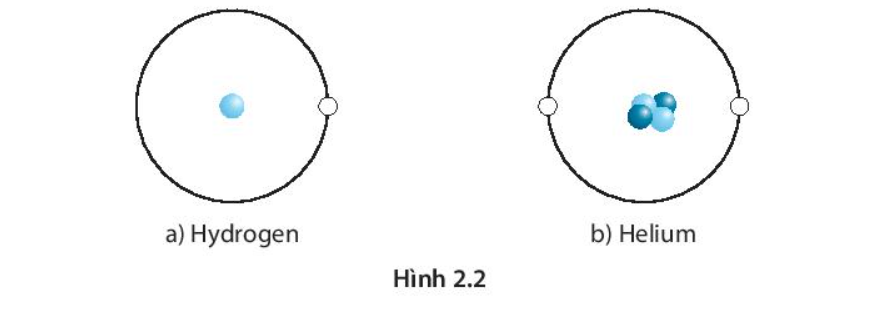
Dựa vào hình vẽ trên hãy cho biết:
a) Mỗi vòng tròn xung quanh hạt nhân được gọi là gì?
A. Một liên kết.
B. Một electron.
C. Một lớp vỏ electron.
D. Một proton.
b) Có bao nhiêu electron trong lớp vỏ của nguyên tử H, He? Có bao nhiêu proton trong hạt nhân của nguyên tử H, He?
-
Giải bài 2.8 trang 9 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Giải thích vì sao có thể coi khối lượng nguyên tử tập trung ở hạt nhân, lấy ví dụ về một nguyên tử để minh họa.
-
Giải bài 2.9 trang 9 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Nguyên tử lithium có 3 proton.
a) Có bao nhiêu electron trong nguyên tử lithium?
b) Biết hạt nhân nguyên tử lithium có 4 neutron, tính khối lượng nguyên tử của lithium theo đơn vị amu.
-
Giải bài 2.10 trang 9 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Mô tả sự khác nhau giữa cấu tạo một nguyên tử hydrogen và cấu tạo một nguyên tử helium.
-
Giải bài 2.11 trang 9 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Oxygen là nguyên tố hóa học phổ biến trong không khí, duy trì sự sống và sự cháy. Hoàn thiện Hình 2.3 để mô tả cấu tạo một nguyên tử oxygen.
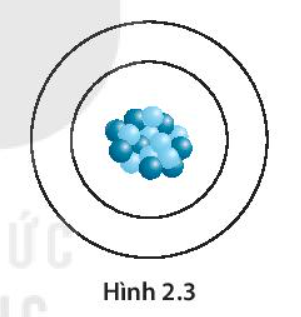
-
Giải bài 2.12 trang 9 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Một nguyên tử có 10 proton trong hạt nhân. Theo mô hình nguyên tử của Ro-dơ-pho – Bo, số lớp electron của nguyên tố đó là
A. 1.
B. 2.
C. 3.
D. 4.
-
Giải bài 2.13 trang 9 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Trong một nguyên tử có số proton bằng 5, số electron trong các lớp của vỏ nguyên tử, viết từ lớp trong ra lớp ngoài, lần lượt là
A. 1, 2, 8.
B. 2, 8, 1.
C. 2, 3.
D. 3, 2.
-
Giải bài 2.14 trang 9 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Nitrogen là nguyên tố hóa học phổ biến trong không khí. Trong hạt nhân nguyên tử nitrogen có 7 proton. Số electron trong các lớp của vỏ nguyên tử nitrogen, viết từ lớp trong ra lớp ngoài, lần lượt là
A. 7.
B. 2, 5.
C. 2, 2, 3.
D. 2, 4, 1.
-
Giải bài 2.15 trang 10 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Trong hạt nhân nguyên tử fluorine có 9 proton. Số electron ở lớp ngoài cùng của vỏ nguyên tử fluorine là?
A. 2.
B. 5.
C. 7.
D. 8.
-
Giải bài 2.16 trang 10 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Nguyên tử calcium có 20 electron ở vỏ nguyên tử. Hạt nhân của nguyên tử có calcium có số proton là
A. 2.
B. 10.
C. 18.
D. 20.
-
Giải bài 2.17 trang 10 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Nguyên tử aluminium có 13 electron ở vỏ. Số electron ở lớp trong cùng của nguyên tử aluminium là
A. 2.
B. 8.
C. 10.
D. 18.
-
Giải bài 2.18 trang 10 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Muối ăn chứa hai nguyên tố hóa học là sodium và chlorine. Trong hạt nhân nguyên tử của các nguyên tố sodium và chlorine có lần lượt 11 và 17 proton. Số electron ở lớp ngoài cùng của vỏ nguyên tử sodium và chlorine lần lượt là
A. 1 và 7.
B. 3 và 9.
C. 9 và 15.
D. 3 và 7.
-
Giải bài 2.19 trang 10 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Trong hạt nhân nguyên tử sulfur có 16 proton. Số electron trong các lớp của vỏ nguyên tử sulfur, viết từ trong ra lớp ngoài, lần lượt là
A. 2, 10, 6.
B. 2, 6 8.
C. 2, 8, 6.
D. 2, 9, 5.
-
Giải bài 2.20 trang 10 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Trong hạt nhân nguyên tử của nguyên tố silicon có 14 proton, vỏ nguyên tử silicon có ba lớp electron. Hãy hoàn thiện hình 2.4 để mô tả mô hình một nguyên tử silicon.
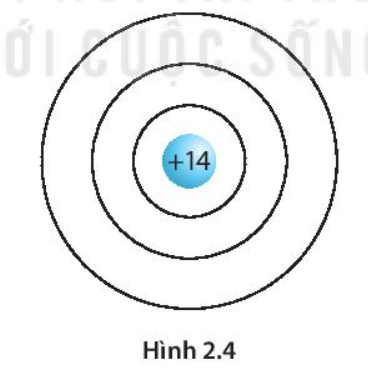
-
Giải bài 2.21 trang 10 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Hạt nhân một nguyên tử flourine có 9 proton và 10 neutron. Khối lượng của nguyên tử flourine xấp xỉ bằng
A. 9 amu.
B. 10 amu.
C. 19 amu.
D. 28 amu.
-
Giải bài 2.22 trang 11 SBT Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Muối ăn chứa hai nguyên tố hóa học là sodium và chlorine. Trong hạt nhân nguyên tử của các nguyên tố sodium và chlorine có lần lượt 11 và 17 proton. Số electron trong các lớp của vỏ nguyên tử sodium và chlorine, viết từ lớp trong ra lớp ngoài, lần lượt là
A. 2, 9 và 2, 10, 5.
B. 2, 9 và 2, 8, 7.
C. 2, 8, 1 và 2, 8, 7
D. 2, 8, 1 và 2, 8, 5.





