Giải bài 14.3 trang 36 SBT Hóa học 10 Kết nối tri thức
Liên kết ion khác với liên kết cộng hoá trị ở điểm nào sau đây?
A. Tính bão hoà lớp electron ở vỏ nguyên tử.
B. Tuân theo quy tắc octet.
C. Tạo ra hợp chất bền vững hơn.
D. Tính không định hướng.
Hướng dẫn giải chi tiết bài 14.3
Phương pháp giải:
Dựa vào sự khác nhau giữa hai loại liên kết
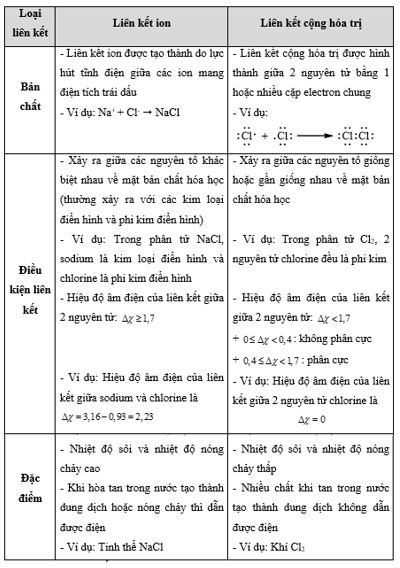
Lời giải chi tiết:
Đáp án: D
Sửa: Một electron của nguyên tử hydrogen và một electron của nguyên tử chlorine được góp chung và lệch về phía nguyên tử Cl.
-- Mod Hóa Học 10 HỌC247
Bài tập SGK khác
Giải bài 14.1 trang 36 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.2 trang 36 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.4 trang 36 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.5 trang 36 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.6 trang 36 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.7 trang 37 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.8 trang 37 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.9 trang 37 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.10 trang 37 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.11 trang 37 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.12 trang 37 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.13 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.14 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.15 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.16 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT
Giải bài 14.17 trang 38 SBT Hóa học 10 Kết nối tri thức - KNTT
-

 Theo dõi (0) 1 Trả lời
Theo dõi (0) 1 Trả lời





