N·ªôi dung t√Ýi li·ªáu ƒê·ªÅ thi gi·ªØa HK1 m√¥n H√≥a h·ªçc 10 KNTT c√≥ ƒë√°p √°n nƒÉm 2022-2023 Tr∆∞·ªùng THPT Nguy·ªÖn Qu√°n Nho ƒë∆∞·ª£c bi√™n so·∫°n b·ªüi ƒë·ªôi ng≈© gi√°o vi√™n HOC247 d∆∞·ªõi ƒë√¢y s·∫Ω gi√∫p c√°c em r√®n luy·ªán kƒ© nƒÉng gi·∫£i ƒë·ªÅ, chu·∫©n b·ªã cho k√¨ k√¨ thi gi·ªØa HK1 s·∫Øp t·ªõi. Hi v·ªçng v·ªõi t√Ýi li·ªáu d∆∞·ªõi ƒë√¢y s·∫Ω gi√∫p c√°c em √¥n t·∫≠p v√Ý h·ªá th·ªëng h√≥a l·∫°i c√°c ki·∫øn th·ª©c H√≥a h·ªçc 10 KNTT ƒë√£ h·ªçc. Ch√∫c c√°c em h·ªçc t·∫≠p t·ªët!
|
TRƯỜNG THPT NGUYỄN QUÁN NHO |
ƒê·ªÄ THI GI·ªÆA H·ªåC K√å I NƒÇM H·ªåC 2022-2023 M√îN H√ìA H·ªåC 10 KNTT Th·ªùi gian l√Ým b√Ýi: 45 ph√∫t |
A. TRẮC NGHIỆM (7 điểm)
C√¢u 1. Trong nguy√™n t·ª≠, lo·∫°i h·∫°t c√≥ kh·ªëi l∆∞·ª£ng kh√¥ng ƒë√°ng k·ªÉ so v·ªõi c√°c h·∫°t c√≤n l·∫°i l√Ý
A. Proton.
B. Neutron.
C. Electron.
D. Neutron v√Ý electron.
Câu 2. Số N trong nguyên tử của một nguyên tố hoá học có thể tính được khi biết số khối A, số thứ tự của nguyên tố (Z) theo công thức:
A. A = Z – N
B. N = A – Z
C. A = N – Z
D. Z = N + A
C√¢u 3. H√¨nh ·∫£nh d∆∞·ªõi ƒë√¢y m√¥ t·∫£ th√≠ nghi·ªám ch·ª©ng minh nguy√™n t·ª≠ c√≥ c·∫•u t·∫°o r·ªóng. Hi·ªán t∆∞·ª£ng n√Ýo ch·ª©ng t·ªè ƒëi·ªÅu ƒë√≥?
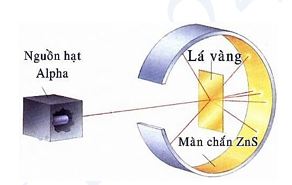
A. Chùm α truyền thẳng.
B. Chùm α bị bật ngược trở lại.
C. Chùm α bị lệch hướng.
D. Chùm α không thể bị xuyên qua.
C√¢u 4. Khi n√≥i v·ªÅ s·ªë kh·ªëi, ƒëi·ªÅu kh·∫≥ng ƒë·ªãnh n√Ýo sau ƒë√¢y lu√¥n ƒë√∫ng?
Trong nguyên tử, số khối
A. b·∫±ng t·ªïng kh·ªëi l∆∞·ª£ng c√°c h·∫°t proton v√Ý neutron.
B. b·∫±ng t·ªïng s·ªë c√°c h·∫°t proton v√Ý neutron.
C. bằng nguyên tử khối.
D. b·∫±ng t·ªïng c√°c h·∫°t proton, neutron v√Ý electron.
C√¢u 5. Nguy√™n t·ª≠ c·ªßa nguy√™n t·ªë X c√≥ t·ªïng s·ªë h·∫°t proton, neutron v√Ý electron l√Ý 40. T·ªïng s·ªë h·∫°t mang ƒëi·ªán nhi·ªÅu h∆°n t·ªïng s·ªë h·∫°t kh√¥ng mang ƒëi·ªán l√Ý 12 h·∫°t. Nguy√™n t·ªë X c√≥ s·ªë kh·ªëi l√Ý
A. 26.
B. 27.
C. 28.
D. 23.
C√¢u 6. M·ªôt nguy√™n t·ª≠ c√≥ 9 electron ·ªü l·ªõp v·ªè, h·∫°t nh√¢n c·ªßa n√≥ c√≥ 10 neutron. S·ªë hi·ªáu nguy√™n t·ª≠ l√Ý
A. 9.
B. 18.
C. 19.
D. 28.
Câu 7. Nguyên tử X có 26 proton trong hạt nhân. Cho các phát biểu sau về X:
(1) X có 26 neutron trong hạt nhân.
(2) X có 26 electron ở vỏ nguyên tử.
(3) X c√≥ ƒëi·ªán t√≠ch h·∫°t nh√¢n l√Ý +26.
(4) Kh·ªëi l∆∞·ª£ng nguy√™n t·ª≠ X l√Ý 26 amu.
Trong c√°c ph√°t bi·ªÉu tr√™n, s·ªë ph√°t bi·ªÉu ƒë√∫ng l√Ý
A. 1.
B. 2.
C. 3.
D. 4.
C√¢u 8. Qui ∆∞·ªõc l·∫•y amu (hay ƒëvC) l√Ým kh·ªëi l∆∞·ª£ng nguy√™n t·ª≠. M·ªôt amu c√≥ kh·ªëi l∆∞·ª£ng b·∫±ng:
A. 12 khối lượng nguyên tử C.
B. 1,6605.10-27kg.
C. 1,6605.10-25kg.
D. 1,6605.10-25g.
C√¢u 9. H·∫°t nh√¢n nguy√™n t·ª≠ ƒë∆∞·ª£c t√¨m ra nƒÉm 1911 b·∫±ng c√°ch cho h·∫°t Œ± b·∫Øn ph√° m·ªôt l√° v√Ýng m·ªèng. Th√≠ nghi·ªám tr√™n ƒë∆∞·ª£c ƒë∆∞a ra ƒë·∫ßu ti√™n do nh√Ý b√°c h·ªçc n√Ýo say ƒë√¢y?
A. Mendeleep.
B. Chatwick.
C. Rutherfor.
D. Thomson.
C√¢u 10. ƒê·ªÉ ƒëo k√≠ch th∆∞·ªõc c·ªßa h·∫°t nh√¢n, nguy√™n t·ª≠..hay c√°c h·ªá vi m√¥ kh√°c, ng∆∞·ªùi ta kh√¥ng d√πng c√°c ƒë∆°n v·ªã ƒëo ph·ªï bi·∫øn ƒë·ªëi v·ªõi c√°c h·ªá vƒ© m√¥ nh∆∞ cm, m, km.. m√Ý th∆∞·ªùng d√πng ƒë∆°n v·ªã ƒëo nanomet (nm) hay angstron (√Ö). C√°ch ƒë·ªïi ƒë∆°n v·ªã ƒë√∫ng l√Ý:
A. 1nm = 10–10m.
B. 1 Å =10–9m.
C. 1nm =10–7cm.
D. 1 √Ö =10nm.
---(Để xem nội dung chi tiết từ câu 11 đến câu 28, các em vui lòng xem online hoặc đăng nhập hoc247.net tải về máy)---
B. TỰ LUẬN (3 điểm)
B√Ýi 1. (1,0 ƒëi·ªÉm)
Viết cấu hình electron nguyên tử của các nguyên tố carbon (Z = 6), sodium (Z = 11).
Cho bi·∫øt s·ªë electron l·ªõp ngo√Ýi c√πng trong nguy√™n t·ª≠ c·ªßa c√°c nguy√™n t·ªë tr√™n? ch√∫ng l√Ý kim lo·∫°i, phi kim hay kh√≠ hi·∫øm?
B√Ýi 2. (2,0 ƒëi·ªÉm)
(a) Nguy√™n t·ª≠ kh·ªëi trung b√¨nh c·ªßa vanadium (V) l√Ý 50,9975. Nguy√™n t·ªë V c√≥ 2 ƒë·ªìng v·ªã trong ƒë√≥ ƒë·ªìng v·ªã chi·∫øm 0,25% v·ªÅ s·ªë l∆∞·ª£ng nguy√™n t·ª≠. T√≠nh s·ªë kh·ªëi c·ªßa ƒë·ªìng v·ªã c√≤n l·∫°i.
(b) Nguy√™n t·ª≠ c·ªßa nguy√™n t·ªë X c√≥ t·ªïng s·ªë h·∫°t proton, electron, neutron l√Ý 49, trong ƒë√≥ s·ªë h·∫°t kh√¥ng mang ƒëi·ªán b·∫±ng 53,125% s·ªë h·∫°t mang ƒëi·ªán.
X√°c ƒë·ªãnh ƒëi·ªán t√≠ch h·∫°t nh·∫≠n, s·ªë proton, s·ªë electron, s·ªë neutron v√Ý s·ªë kh·ªëi c·ªßa X?
ĐÁP ÁN
A. TRẮC NGHIỆM (7 điểm)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
C |
B |
A |
B |
B |
A |
B |
B |
C |
C |
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
A |
D |
B |
A |
A |
D |
B |
B |
B |
A |
|
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
||
|
B |
C |
C |
A |
D |
C |
B |
C |
B. TỰ LUẬN (3 điểm)
B√Ýi 1
Carbon (Z = 6): 1s22s22p2
‚áí C√≥ 4 electron ·ªü l·ªõp ngo√Ýi c√πng, l√Ý nguy√™n t·ªë phi kim.
Sodium (Z = 11): 1s22s22p63s1
‚áí C√≥ 1 electron ·ªü l·ªõp ngo√Ýi c√πng, l√Ý nguy√™n t·ªë kim lo·∫°i.
B√Ýi 2
a.
G·ªçi s·ªë kh·ªëi ƒë·ªìng v·ªã c√≤n l·∫°i l√Ý a. Ta c√≥ ph∆∞∆°ng tr√¨nh
\(\overline {{A_V}} = \frac{{50.0,25 + a.99,75}}{{100}} = 50,9975 \Rightarrow a = 51\)
V·∫≠y s·ªë kh·ªëi ƒë·ªìng v·ªã c√≤n l·∫°i c·ªßa vanadium l√Ý 51
b.
G·ªçi s·ªë electron = s·ªë proton trong X l√Ý Z; s·ªë neutron trong X l√Ý N.
T·ªïng s·ªë proton, electron v√Ý neutron trong X l√Ý 49 n√™n 2Z + N = 49 (1).
Số hạt không mang điện bằng 53,125% số hạt mang điện
\(\Rightarrow N = 2Z \times 53,125\% \Leftrightarrow 17Z - 16N{\rm{ }} = 0\)(2).
T·ª´ (1) v√Ý (2) ta c√≥ Z = 16, N = 17
Nguy√™n t·ª≠ nguy√™n t·ªë X c√≥ ƒëi·ªán t√≠ch h·∫°t nh√¢n l√Ý +16; 16 proton; 16 electron; 17 neutron v√Ý c√≥ s·ªë kh·ªëi
\({A_X} = 16 + 17 = 33\)
Tr√™n ƒë√¢y l√Ý m·ªôt ph·∫ßn tr√≠ch ƒëo·∫°n n·ªôi dung ƒê·ªÅ thi gi·ªØa HK1 m√¥n H√≥a h·ªçc 10 KNTT c√≥ ƒë√°p √°n nƒÉm 2022-2023 Tr∆∞·ªùng THPT Nguy·ªÖn Qu√°n Nho. ƒê·ªÉ xem th√™m nhi·ªÅu t√Ýi li·ªáu tham kh·∫£o h·ªØu √≠ch kh√°c c√°c em ch·ªçn ch·ª©c nƒÉng xem online ho·∫∑c ƒëƒÉng nh·∫≠p v√Ýo trang hoc247.net ƒë·ªÉ t·∫£i t√Ýi li·ªáu v·ªÅ m√°y t√≠nh.
Hy v·ªçng t√Ýi li·ªáu n√Ýy s·∫Ω gi√∫p c√°c em h·ªçc sinh √¥n t·∫≠p t·ªët v√Ý ƒë·∫°t th√Ýnh t√≠ch cao trong h·ªçc t·∫≠p.
C√°c em quan t√¢m c√≥ th·ªÉ tham kh·∫£o t√Ýi li·ªáu c√πng chuy√™n m·ª•c:
- Bộ 5 đề thi giữa HK1 môn Tiếng Anh 10 KNTT năm 2022-2023 có đáp án Trường THPT Phan Bội Châu
- Bộ 3 Đề thi giữa HK1 môn Công Nghệ 10 KNTT năm 2022-2023 Trường THPT Nguyễn Trãi có đáp án
Chúc các em học tập tốt !
T√Ýi li·ªáu li√™n quan
Tư liệu nổi bật tuần
- Xem thêm


