HOC 247 xin mб»қi cГЎc em hб»Қc sinh lб»ӣp 12 cГ№ng tham khбәЈo:
Nб»ҷi dung tГ i liб»Үu Bб»ҷ 5 Д‘б»Ғ thi thб»ӯ THPT QG mГҙn HГіa hб»Қc nДғm 2021-2022 cГі Д‘ГЎp ГЎn TrЖ°б»қng THPT Cao ThбәҜng Д‘б»ғ cГі thб»ғ Гҙn tбәӯp vГ củng cб»‘ cГЎc kiбәҝn thб»©c, chuбә©n bб»Ӣ tб»‘t cho kГ¬ thi sбәҜp tб»ӣi. ChГәc cГЎc em hб»Қc tбәӯp tб»‘t vГ Д‘бәЎt kбәҝt quбәЈ cao.
|
TRЖҜб»ңNG THPT CAO THбә®NG |
Дҗб»Җ THI THỬ THPT QUб»җC GIA MГ”N HГ“A Hб»ҢC NДӮM Hб»ҢC 2021-2022 Thб»қi gian 60 phГәt |
Дҗб»Ғ thi sб»‘ 1
CГўu 41: TГӯnh chбәҘt hГіa hб»Қc Д‘бә·c trЖ°ng của anken:
A. phбәЈn б»©ng thбәҝ.
B. phбәЈn б»©ng oxi hГіa hoГ n toГ n.
C. phбәЈn б»©ng cб»ҷng.
D. phбәЈn б»©ng crackinh.
CГўu 42: CГЎc khГӯ thбәЈi cГҙng nghiб»Үp vГ của cГЎc Д‘б»ҷng cЖЎ Гҙ tГҙ, xe mГЎy... lГ nguyГӘn nhГўn chủ yбәҝu gГўy ra mЖ°a axit. Nhб»Ҝng thГ nh phбә§n hГіa hб»Қc chủ yбәҝu trong cГЎc khГӯ thбәЈi trб»ұc tiбәҝp gГўy ra mЖ°a axit lГ
A. NO2, CO2, CO. B. SO2, CO, NO. C. SO2, CO, NO2. D. NO, NO2, SO2.
CГўu 43: Cho cГЎc phГЎt biб»ғu sau:
(1) Crom, sбәҜt, thiбәҝc khi tГЎc dб»Ҙng vб»ӣi dung dб»Ӣch HCl loГЈng nГіng cho muб»‘i cГі hГіa trб»Ӣ II.
(2) NhГҙm, sбәҜt, crom bб»Ӣ thб»Ҙ Д‘б»ҷng bб»ҹi dung dб»Ӣch axit HNO3 Д‘бә·c nguб»ҷi.
(3) б»һ nhiб»Үt Д‘б»ҷ thЖ°б»қng Be, Ca, Ba Д‘б»Ғu khб»ӯ Д‘Ж°б»Јc nЖ°б»ӣc giбәЈi phГіng hidro.
(4) CГЎc hiД‘roxit của nhГҙm, crom, kбәҪm Д‘б»Ғu lГ chбәҘt lЖ°б»Ўng tГӯnh.
(5) NhГҙm hidroxit tan Д‘Ж°б»Јc trong dung dб»Ӣch amoniac.
CГі bao nhiГӘu phГЎt biб»ғu Д‘Гәng?
A. 2. B. 4. C. 3. D. 5.
CГўu 44: Cho dГЈy cГЎc chбәҘt: C2H5OH, C12H22O11 (saccarozЖЎ), CH3COOH, Ca(OH)2, CH3COONH4, KAl(SO4)2.12H2O. Sб»‘ chбәҘt Д‘iб»Үn li lГ
A. 3. B. 2. C. 5. D. 4.
CГўu 45: Trong thГӯ nghiб»Үm nГ o sau Д‘Гўy xбәЈy ra Дғn mГІn Д‘iб»Үn hГіa?
A. Cho lГЎ Д‘б»“ng nguyГӘn chбәҘt vГ o dung dб»Ӣch gб»“m Fe(NO3)3 vГ HNO3.
B. Cho lГЎ sбәҜt nguyГӘn chбәҘt vГ o dung dб»Ӣch gб»“m CuSO4 vГ H2SO4 loГЈng.
C. NhГәng thanh kбәҪm nguyГӘn chбәҘt vГ o dung dб»Ӣch HCl.
D. Дҗб»ғ thanh thГ©p Д‘ГЈ sЖЎn kГӯn trong khГҙng khГӯ khГҙ.
CГўu 46: Cho 6,6 gam CH3CHO tГЎc dб»Ҙng vб»ӣi lЖ°б»Јng dЖ° dung dб»Ӣch AgNO3 trong NH3, thu Д‘Ж°б»Јc m gam Ag. GiГЎ trб»Ӣ của m lГ
A. 32,4. B. 21,6. C. 64,8. D. 16,2.
CГўu 47: Cho cГЎc thГӯ nghiб»Үm vб»ӣi mб»ҷt sб»‘ hiб»Үn tЖ°б»Јng sau:
(1) Khi thГӘm (dЖ°) NaOH vГ o dung dб»Ӣch K2Cr2O7 thГ¬ dung dб»Ӣch chuyб»ғn tб»« mГ u da cam sang mГ u vГ ng.
(2) Khi thГӘm tб»« tб»« dung dб»Ӣch hб»—n hб»Јp H2SO4 loГЈng vГ FeSO4 vГ o dung dб»Ӣch chб»©a K2Cr2O7, thГ¬ dung dб»Ӣch tб»« mГ u da cam chuyб»ғn dбә§n thГ nh mГ u xanh.
(3) ThГӘm tб»« tб»« dung dб»Ӣch NaOH vГ o dung dб»Ӣch CrCl3 thбәҘy xuбәҘt hiб»Үn kбәҝt tủa vГ ng nГўu sau Д‘Гі tan dбә§n cho Д‘бәҝn hбәҝt trong dung dб»Ӣch NaOH (dЖ°).
(4) ThГӘm tб»« tб»« Д‘бәҝn dЖ° dung dб»Ӣch HCl vГ o dung dб»Ӣch Na[Cr(OH)4] thбәҘy xuбәҘt hiб»Үn kбәҝt tủa lб»Ҙc xГЎm, sau Д‘Гі tan hoГ n toГ n tбәЎo dung dб»Ӣch trong suб»‘t.
Sб»‘ hiб»Үn tЖ°б»Јng Д‘Ж°б»Јc mГҙ tбәЈ Д‘Гәng lГ
A. 2. B. 4. C. 3. D. 1.
CГўu 48: Hiб»Үn tЖ°б»Јng gГ¬ xбәЈy ra khi Д‘un nГіng toluen vб»ӣi dung dб»Ӣch KMnO4?
A. KhГҙng cГі hiб»Үn tЖ°б»Јng gГ¬. B. Sủi bб»Қt khГӯ.
C. CГі kбәҝt tủa trбәҜng. D. Dung dб»Ӣch KMnO4 bб»Ӣ mбәҘt mГ u.
CГўu 49: TГӯnh chбәҘt vбәӯt lГӯ nГ o sau Д‘Гўy khГҙng phбәЈi lГ tГӯnh chбәҘt vбәӯt lГӯ chung của kim loбәЎi?
A. ГҒnh kim.
B. TГӯnh dбә«n Д‘iб»Үn vГ nhiб»Үt.
C. TГӯnh cб»©ng.
D. TГӯnh dбә»o.
CГўu 50: Trong cГЎc tЖЎ sau: tЖЎ xenlulozЖЎ triaxetat, tЖЎ tбәұm, tЖЎ visco, tЖЎ nitron, bГҙng, tЖЎ nilon - 6,6, tЖЎ capron. CГі bao nhiГӘu tЖЎ lГ tЖЎ hГіa hб»Қc?
A. 7. B. 5. C. 4. D. 6.
CГўu 51: Cho cГЎc chбәҘt: (1) NaHCO3; (2) Ca(OH)2; (3) HCl; (4) Na3PO4; (5) NaOH. ChбәҘt nГ o trong sб»‘ cГЎc chбәҘt trГӘn khГҙng cГі khбәЈ nДғng lГ m giбәЈm Д‘б»ҷ cб»©ng của nЖ°б»ӣc?
A. (3), (5). B. (2), (5). C. (1), (3). D. (2), (4).
CГўu 52: Trong cГЎc ion sau Д‘Гўy, ion nГ o cГі tГӯnh oxi hГіa mбәЎnh nhбәҘt?
A. Ca2+. B. Ag+. C. Cu2+. D. Zn2+.
CГўu 53: Cho dГЈy cГЎc chбәҘt: axit fomic, ancol etylic, glixerol, tristearin vГ etyl axetat. Sб»‘ chбәҘt trong dГЈy phбәЈn б»©ng vб»ӣi Cu(OH)2 б»ҹ Д‘iб»Ғu kiб»Үn thЖ°б»қng lГ
A. 5. B. 4. C. 3. D. 2.
CГўu 54: Cho phenol lб»Ҹng lбә§n lЖ°б»Јt vГ o cГЎc б»‘ng nghiб»Үm chб»©a cГЎc chбәҘt riГӘng biб»Үt sau: Na, NaOH, dung dб»Ӣch HCl, dung dб»Ӣch Br2, CaCO3 vГ CH3COOH. Sб»‘ б»‘ng nghiб»Үm cГі xбәЈy ra phбәЈn б»©ng lГ
A. 5. B. 6. C. 4. D. 3.
CГўu 55: Cho cГЎc chбәҘt sau: CH2=CHвҖ“CH=O, , CH3CH=CHCOOH, CH3CH2CHO, CH2=CHвҖ“CH2OH, CH3COCH3, CHвүЎCвҖ“CH=O. Sб»‘ chбәҘt khi phбәЈn б»©ng vб»ӣi H2 dЖ°, xГәc tГЎc Ni, Д‘un nГіng tбәЎo ra cГ№ng mб»ҷt sбәЈn phбә©m lГ
A. 5. B. 2. C. 4. D. 3.
CГўu 56: Cho dГЈy cГЎc chбәҘt sau: Etyl axetat, GlucozЖЎ, SaccarozЖЎ, Ala-Gly-Glu, Ala-Gly, anbumin. Sб»‘ chбәҘt trong dГЈy cГі phбәЈn б»©ng vб»ӣi Cu(OH)2 lГ
A. 2. B. 4. C. 5. D. 3.
CГўu 57: Trong phГІng thГӯ nghiб»Үm, bб»ҷ dб»Ҙng cб»Ҙ vбәҪ dЖ°б»ӣi Д‘Гўy cГі thб»ғ dГ№ng Д‘iб»Ғu chбәҝ bao nhiГӘu khГӯ trong sб»‘ cГЎc khГӯ sau: Cl2, NH3, SO2, CO2, H2, C2H4 (cГЎc Д‘iб»Ғu kiб»Үn phбәЈn б»©ng cГі đủ)?
.jpg?enablejsapi=1)
A. 3. B. 4. C. 2. D. 5.
CГўu 58: Cho 500ml dung dб»Ӣch NaOH 1M tГЎc dб»Ҙng vб»ӣi 200ml dung dб»Ӣch H3PO4 1M. Muб»‘i nГ o sau Д‘Гўy thu Д‘Ж°б»Јc sau phбәЈn б»©ng?
A. Na3PO4 vГ Na2HPO4.
B. Chб»ү cГі NaH2PO4.
C. Na2HPO4 vГ NaH2PO4.
D. Chб»ү cГі Na2HPO4.
CГўu 59: Cho 7,5 gam glyxin phбәЈn б»©ng hбәҝt vб»ӣi dung dб»Ӣch NaOH dЖ°. Sau phбәЈn б»©ng, khб»‘i lЖ°б»Јng muб»‘i thu Д‘Ж°б»Јc lГ
A. 9,8 gam. B. 9,7 gam. C. 7,9 gam. D. 9,9 gam.
CГўu 60: CГҙng thб»©c nГ o sau Д‘Гўy lГ của chбәҘt bГ©o?
A. (C17H31COO)3C3H5.
B. (CH3COO)3C3H5.
C. (HCOO)3C3H5.
D. CH3COOC2H5.
CГўu 61: Cho 4,48 lГӯt NH3 (Д‘ktc) Д‘i qua б»‘ng sб»© Д‘б»ұng 48 gam CuO nung nГіng, thu Д‘Ж°б»Јc chбәҘt rбәҜn X vГ giбәЈi phГіng khГӯ Y. Дҗб»ғ tГЎc dб»Ҙng vб»«a đủ vб»ӣi chбәҘt rбәҜn X cбә§n mб»ҷt thб»ғ tГӯch dung dб»Ӣch HCl 2M lГ
A. 600 ml. B. 1200 ml. C. 300 ml. D. 900 ml.
CГўu 62: Cho cГЎc nhбәӯn xГ©t sau:
1. XenlulozЖЎ cГі cбәҘu trГәc khГҙng nhГЎnh vГ khГҙng xoбәҜn.
2. Дҗб»ҷ ngб»Қt: fructozЖЎ > saccaarozЖЎ > glucozЖЎ.
3. Tinh bб»ҷt do nhiб»Ғu gб»‘c ОІ-glucozЖЎ tбәЎo nГӘn.
4. SaccarozЖЎ Д‘Ж°б»Јc cбәҘu tбәЎo tб»« mб»ҷt gб»‘c a-glucozЖЎ vГ mб»ҷt gб»‘c b-fructozЖЎ.
5. Dung dб»Ӣch glucozЖЎ, saccarozЖЎ, fructozЖЎ Д‘б»Ғu hoГ tan Д‘Ж°б»Јc Cu(OH)2 tбәЎo dung dб»Ӣch xanh lam.
6. Дҗб»ғ nhбәӯn biбәҝt dung dб»Ӣch glucozЖЎ vГ saccarozЖЎ cГі thб»ғ dГ№ng phбәЈn б»©ng trГЎng gЖ°ЖЎng.
Sб»‘ nhбәӯn xГ©t Д‘Гәng lГ
A. 5. B. 6. C. 4. D. 3.
CГўu 63: Hб»Јp chбәҘt hб»Ҝu cЖЎ X cГі cГҙng thб»©c phГўn tб»ӯ C5H6O3. Cho X tГЎc dб»Ҙng vб»ӣi dung dб»Ӣch NaOH thu Д‘Ж°б»Јc 2 chбәҘt hб»Ҝu cЖЎ Y vГ Z, trong Д‘Гі chбәҘt Z (chб»©a C, H, O) cГі mбәЎch phГўn nhГЎnh. Khi cho 1 mol Z phбәЈn б»©ng hoГ n toГ n vб»ӣi lЖ°б»Јng dЖ° dung dб»Ӣch AgNO3 trong NH3Вӯ thu Д‘Ж°б»Јc 4 mol Ag. Nhбәӯn xГ©t nГ o sau vб»Ғ X vГ Y lГ Д‘Гәng?
A. X tГЎc dб»Ҙng Д‘Ж°б»Јc vб»ӣi Na tбәЎo thГ nh H2.
B. 1 mol X phбәЈn б»©ng tб»‘i Д‘a vб»ӣi 4 mol AgNO3 trong dung dб»Ӣch NH3.
C. Y phбәЈn б»©ng vб»ӣi NaOH (cГі mбә·t CaO, to) thu Д‘Ж°б»Јc hidrocacbon.
D. X lГ hб»Јp chбәҘt Д‘a chб»©c.
CГўu 64: Tiбәҝn hГ nh thГӯ nghiб»Үm vб»ӣi cГЎc chбәҘt X, Y, Z, T. Kбәҝt quбәЈ Д‘Ж°б»Јc ghi б»ҹ bбәЈng sau:
|
Mбә«u |
ThГӯ nghiб»Үm |
Hiб»Үn tЖ°б»Јng |
|
X |
TГЎc dб»Ҙng vб»ӣi Cu(OH)2 trong mГҙi trЖ°б»қng kiб»Ғm. |
CГі mГ u xanh lam. |
|
Дҗun nГіng vб»ӣi dung dб»Ӣch H2SO4 loГЈng. ThГӘm tiбәҝp dung dб»Ӣch AgNO3 trong NH3, Д‘un nГіng. |
TбәЎo kбәҝt tủa Ag. |
|
|
Y |
Дҗun nГіng vб»ӣi dung dб»Ӣch NaOH (loГЈng, dЖ°), Д‘б»ғ nguб»ҷi. ThГӘm tiбәҝp vГ i giб»Қt dung dб»Ӣch CuSO4. |
TбәЎo dung dб»Ӣch mГ u xanh lam. |
|
Z |
TГЎc dб»Ҙng vб»ӣi quб»і tГӯm. |
Quб»і tГӯm chuyб»ғn mГ u xanh. |
|
T |
TГЎc dб»Ҙng vб»ӣi nЖ°б»ӣc Brom. |
CГі kбәҝt tủa trбәҜng. |
CГЎc chбәҘt X, Y, Z, T lбә§n lЖ°б»Јt lГ
A. xenlulozЖЎ, vinyl axetat, natri axetat, glucozЖЎ.
B. saccarozЖЎ, triolein, lysin, anilin.
C. hб»“ tinh bб»ҷt, triolein, metylamin, phenol.
D. saccarozЖЎ, etyl axetat, glyxin, anilin.
CГўu 65: Cho sЖЎ Д‘б»“ phбәЈn б»©ng: axit glutamic вҶ’ X вҶ’ Y. Trong sЖЎ Д‘б»“ trГӘn, mб»—i mЕ©i tГӘn lГ mб»ҷt phЖ°ЖЎng trГ¬nh phбәЈn б»©ng, Y lГ chбәҘt nГ o sau Д‘Гўy?
A. NaOOCCH2CH(NH3Cl)COONa.
B. NaOOCCH2CH2CH(NH2)COONa.
C. NaCOOCCH2CH2CH(NH3Cl)COONa.
D. NaOOCCH2CH(NH2)COONa.
CГўu 66: Hб»—n hб»Јp T gб»“m ba chбәҘt hб»Ҝu cЖЎ X, Y, Z (Д‘б»Ғu cГі khб»‘i lЖ°б»Јng phГўn tб»ӯ lб»ӣn hЖЎn 50 vГ Д‘б»Ғu tбәЎo nГӘn tб»« cГЎc nguyГӘn tб»‘ C, H, O). Дҗб»‘t chГЎy hoГ n toГ n m gam T thu Д‘Ж°б»Јc H2O vГ 4,032 lГӯt (Д‘ktc) khГӯ CO2. Cho m gam T phбәЈn б»©ng vб»ӣi dung dб»Ӣch NaHCO3 dЖ°, thu Д‘Ж°б»Јc 1,568 lГӯt (Д‘ktc) khГӯ CO2. Mбә·t khГЎc, cho m gam T phбәЈn б»©ng hoГ n toГ n vб»ӣi lЖ°б»Јng dЖ° dung dб»Ӣch AgNO3 trong NH3, thu Д‘Ж°б»Јc 23,76 gam Ag. CГі cГЎc kбәҝt luбәӯn sau:
(1) X, Y, Z khГҙng thб»ғ lГ HCHO, HCOOH.
(2) GiГЎ trб»Ӣ m < 6,4.
(3) CГі mб»ҷt chбәҘt trong hб»—n hб»Јp T lГ hб»Јp chбәҘt Д‘a chб»©c.
(4) CГі Гӯt nhбәҘt hai chбәҘt trong hб»—n hб»Јp T phбәЈn б»©ng vб»ӣi NaHCO3.
(5) Chб»ү mб»ҷt chбәҘt trong hб»—n hб»Јp T phбәЈn б»©ng vб»ӣi dung dб»Ӣch AgNO3 trong NH3.
Sб»‘ kбәҝt luбәӯn Д‘Гәng lГ
A. 3. B. 5. C. 4. D. 2.
CГўu 67: Cho 31,15 gam hб»—n hб»Јp bб»ҷt Zn vГ Mg (tб»· lб»Ү mol 1 : 1) tan hбәҝt trong dung dб»Ӣch hб»—n hб»Јp gб»“m NaNO3 vГ NaHSO4 thu Д‘Ж°б»Јc dung dб»Ӣch X chб»ү chб»©a m gam hб»—n hб»Јp cГЎc muб»‘i vГ 4,48 lГӯt (Д‘ktc) hб»—n hб»Јp khГӯ Y gб»“m N2O vГ H2. KhГӯ Y cГі tб»· khб»‘i so vЖЎi H2 bбәұng 11,5. GiГЎ trб»Ӣ của m gбә§n nhбәҘt vб»ӣi giГЎ trб»Ӣ nГ o sau Д‘Гўy?
A. 240. B. 242. C. 241. D. 239.
CГўu 68: Khi cho tб»« tб»« Д‘бәҝn hбәҝt 200 ml dung dб»Ӣch gб»“m Na2CO3 1M vГ KHCO3 0,5M vГ o 375 ml dung dб»Ӣch HCl 1M. Дҗбәҝn khi phбәЈn б»©ng hoГ n toГ n thu Д‘Ж°б»Јc V lГӯt (Д‘ktc) khГӯ CO2. GiГЎ trб»Ӣ của V lГ
A. 5,6. B. 5,32. C. 3,92. D. 5,04.
CГўu 69: HГІa tan hoГ n toГ n x mol Fe vГ o dung dб»Ӣch chб»©a y mol FeCl3 vГ z mol HCl, thu Д‘Ж°б»Јc dung dб»Ӣch chб»ү chб»©a mб»ҷt chбәҘt tan duy nhбәҘt. Biб»ғu thб»©c liГӘn hб»Ү giб»Ҝa x, y vГ z lГ
A. 2x = y + 2z. B. y = 2x. C. 2x = y + z. D. x = y вҖ“ 2z.
CГўu 70: Cho hб»—n hб»Јp gб»“m Fe vГ Zn vГ o dung dб»Ӣch chб»©a AgNO3 Д‘бәҝn khi cГЎc phбәЈn б»©ng xбәЈy ra hoГ n toГ n, thu Д‘Ж°б»Јc dung dб»Ӣch X gб»“m ba muб»‘i vГ chбәҘt rбәҜn Y chб»ү chб»©a mб»ҷt kim loбәЎi. Biбәҝt dung dб»Ӣch X cГі khбәЈ nДғng tГЎc dб»Ҙng Д‘Ж°б»Јc vб»ӣi HCl tбәЎo kбәҝt tủa trбәҜng. Ba muб»‘i trong X lГ
A. Fe(NO3)2, Zn(NO3)2 vГ AgNO3.
B. Fe(NO3)3, Fe(NO3)2 vГ Zn(NO3)2.
C. Fe(NO3)3, Fe(NO3)2 vГ AgNO3.
D. Fe(NO3)3, Zn(NO3)2 vГ AgNO3.
CГўu 71: Thủy phГўn hбәҝt m gam hб»—n hб»Јp X gб»“m mб»ҷt sб»‘ este Д‘Ж°б»Јc tбәЎo bб»ҹi axit Д‘ЖЎn chб»©c vГ ancol Д‘ЖЎn chб»©c bбәұng mб»ҷt lЖ°б»Јng dung dб»Ӣch NaOH vб»«a đủ rб»“i cГҙ cбәЎn dung dб»Ӣch sau phбәЈn б»©ng, thu Д‘Ж°б»Јc a gam muб»‘i vГ b gam hб»—n hб»Јp ancol. Дҗб»‘t chГЎy a gam hб»—n hб»Јp muб»‘i thu Д‘Ж°б»Јc hб»—n hб»Јp khГӯ Y vГ 7,42 gam Na2CO3. Cho toГ n bб»ҷ hб»—n hб»Јp khГӯ Y sinh ra qua bГ¬nh Д‘б»ұng dung dб»Ӣch Ca(OH)2 dЖ° thu Д‘Ж°б»Јc 23 gam kбәҝt tủa, Д‘б»“ng thб»қi thбәҘy khб»‘i lЖ°б»Јng bГ¬nh tДғng 13,18 gam so vб»ӣi ban Д‘бә§u. Дҗun b gam hб»—n hб»Јp ancol sinh ra vб»ӣi H2SO4 Д‘бә·c б»ҹ 140oC, thu Д‘Ж°б»Јc 4,34 gam hб»—n hб»Јp cГЎc ete. GiбәЈ thiбәҝt cГЎc phбәЈn б»©ng xбәЈy ra hoГ n toГ n. GiГЎ trб»Ӣ m gбә§n giГЎ trб»Ӣ nГ o nhбәҘt sau Д‘Гўy?
A. 10. B. 12. C. 11. D. 13.
CГўu 72: Дҗб»ғ phГўn biб»Үt H2 vГ CO ngЖ°б»қi ta dГ№ng thГӯ nghiб»Үm nГ o sau Д‘Гўy?
A. Дҗб»‘t khГӯ trong б»‘ng nghiб»Үm rб»“i dбә«n sбәЈn phбә©m chГЎy qua nuб»ӣc vГҙi trong.
B. Dбә«n tб»«ng khГӯ qua CuO Д‘un nГіng.
C. DГ№ng quб»і tГӯm бә©m Д‘б»ғ thб»ӯ.
D. Dбә«n qua nЖ°б»ӣc vГҙi trong.
CГўu 73: Thủy phГўn hoГ n toГ n m gam chбәҘt bГ©o X bбәұng 750 ml dung dб»Ӣch KOH 0,5M, Д‘un nГіng (lЖ°б»Јng KOH Д‘Ж°б»Јc lбәҘy dЖ° 25% so vб»ӣi lЖ°б»Јng cбә§n phбәЈn б»©ng). CГҙ cбәЎn dung dб»Ӣch sau phбәЈn б»©ng thu Д‘Ж°б»Јc 100,2 gam hб»—n hб»Јp chбәҘt rбәҜn khan gб»“m hai chбәҘt. TГӘn gб»Қi của X lГ
A. tristearin.
B. trilinolein.
C. triolein.
D. tripanmitin.
CГўu 74: Cho cГЎc chбәҘt hб»Ҝu cЖЎ mбәЎch hб»ҹ: X lГ axit khГҙng no, cГі hai liГӘn kбәҝt ПҖ trong phГўn tб»ӯ, Y lГ axit no Д‘ЖЎn chб»©c, Z lГ ancol no hai chб»©c, T lГ este của X, Y vб»ӣi Z. Дҗб»‘t chГЎy hoГ n toГ n a gam hб»—n hб»Јp M gб»“m X vГ T, thu Д‘Ж°б»Јc 0,1 mol CO2 vГ 0,07 mol H2O. Cho 6,9 gam M phбәЈn б»©ng vб»«a đủ vб»ӣi dung dб»Ӣch NaOH, cГҙ cбәЎn dung dб»Ӣch sau phбәЈn б»©ng thu Д‘Ж°б»Јc hб»—n hб»Јp muб»‘i khan E. Дҗб»‘t chГЎy hoГ n toГ n E, thu Д‘Ж°б»Јc Na2CO3; 0,195 mol CO2 vГ 0,135 mol H2O. Tб»•ng sб»‘ nguyГӘn tб»ӯ cГі trong phГўn tб»ӯ chбәҘt T lГ
A. 23. B. 21. C. 19. D. 25.
CГўu 75: Khi cho tб»« tб»« dung dб»Ӣch NaOH vГ o dung dб»Ӣch X chб»©a HCl vГ Al2(SO4)3, kбәҝt quбәЈ Д‘б»“ thб»Ӣ nhЖ° sau:
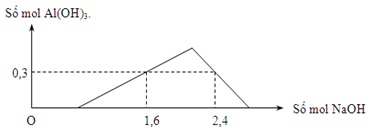
Nбәҝu rГіt vГ o dung dб»Ӣch X б»ҹ trГӘn 500 ml dung dб»Ӣch Ba(OH)2 2M. Khб»‘i lЖ°б»Јng kбәҝt tủa thu Д‘Ж°б»Јc lГ
A. 229,35 gam.
B. 215,6 gam.
C. 208,55 gam.
D. 226,75 gam.
CГўu 76: Thб»ұc hiб»Үn phбәЈn б»©ng nhiб»Үt nhГҙm hб»—n hб»Јp Al vГ Fe2O3 (trong Д‘iб»Ғu kiб»Үn khГҙng cГі khГҙng khГӯ), thu Д‘Ж°б»Јc 36,15 gam hб»—n hб»Јp X. Nghiб»Ғn nhб»Ҹ, trб»ҷn Д‘б»Ғu vГ chia X thГ nh hai phбә§n. Cho phбә§n mб»ҷt tГЎc dб»Ҙng vб»ӣi dung dб»Ӣch NaOH dЖ°, thu Д‘Ж°б»Јc 1,68 lГӯt (Д‘ktc) khГӯ H2 vГ 5,6 gam chбәҘt rбәҜn khГҙng tan. HГІa tan hбәҝt phбә§n hai trong 850 ml dung dб»Ӣch HNO3 2M, thu Д‘Ж°б»Јc 3,36 lГӯt (Д‘ktc) khГӯ NO vГ dung dб»Ӣch chб»ү chб»©a m gam hб»—n hб»Јp muб»‘i. Biбәҝt cГЎc phбәЈn б»©ng xбәЈy ra hoГ n toГ n. GiГЎ trб»Ӣ của m gбә§n nhбәҘt vб»ӣi giГЎ trб»Ӣ nГ o sau Д‘Гўy?
A. 103. B. 95. C. 110. D. 113.
CГўu 77: Hб»—n hб»Јp X gб»“m Cu2O, FeO, M (kim loбәЎi M cГі hГіa trб»Ӣ khГҙng Д‘б»•i), trong X sб»‘ mol của oxi (nguyГӘn tб»ӯ) gбәҘp 2 lбә§n sб»‘ mol M (nguyГӘn tб»ӯ). HГІa tan hбәҝt 48 gam X trong dung dб»Ӣch HNO3 loГЈng dЖ°, thбәҘy cГі 2,1 mol HNO3 phбәЈn б»©ng, sau phбәЈn б»©ng thu Д‘Ж°б»Јc 157,2 gam hб»—n hб»Јp muб»‘i vГ 4,48 lГӯt (Д‘ktc) khГӯ NO duy nhбәҘt. Phбә§n trДғm khб»‘i lЖ°б»Јng của M lГ
A. 20,00%. B. 15,00%. C. 10,00%. D. 11,25%.
CГўu 78: Дҗiб»Үn phГўn (Д‘iб»Үn cб»ұc trЖЎ, hiб»Үu suбәҘt 100%) 300 ml dung dб»Ӣch CuSO4 0,5M vб»ӣi cЖ°б»қng Д‘б»ҷ dГІng Д‘iб»Үn khГҙng Д‘б»•i 2,68A, trong thб»қi gian t giб»қ thu Д‘Ж°б»Јc dung dб»Ӣch X. Cho dung dб»Ӣch Ba(OH)2 dЖ° vГ o X thбәҘy xuбәҘt hiб»Үn 45,73 gam kбәҝt tủa. GiГЎ trб»Ӣ của t lГ
A. 0,4. B. 0,12. C. 0,10. D. 0,8.
CГўu 79: Thủy phГўn hoГ n toГ n m gam hб»—n hб»Јp E gб»“m hai peptit mбәЎch hб»ҹ X vГ Y bбәұng dung dб»Ӣch NaOH thu Д‘Ж°б»Јc 9,02 gam hб»—n hб»Јp cГЎc muб»‘i natri của Gly, Ala, Val. Mбә·t khГЎc, nбәҝu Д‘б»‘t chГЎy hoГ n toГ n m gam E thГ¬ cбә§n 7,056 lГӯt (Д‘ktc) khГӯ O2, thu Д‘Ж°б»Јc 4,32 gam H2O. GiГЎ trб»Ӣ của m lГ
A. 6,36 gam. B. 5,36 gam. C. 8,24 gam. D. 6,42 gam.
CГўu 80: Khi cho 7,75 gam hб»—n hб»Јp X gб»“m 2 amin Д‘ЖЎn chб»©c tГЎc dб»Ҙng hoГ n toГ n vб»ӣi dung dб»Ӣch HCl dЖ° thu Д‘Ж°б»Јc 13,225 gam hб»—n hб»Јp muб»‘i. Nбәҝu Д‘б»‘t chГЎy lЖ°б»Јng X trГӘn bбәұng khГҙng khГӯ vб»«a đủ (xem khГҙng khГӯ gб»“m 20% oxi vГ 80% nitЖЎ vб»Ғ thб»ғ tГӯch) thu Д‘Ж°б»Јc 17,6 gam CO2 vГ V lГӯt (Д‘ktc) khГӯ N2. GiГЎ trб»Ӣ của V lГ
A. 1,68. B. 54,88. C. 5,04. D. 56,56.
ДҗГҒP ГҒN Дҗб»Җ Sб»җ 1
|
41 |
C |
51 |
C |
61 |
C |
71 |
B |
|
42 |
D |
52 |
B |
62 |
A |
72 |
A |
|
43 |
A |
53 |
D |
63 |
B |
73 |
C |
|
44 |
D |
54 |
D |
64 |
B |
74 |
B |
|
45 |
B |
55 |
C |
65 |
B |
75 |
C |
|
46 |
A |
56 |
B |
66 |
A |
76 |
D |
|
47 |
C |
57 |
A |
67 |
A |
77 |
C |
|
48 |
D |
58 |
A |
68 |
D |
78 |
D |
|
49 |
C |
59 |
B |
69 |
C |
79 |
A |
|
50 |
B |
60 |
A |
70 |
D |
80 |
D |
Дҗб»Ғ thi sб»‘ 2
Дҗб»Җ THI THỬ THPT QG MГ”N HГ“A Hб»ҢC TRЖҜб»ңNG THPT CAO THбә®NG- Дҗб»Җ 02
CГўu 1: Kim loбәЎi nГ o sau Д‘Гўy tГЎc dб»Ҙng mбәЎnh vб»ӣi nЖ°б»ӣc б»ҹ nhiб»Үt Д‘б»ҷ thЖ°б»қng?
A. Fe. B. Be. C. K. D. Cu.
CГўu 2: Sб»‘ este cГі cГҙng thЖ°МҒc phГўn tЖ°Мү C4H8O2 khi xГ phГІng hГіa tбәЎo thГ nh ancol cГі sб»‘ nguyГӘn tб»ӯ cacbon lб»ӣn hЖЎn mб»ҷt lГ
A. 2. B. 4. C. 3. D. 1.
CГўu 3: Cho vГ o cб»‘c thủy tinh chб»©a 100 ml dung dб»Ӣch CuSO4 0,1M mб»ҷt mбә©u kim loбәЎi sбәҜt cГі khб»‘i lЖ°б»Јng 5,6 gam. Sau khi phбәЈn б»©ng hoГ n toГ n, khб»‘i lЖ°б»Јng (gam) kim loбәЎi cГі trong cб»‘c lГ
A. 5,68. B. 0,64. C. 6,24. D. 5,52.
CГўu 4: DГЈy cГЎc kim loбәЎi Д‘Ж°б»Јc Д‘iб»Ғu chбәҝ trong cГҙng nghiб»Үp bбәұng phЖ°ЖЎng phГЎp Д‘iб»Үn phГўn nГіng chбәЈy hб»Јp chбәҘt của chГәng lГ
A. Na, Ca, Zn. B. Fe, Ca, Al. C. Na, Ca, Al. D. Na, Cu, Al.
CГўu 5: Oxi hoМҒa hoaМҖn toaМҖn 13 gam kбәҪm cГўМҖn vб»«a đủ V liМҒt khiМҒ clo (Д‘ktc). GiaМҒ triМЈ cuМүa V laМҖ
A. 4,48. B. 1,12. C. 2,24. D. 6,72.
CГўu 6: Cho 12,00 gam glucozЖЎ tГЎc dб»Ҙng vб»ӣi lЖ°б»Јng dЖ° dung dб»Ӣch AgNO3 trong NH3, Д‘un nГіng (hiб»Үu suбәҘt phбәЈn б»©ng trГЎng bбәЎc Д‘бәЎt 75%), khб»‘i lЖ°б»Јng kбәҝt tủa bбәЎc (gam) thu Д‘Ж°б»Јc lГ
A. 10,80. B. 5,40. C. 14,40. D. 7,20.
CГўu 7: Дҗб»ғ hбәЎn chбәҝ khГӯ clo thoГЎt ra gГўy Гҙ nhiб»…m mГҙi trЖ°б»қng khi tiбәҝn hГ nh thГӯ nghiб»Үm Д‘iб»Ғu chбәҝ khГӯ clo, cбә§n Д‘бә·t trГӘn miб»Үng bГ¬nh thu mб»ҷt mбә©u bГҙng tбә©m dung dб»Ӣch nГ o trong sб»‘ cГЎc dung dб»Ӣch sau Д‘Гўy?
A. CaCl2. B. Ca(OH)2. C. H2SO4. D. quб»і tГӯm.
CГўu 8: CГі cГЎc thГӯ nghiб»Үm sau
(1) Cho kim loбәЎi Na vГ o dung dб»Ӣch CuSO4;
(2) Sб»Ҙc CO2 Д‘бәҝn dЖ° vГ o dung dб»Ӣch Ca(OH)2;
(3) Cho tб»« tб»« dung dб»Ӣch NaOH Д‘бәҝn dЖ° vГ o dung dб»Ӣch Al2(SO4)3;
(4) Cho tб»« tб»« dung dб»Ӣch NaOH Д‘бәҝn dЖ° vГ o dung dб»Ӣch FeCl3;
Sau khi kбәҝt thГәc cГЎc phбәЈn б»©ng, sб»‘ thГӯ nghiб»Үm thu Д‘Ж°б»Јc kбәҝt tủa lГ
A. 1. B. 4. C. 3. D. 2.
CГўu 9: PhбәЈn б»©ng nГ o sau Д‘Гўy chб»©ng minh hб»Јp chбәҘt Fe(II) cГі tГӯnh khб»ӯ?
A. 3FeO + 10HNO3 вҶ’ 3Fe(NO3)3 + NO + 5H2O.
B. FeCl2 + 2NaOH вҶ’ Fe(OH)2 + 2NaCl.
C. Fe(OH)2 + 2HCl вҶ’ FeCl2 + 2H2O.
D. FeO + CO вҶ’ Fe + CO2.
CГўu 10: PhГЁn chua Д‘Ж°б»Јc dГ№ng trong ngГ nh cГҙng nghiб»Үp thuб»ҷc da, cГҙng nghiб»Үp giбәҘy, chбәҘt cбә§m mГ u trong ngГ nh nhuб»ҷm vбәЈi, chбәҘt lГ m trong nЖ°б»ӣc. CГҙng thб»©c hoГЎ hб»Қc của phГЁn chua lГ
A. (NH4)2SO4.Al2(SO4)3.24H2O.
B. Na2SO4.Al2(SO4)3.24H2O.
C. Li2SO4.Al2(SO4)3.24H2O.
D. K2SO4.Al2(SO4)3.24H2O.
---(Дҗб»ғ xem tiбәҝp nб»ҷi dung tб»« cГўu 11 Д‘бәҝn cГўu 40 của Д‘б»Ғ thi sб»‘ 2 cГЎc em vui lГІng xem Online hoбә·c ДҗДғng nhбәӯp vГ o HOC247 Д‘б»ғ tбәЈi vб»Ғ mГЎy)---
ДҗГҒP ГҒN Дҗб»Җ Sб»җ 2
|
1 |
C |
11 |
B |
21 |
D |
31 |
C |
|
2 |
C |
12 |
B |
22 |
D |
32 |
D |
|
3 |
A |
13 |
A |
23 |
D |
33 |
B |
|
4 |
C |
14 |
A |
24 |
B |
34 |
C |
|
5 |
A |
15 |
C |
25 |
B |
35 |
C |
|
6 |
A |
16 |
D |
26 |
B |
36 |
C |
|
7 |
B |
17 |
D |
27 |
B |
37 |
A |
|
8 |
D |
18 |
D |
28 |
B |
38 |
A |
|
9 |
A |
19 |
D |
29 |
B |
39 |
A |
|
10 |
D |
20 |
C |
30 |
A |
40 |
C |
Дҗб»Ғ thi sб»‘ 3
Дҗб»Җ THI THỬ THPT QG MГ”N HГ“A Hб»ҢC TRЖҜб»ңNG THPT CAO THбә®NG- Дҗб»Җ 03
CГўu 1: Hб»Јp chбәҘt CH3COOCH2CH3 cГі tГӘn gб»Қi lГ
A. etyl axetat.
B. metyl propionat.
C. propyl axetat.
D. metyl axetat.
CГўu 2: Cho 0,15 mol alanin tГЎc dб»Ҙng hбәҝt vб»ӣi dung dб»Ӣch HCl, thu Д‘Ж°б»Јc m gam muб»‘i. GiГЎ trб»Ӣ của m lГ
A. 18,675. B. 16,575. C. 16,725. D. 18,825.
CГўu 3: Sб»‘ este cГі cГҙng thЖ°МҒc phГўn tЖ°Мү C4H8O2 khi xГ phГІng hГіa tбәЎo thГ nh ancol cГі sб»‘ nguyГӘn tб»ӯ cacbon lб»ӣn hЖЎn mб»ҷt lГ
A. 2. B. 3. C. 4. D. 1.
CГўu 4: PhГЁn chua Д‘Ж°б»Јc dГ№ng trong ngГ nh cГҙng nghiб»Үp thuб»ҷc da, cГҙng nghiб»Үp giбәҘy, chбәҘt cбә§m mГ u trong ngГ nh nhuб»ҷm vбәЈi, chбәҘt lГ m trong nЖ°б»ӣc. CГҙng thб»©c hoГЎ hб»Қc của phГЁn chua lГ
A. K2SO4.Al2(SO4)3.24H2O.
B. (NH4)2SO4.Al2(SO4)3.24H2O.
C. Li2SO4.Al2(SO4)3.24H2O.
D. Na2SO4.Al2(SO4)3.24H2O.
CГўu 5: Cho dГЈy cГЎc chбәҘt sau: vinyl axetat, triolein, fructozЖЎ, saccarozЖЎ, etylamin, alanin. PhГЎt biб»ғu nГ o sau Д‘Гўy sai?
A. CГі 5 chбәҘt phбәЈn б»©ng vб»ӣi dung dб»Ӣch HCl Д‘un nГіng.
B. CГі 2 chбәҘt bб»Ӣ thủy phГўn trong mГҙi trЖ°б»қng kiб»Ғm.
C. CГі 3 chбәҘt phбәЈn б»©ng vб»ӣi H2 (xt Ni, t0).
D. CГі 3 chбәҘt lГ m mбәҘt mГ u nЖ°б»ӣc brom.
CГўu 6: HГІa tan hбәҝt m gam Al bбәұng dung dб»Ӣch NaOH dЖ°, thu Д‘Ж°б»Јc 6,72 lГӯt khГӯ H2(Д‘ktc). GiГЎ trб»Ӣ của m lГ
A. 5,4. B. 8,1. C. 2,7. D. 6,75.
CГўu 7: Oxi hoМҒa hoaМҖn toaМҖn 13 gam kбәҪm cГўМҖn vб»«a đủ V liМҒt khiМҒ clo (Д‘ktc). GiaМҒ triМЈ cuМүa V laМҖ
A. 4,48. B. 1,12. C. 2,24. D. 6,72.
CГўu 8: ThГӯ nghiб»Үm nГ o sau Д‘Гўy khГҙng cГі sб»ұ hГІa tan chбәҘt rбәҜn?
A. Cho CrO3 vГ o H2O.
B. Cho Cr vГ o dung dб»Ӣch H2SO4 Д‘бә·c, nguб»ҷi.
C. Cho Cr(OH)3 vГ o dung dб»Ӣch HCl.
D. Cho Cr vГ o dung dб»Ӣch H2SO4 loГЈng, nГіng.
CГўu 9: Trong cГЎc ion sau: Ag+, Cu2+, Fe2+, Fe3+. Ion cГі tГӯnh oxi hГіa mбәЎnh nhбәҘt lГ
A. Cu2+. B. Fe2+. C. Fe3+. D. Ag+.
CГўu 10: Cho 12,00 gam glucozЖЎ tГЎc dб»Ҙng vб»ӣi lЖ°б»Јng dЖ° dung dб»Ӣch AgNO3 trong NH3, Д‘un nГіng (hiб»Үu suбәҘt phбәЈn б»©ng trГЎng bбәЎc Д‘бәЎt 75%), khб»‘i lЖ°б»Јng kбәҝt tủa bбәЎc (gam) thu Д‘Ж°б»Јc lГ
A. 10,80. B. 5,40. C. 14,40. D. 7,20.
---(Дҗб»ғ xem tiбәҝp nб»ҷi dung tб»« cГўu 11 Д‘бәҝn cГўu 40 của Д‘б»Ғ thi sб»‘ 3 cГЎc em vui lГІng xem Online hoбә·c ДҗДғng nhбәӯp vГ o HOC247 Д‘б»ғ tбәЈi vб»Ғ mГЎy)---
ДҗГҒP ГҒN Дҗб»Җ Sб»җ 3
|
1 |
A |
11 |
B |
21 |
B |
31 |
B |
|
2 |
D |
12 |
A |
22 |
B |
32 |
C |
|
3 |
B |
13 |
B |
23 |
A |
33 |
D |
|
4 |
A |
14 |
A |
24 |
D |
34 |
B |
|
5 |
D |
15 |
D |
25 |
C |
35 |
B |
|
6 |
A |
16 |
D |
26 |
C |
36 |
C |
|
7 |
A |
17 |
D |
27 |
C |
37 |
C |
|
8 |
B |
18 |
D |
28 |
D |
38 |
B |
|
9 |
D |
19 |
C |
29 |
C |
39 |
C |
|
10 |
A |
20 |
A |
30 |
C |
40 |
A |
Дҗб»Ғ thi sб»‘ 4
Дҗб»Җ THI THỬ THPT QG MГ”N HГ“A Hб»ҢC TRЖҜб»ңNG THPT CAO THбә®NG- Дҗб»Җ 04
CГўu 1: PhГЁn chua Д‘Ж°б»Јc dГ№ng trong ngГ nh cГҙng nghiб»Үp thuб»ҷc da, cГҙng nghiб»Үp giбәҘy, chбәҘt cбә§m mГ u trong ngГ nh nhuб»ҷm vбәЈi, chбәҘt lГ m trong nЖ°б»ӣc. CГҙng thб»©c hoГЎ hб»Қc của phГЁn chua lГ
A. K2SO4.Al2(SO4)3.24H2O.
B. (NH4)2SO4.Al2(SO4)3.24H2O.
C. Na2SO4.Al2(SO4)3.24H2O.
D. Li2SO4.Al2(SO4)3.24H2O.
CГўu 2: Hб»Јp chбәҘt CH3COOCH2CH3 cГі tГӘn gб»Қi lГ
A. etyl axetat. B. metyl propionat. C. propyl axetat. D. metyl axetat.
CГўu 3: DГЈy cГЎc kim loбәЎi Д‘Ж°б»Јc Д‘iб»Ғu chбәҝ trong cГҙng nghiб»Үp bбәұng phЖ°ЖЎng phГЎp Д‘iб»Үn phГўn nГіng chбәЈy hб»Јp chбәҘt của chГәng lГ
A. Fe, Ca, Al. B. Na, Ca, Al. C. Na, Cu, Al. D. Na, Ca, Zn.
CГўu 4: Cho dГЈy cГЎc chбәҘt sau: vinyl axetat, triolein, fructozЖЎ, saccarozЖЎ, etylamin, alanin. PhГЎt biб»ғu nГ o sau Д‘Гўy sai?
A. CГі 5 chбәҘt phбәЈn б»©ng vб»ӣi dung dб»Ӣch HCl Д‘un nГіng.
B. CГі 2 chбәҘt bб»Ӣ thủy phГўn trong mГҙi trЖ°б»қng kiб»Ғm.
C. CГі 3 chбәҘt phбәЈn б»©ng vб»ӣi H2 (xt Ni, t0).
D. CГі 3 chбәҘt lГ m mбәҘt mГ u nЖ°б»ӣc brom.
CГўu 5: Cho vГ o cб»‘c thủy tinh chб»©a 100 ml dung dб»Ӣch CuSO4 0,1M mб»ҷt mбә©u kim loбәЎi sбәҜt cГі khб»‘i lЖ°б»Јng 5,6 gam. Sau khi phбәЈn б»©ng hoГ n toГ n, khб»‘i lЖ°б»Јng (gam) kim loбәЎi cГі trong cб»‘c lГ
A. 6,24. B. 0,64. C. 5,68. D. 5,52.
CГўu 6: Trong cГЎc chбәҘt dЖ°б»ӣi Д‘Гўy, chбәҘt nГ o cГі lб»ұc bazЖЎ yбәҝu nhбәҘt?
A. CH3NH2.
B. C6H5NH2 (anilin).
C. NH3.
D. (C6H5)2NH (Д‘iphenyl amin).
CГўu 7: ThГӯ nghiб»Үm nГ o sau Д‘Гўy khГҙng cГі sб»ұ hГІa tan chбәҘt rбәҜn?
A. Cho Cr vГ o dung dб»Ӣch H2SO4 Д‘бә·c, nguб»ҷi.
B. Cho Cr vГ o dung dб»Ӣch H2SO4 loГЈng, nГіng.
C. Cho Cr(OH)3 vГ o dung dб»Ӣch HCl.
D. Cho CrO3 vГ o H2O.
CГўu 8: Trong cГЎc ion sau: Ag+, Cu2+, Fe2+, Fe3+. Ion cГі tГӯnh oxi hГіa mбәЎnh nhбәҘt lГ
A. Cu2+. B. Ag+. C. Fe3+. D. Fe2+.
CГўu 9: ChбәҘt nГ o sau Д‘Гўy lГ amin bбәӯc 1?
A. CH3NHC2H5.
B. (C6H5)2NH.
C. (CH3)2CHNH2.
D. (CH3)3N.
CГўu 10: Cho 12,00 gam glucozЖЎ tГЎc dб»Ҙng vб»ӣi lЖ°б»Јng dЖ° dung dб»Ӣch AgNO3 trong NH3, Д‘un nГіng (hiб»Үu suбәҘt phбәЈn б»©ng trГЎng bбәЎc Д‘бәЎt 75%), khб»‘i lЖ°б»Јng kбәҝt tủa bбәЎc (gam) thu Д‘Ж°б»Јc lГ
A. 14,40. B. 10,80. C. 7,20. D. 5,40.
---(Дҗб»ғ xem tiбәҝp nб»ҷi dung tб»« cГўu 11 Д‘бәҝn cГўu 40 của Д‘б»Ғ thi sб»‘ 4 cГЎc em vui lГІng xem Online hoбә·c ДҗДғng nhбәӯp vГ o HOC247 Д‘б»ғ tбәЈi vб»Ғ mГЎy)---
ДҗГҒP ГҒN Дҗб»Җ Sб»җ 4
|
1 |
A |
11 |
B |
21 |
A |
31 |
A |
|
2 |
A |
12 |
C |
22 |
B |
32 |
C |
|
3 |
B |
13 |
D |
23 |
A |
33 |
B |
|
4 |
D |
14 |
A |
24 |
C |
34 |
C |
|
5 |
C |
15 |
D |
25 |
C |
35 |
A |
|
6 |
D |
16 |
D |
26 |
C |
36 |
B |
|
7 |
A |
17 |
D |
27 |
C |
37 |
D |
|
8 |
B |
18 |
C |
28 |
D |
38 |
C |
|
9 |
A |
19 |
D |
29 |
B |
39 |
B |
|
10 |
B |
20 |
A |
30 |
B |
40 |
D |
Дҗб»Ғ thi sб»‘ 5
Дҗб»Җ THI THỬ THPT QG MГ”N HГ“A Hб»ҢC TRЖҜб»ңNG THPT CAO THбә®NG- Дҗб»Җ 05
CГўu 1: Cho 0,15 mol alanin tГЎc dб»Ҙng hбәҝt vб»ӣi dung dб»Ӣch HCl, thu Д‘Ж°б»Јc m gam muб»‘i. GiГЎ trб»Ӣ của m lГ
A. 18,825. B. 16,575. C. 16,725. D. 18,675.
CГўu 2: Oxi hoМҒa hoaМҖn toaМҖn 13 gam kбәҪm cГўМҖn vб»«a đủ V liМҒt khiМҒ clo (Д‘ktc). GiaМҒ triМЈ cuМүa V laМҖ
A. 4,48. B. 2,24. C. 1,12. D. 6,72.
CГўu 3: Trong cГЎc chбәҘt dЖ°б»ӣi Д‘Гўy, chбәҘt nГ o cГі lб»ұc bazЖЎ yбәҝu nhбәҘt?
A. C6H5NH2 (anilin).
B. (C6H5)2NH (Д‘iphenyl amin).
C. NH3.
D. CH3NH2.
CГўu 4: NЖ°б»ӣc cб»©ng lГ nЖ°б»ӣc cГі chб»©a nhiб»Ғu ion
A. Na+, K+. B. ClвҖ‘, HCO3-. C. Be2+, Ba2+. D. Mg2+, Ca2+.
CГўu 5: CГі cГЎc thГӯ nghiб»Үm sau
(1) Cho kim loбәЎi Na vГ o dung dб»Ӣch CuSO4;
(2) Sб»Ҙc CO2 Д‘бәҝn dЖ° vГ o dung dб»Ӣch Ca(OH)2;
(3) Cho tб»« tб»« dung dб»Ӣch NaOH Д‘бәҝn dЖ° vГ o dung dб»Ӣch Al2(SO4)3;
(4) Cho tб»« tб»« dung dб»Ӣch NaOH Д‘бәҝn dЖ° vГ o dung dб»Ӣch FeCl3;
Sau khi kбәҝt thГәc cГЎc phбәЈn б»©ng, sб»‘ thГӯ nghiб»Үm thu Д‘Ж°б»Јc kбәҝt tủa lГ
A. 4. B. 1. C. 2. D. 3.
CГўu 6: ThГӯ nghiб»Үm nГ o sau Д‘Гўy khГҙng cГі sб»ұ hГІa tan chбәҘt rбәҜn?
A. Cho Cr vГ o dung dб»Ӣch H2SO4 Д‘бә·c, nguб»ҷi.
B. Cho Cr vГ o dung dб»Ӣch H2SO4 loГЈng, nГіng.
C. Cho Cr(OH)3 vГ o dung dб»Ӣch HCl.
D. Cho CrO3 vГ o H2O.
CГўu 7: Sб»‘ este cГі cГҙng thЖ°МҒc phГўn tЖ°Мү C4H8O2 khi xГ phГІng hГіa tбәЎo thГ nh ancol cГі sб»‘ nguyГӘn tб»ӯ cacbon lб»ӣn hЖЎn mб»ҷt lГ
A. 1. B. 4. C. 3. D. 2.
CГўu 8: ChбәҘt nГ o sau Д‘Гўy lГ amin bбәӯc 1?
A. CH3NHC2H5.
B. (C6H5)2NH.
C. (CH3)2CHNH2.
D. (CH3)3N.
CГўu 9: Cho dГЈy cГЎc chбәҘt sau: vinyl axetat, triolein, fructozЖЎ, saccarozЖЎ, etylamin, alanin. PhГЎt biб»ғu nГ o sau Д‘Гўy sai?
A. CГі 5 chбәҘt phбәЈn б»©ng vб»ӣi dung dб»Ӣch HCl Д‘un nГіng.
B. CГі 3 chбәҘt lГ m mбәҘt mГ u nЖ°б»ӣc brom.
C. CГі 2 chбәҘt bб»Ӣ thủy phГўn trong mГҙi trЖ°б»қng kiб»Ғm.
D. CГі 3 chбәҘt phбәЈn б»©ng vб»ӣi H2 (xt Ni, t0).
CГўu 10: DГЈy cГЎc kim loбәЎi Д‘Ж°б»Јc Д‘iб»Ғu chбәҝ trong cГҙng nghiб»Үp bбәұng phЖ°ЖЎng phГЎp Д‘iб»Үn phГўn nГіng chбәЈy hб»Јp chбәҘt của chГәng lГ
A. Fe, Ca, Al.
B. Na, Ca, Zn.
C. Na, Cu, Al.
D. Na, Ca, Al.
---(Дҗб»ғ xem tiбәҝp nб»ҷi dung tб»« cГўu 11 Д‘бәҝn cГўu 40 của Д‘б»Ғ thi sб»‘ 5 cГЎc em vui lГІng xem Online hoбә·c ДҗДғng nhбәӯp vГ o HOC247 Д‘б»ғ tбәЈi vб»Ғ mГЎy)---
ДҗГҒP ГҒN Дҗб»Җ Sб»җ 5
|
1 |
A |
11 |
A |
21 |
B |
31 |
A |
|
2 |
A |
12 |
B |
22 |
B |
32 |
C |
|
3 |
B |
13 |
A |
23 |
D |
33 |
D |
|
4 |
D |
14 |
D |
24 |
A |
34 |
B |
|
5 |
C |
15 |
C |
25 |
C |
35 |
C |
|
6 |
A |
16 |
C |
26 |
C |
36 |
B |
|
7 |
C |
17 |
D |
27 |
B |
37 |
C |
|
8 |
A |
18 |
D |
28 |
D |
38 |
C |
|
9 |
B |
19 |
B |
29 |
B |
39 |
D |
|
10 |
D |
20 |
A |
30 |
A |
40 |
D |
TrГӘn Д‘Гўy lГ mб»ҷt phбә§n trГӯch dбә«n nб»ҷi dung Bб»ҷ 5 Д‘б»Ғ thi thб»ӯ THPT QG mГҙn HГіa hб»Қc nДғm 2021-2022 cГі Д‘ГЎp ГЎn TrЖ°б»қng THPT Cao ThбәҜng. Дҗб»ғ xem toГ n bб»ҷ nб»ҷi dung cГЎc em Д‘Дғng nhбәӯp vГ o trang hoc247.net Д‘б»ғ tбәЈi tГ i liб»Үu vб»Ғ mГЎy tГӯnh.
Hy vб»Қng tГ i liб»Үu nГ y sбәҪ giГәp cГЎc em hб»Қc sinh Гҙn tбәӯp tб»‘t vГ Д‘бәЎt thГ nh tГӯch cao trong hб»Қc tбәӯp.
NgoГ i ra cГЎc em cГі thб»ғ tham khбәЈo thГӘm mб»ҷt sб»‘ tЖ° liб»Үu cГ№ng chuyГӘn mб»Ҙc tбәЎi Д‘Гўy:
- Bб»ҷ 5 Д‘б»Ғ thi thб»ӯ THPT QG mГҙn HГіa hб»Қc nДғm 2021-2022 cГі Д‘ГЎp ГЎn TrЖ°б»қng THPT LГҪ Tб»ұ Trб»Қng
- Bб»ҷ 5 Д‘б»Ғ thi thб»ӯ THPT QG mГҙn HГіa hб»Қc nДғm 2021-2022 cГі Д‘ГЎp ГЎn TrЖ°б»қng THPT HГ Huy Tбәӯp
ChГәc cГЎc em hб»Қc tб»‘t!
TГ i liб»Үu liГӘn quan
TЖ° liб»Үu nб»•i bбәӯt tuбә§n
-
Дҗб»Ғ thi minh hб»Қa mГҙn ToГЎn tб»‘t nghiб»Үp THPT nДғm 2025
22/10/20241489 - Xem thГӘm




