Giải bài 5.15 trang 17 SBT Khoa học tự nhiên 7 Cánh Diều
Hạt nhân nguyên tử X có 3 proton, tổng số electron có trong nguyên tử Y là 9.
a) Nguyên tử X có tạo ra được liên kết với nguyên tử Y không?
b) Nếu X và Y liên kết được với nhau thì liên kết đó là liên kết ion hay liên kết cộng hoá trị? Viết sơ đồ minh hoạ sự tạo thành liên kết giữa X và Y.
Hướng dẫn giải chi tiết Bài 5.15
Phương pháp giải
Liên kết ion được hình thành giữa các nguyên tử kim loại và nguyên tử phi kim, nguyên tử kim loại nhường electron, trở thành ion dương, nguyên tử phi kim nhận electron từ kim loại, trở thành ion âm. Các ion trái dấu hút nhau tạo thành liên kết trong hợp chất ion.
Lời giải chi tiết:
a)
Nguyên tử X có tạo ra được liên kết với nguyên tử Y. Vì:
− Nguyên tử X ở ô thứ ba (X có 3 proton) ð X là nguyên tố kim loại Li.
− Nguyên tử Y (Y có 9 electron) ở ô thứ 9 ð Y là nguyên tố phi kim F.
→ X và Y không phải là khí hiếm, do đó X và Y có thể tạo liên kết với nhau.
b)
Liên kết giữa kim loại Li và phi kim F là liên kết ion.
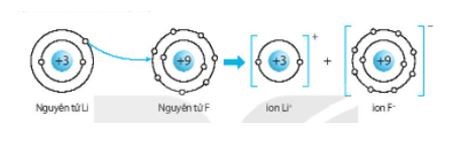
− Nguyên tử kim loại Li có 1 electron lớp ngoài cùng, để đạt được 2 electron lớp ngoài cùng giống khí hiếm He gần nó thì nguyên tử Li nhường nguyên tử F 1 electron.
− Nguyên tử F có 7 electron lớp ngoài cùng, cần nhận thêm 1 electron để đạt được 8 electron lớp ngoài cùng giống Neon.
→ 1 nguyên tử Li liên kết ion với 1 nguyên tử F.
-- Mod Khoa học tự nhiên 7 HỌC247
Bài tập SGK khác
Chưa có câu hỏi nào. Em hãy trở thành người đầu tiên đặt câu hỏi.




