Hướng dẫn giải bài tập SGK chương trình Hóa học 8 Bài 17 Bài luyện tập 3 giúp các em học sinh rèn luyện kĩ năng phân biệt được hiện tượng hóa học và hiện tượng vật lí; Lập phương trình hóa học khi biết các chất phản ứng và sản phẩm.
-
Bài tập 1 trang 60 SGK Hóa học 8
Hình dưới đây là sơ đồ tương trựng cho phản ứng: Giữa khí N2 và khí H2 tạo ra ammoniac NH3.
Hãy cho biết:
a) Tên các chất tham gia và sản phẩm?
b) Liên kết giữa các nguyên tử thay đổi như thế nào? Phân tử nào biến đổi, phân tử nào được tạo ra?
c) Số nguyên tử mỗi nguyên tố trước và sau phản ứng bằng bao nhiêu có giữ nguyên không?
-
Bài tập 2 trang 61 SGK Hóa học 8
Khẳng định sau gồm hai ý: "Trong phản ứng hóa học chỉ phân tử biến đổi còn các nguyên tử giữ nguyên, nên tổng khối lượng các chất phản ứng được bảo toàn"
Hãy chọn phương án trả lời đúng trong số các phương án cho sau:
A. Ý 1 đúng, ý 2 sai.
B. Ý 1 sai ý 2 đúng.
C. Cả hai ý đều đúng nhưng ý 1 không giải thích ý 2.
D. Cả hai ý đều đúng và ý 1 giải thích ý 2.
E. Cả hai ý đều sai.
-
Bài tập 3 trang 61 SGK Hóa học 8
Canxi cacbonat là thành phần chính của đá vôi. Khi nung đá vôi xảy ra phản ứng hóa học sau:
Canxi cacbonat → Canxi oxit + cacbon đioxit.
Biết rằng khi nung 280kg đá vôi tạo ra 140kg canxi oxit CaO (vôi sống) và 110kg khí cacbon đioxit CO2.
a) Viết công thức về khối lượng của các chất trong phản ứng.
b) Tính tỉ lệ phần trăm về khối lượng canxi cacbonat chứa trong đá vôi.
-
Bài tập 4 trang 61 SGK Hóa học 8
Biết rằng khí etilen C2H4 cháy là xảy ra phản ứng với khí O2 sinh ra khí cacbon đioxit CO2 và nước.
a) Lập phương trình hóa học phản ứng xảy ra?
b) Cho biết tỉ lệ giữa số phân tử etilen lần lượt với số phân tử oxi và số phân tử cacbon đioxit.
- VIDEOYOMEDIA
-
Bài tập 5 trang 61 SGK Hóa học 8
Cho sơ đồ của phản ứng như sau:
Al + CuSO4 → Alx(SO4)y + Cu
a) Xác định các chỉ số x và y.
b) Lập phương trình hóa học và cho biết tỉ lệ số nguyên tử của cặp đơn chất kim loại số phân tử của cặp hợp chất.
-
Bài tập 17.1 trang 23 SBT Hóa học 8
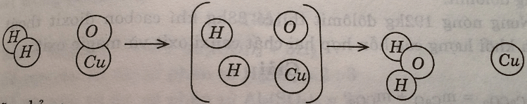
Hình dưới đây là sơ đồ tượng trưng cho phản ứng giữa khí hidro H2 và chất đồng (II) oxit CuO tạo ra kim loại đồng và nước:
Hãy chỉ ra:
a) Mỗi phản ứng xảy ra với bao nhiêu phân tử của mỗi chất phản ứng, tạo ra bao nhiêu phân tử nước và nguyên tử đồng?
b) Liên kết giữa những nguyên tử trong phân tử nào bị tách rời, trong phân tử nào được tạo ra?
-
Bài tập 17.2 trang 23 SBT Hóa học 8
Trong một phản ứng hóa học, chất phản ứng và sản phẩm phải chứa cùng:
A. Số nguyên tử trong mỗi chất
B. Số nguyên tố tạo ra chất
C. Số nguyên tử của mỗi nguyên tố
D. Số phân tử của mỗi chất
Khẳng định nào là đúng (A,B, C hay D)?
-
Bài tập 17.3 trang 23 SBT Hóa học 8
Dây tóc trong bóng đèn nóng đỏ và phát sáng mỗi khi có dòng điện đi qua. Trường hợp bóng đèn bị nứt và không khí (có khí oxi) chui vào bên trong thì dây tóc bị cháy khi bật công tắc điện. (Xem lại bài tập 2.2 về dây tóc trong dây điện).
Hãy phân tích và chỉ ra khi nào xảy ra hiện tượng vật lí, khi nào xảy ra hiện tượng hóa học.
-
Bài tập 17.4 trang 23 SBT Hóa học 8
Đá đôlomit là hỗn hợp hai chất canxi cacbonat CaCO3 và magie cacbonat MgCO3. Khi nung nóng, tương tự canxi cacbonat, từ chất magie cacbonat cũng tạo ra chất magie oxit MgO và khí cacbon đioxit.
a) Viết công thức về khối lượng của hai phản ứng xảy ra khi nung nóng đôlômit.
b) Nung nóng 192kg đôlômit thì có 88kg khí cacbon đioxit thoát ra. Tính khối lượng của hỗn hợp hai chất canxi oxit và magie oxit
-
Bài tập 17.5 trang 23 SBT Hóa học 8
Cho sơ đồ của các phản ứng sau:
a) K + O2 → K2O
b) Al + CuCl2 → AlCl3 + Cu
c) NaOH + Fe2(SO4)3 → Fe(OH)3 + Na2SO4
Lập phương trình hóa học của mỗi phản ứng và cho biết tỉ lệ só nguyên tử, số phân tử của hai cặp chất trong phản ứng ( tùy chọn).
-
Bài tập 17.6 trang 24 SBT Hóa học 8
Biết rằng khí axetilen (khí đất đèn) C2H2 cháy là xảy ra phản ứng với khí oxi O2, sinh ra khí cacbon đioxit CO2 và nước.
a) Lập phương trình hóa học của phản ứng.
b) Cho biết tỉ lệ giữa số phân tử axetilen lần lượt với số phân tử khí cacbon đioxit và số phân tử nước.
-
Bài tập 17.7 trang 24 SBT Hóa học 8
Biết rằng kim loại nhôm tác dụng với axit sunfuric H2SO4 tạo ra khi hidro H2 và chất nhôm sunfat Al2(SO4)3
a) Lập phương trình hóa học của phản ứng.
b) Cho biết tỉ lệ giữa sô nguyên tử Al lần lượt với số phân tử của ba chất trong phản ứng.
-
Bài tập 17.8 trang 24 SBT Hóa học 8
Hãy chọn hệ số và công thức hóa học thích hợp điền vào những chỗ có dấu hỏi trong các phương trình hóa học sau (chép vào vở bài tập).
a) CO2 + Ca(OH)2 → CaCO3 + ?
b) ? + ?AgNO3 → Al(NO3)3 + 3Ag
c) ?HCl + CaCO3 → CaCl2 + H2O + ?
-
Bài tập 17.9 trang 24 SBT Hóa học 8
Cho sơ đồ phản ứng sau: Fe(OH)y + H2SO4 → Fex(SO4)y + H2O
a) Hãy biện luận để thay x, y (biết rằng x ≠ y) bằng các chỉ số thích hợp rồi lập phương trình hóa học của phản ứng.
b) Cho biết tỉ lệ só phân tử của bốn cặp chất trong phản ứng (tùy chọn).
-
Bài tập 17.10 trang 24 SBT Hóa học 8
a) Biết rằng khí hidro dễ tác dụng vơi chất chì (IV) oxit PbO2, chiếm lấy oxi của chất này để tạo ra nước.
Viết phương trình hóa học của phản ứng và tên chất mới sinh ra.
b) Biết rằng 3g khí hidro tác dụng vừa đủ với 179,25g PbO2, tạo ra 27g nước. Tính khối lượng chất mới sinh ra.
-
Bài tập 17.11 trang 24 SBT Hóa học 8
Quặng malachite có thành phần chính là hai hợp chất của đồng được ghi bằng công thức chung là Cu2(OH)2CO3 . Khi nung nóng thì hợp chất này bị phân hủy, sản phẩm của phản ứng phân hủy gồm có CuO, H2O và CO2.
a) Viết phương trình hóa học của phản ứng phân hủy của mỗi hợp chất của đồng.
b) Biết rằng khi nung nóng 4,8kg quặng thì thu được 3,2kg CuO cùng 0,36kg H2O và 0,88kg CO2. Tính tỉ lệ phần trăm về khối lượng hai hợp chất của đồng có chứa trong quặng.
-
Bài tập 17.12 trang 25 SBT Hóa học 8
Để điều chế kali clorua KCl (dùng làm phân bón), người ta cho kim loại kali K tác dụng với khí clo Cl2.
a) Viết phương trình hóa học của phản ứng.
b) Nếu có 6,02.1023 nguyên tử K, cần lấy vào phản ứng bao nhiêu phân tử Cl2 và thu được bao nhiêu phân tử KCl?
(Xem lại các bài tập 8.9*,9.6*,16.8* trước khi làm bài tập này và bài tập tiếp theo).
-
Bài tập 17.13 trang 25 SBT Hóa học 8
Những câu trong bài tập này coi là tiếp theo của bài tập 17.12*.
a) Tính khối lượng bằng gam của:
- 6,02.1023 nguyên tử K,
- 6,02.1023 nguyên tử Cl2,
- 6,02.1023 phân tử KCl
b) Tính khối lượng khí clo để tác dụng vừa đủ với 39g kim loại kali.
c) Từ khối lượng kim loại cho biết và khối lượng khí clo tính được trong câu b), tính khối lượng kali clorua thu được theo hai cách.