Nß╗Öi dung b├ái hß╗ìc tr├¼nh b├áy c├íc phã░ãíng ph├íp ─æ├ú ─æã░ß╗úc kiß╗âm chß╗®ng bß║▒ng thß╗▒c nghiß╗çm ─æß╗â ß╗®ng dß╗Ñng v├áo viß╗çc Nhß║¡n biß║┐t mß╗Öt sß╗æ ion trong dung dß╗ïch bao gß╗ôm Cation (Na+, NH4+, Ba2+, Al3+, Fe2+, Fe3+, Cu2+) v├á Anion (NO3-, SO42-,Cl-,CO32-)
Tóm tắt lÛ thuyết
2.1. Nguyên tắc nhận biết ion trong dung dịch
Dung dß╗ïch chß╗®a ion + Thuß╗æc thß╗¡:
- Chất kết tủa
- Sß║ún phß║®m c├│ m├áu
- Chất khí khó tan sủi bọt
- Chất khí bay khỏi dung dịch
2.2. Nhận biết một số Cation trong dung dịch
a. Bảng nhận biết
| Cation | Thuß╗æc thß╗¡ | Hiß╗çn tã░ß╗úng | Giß║úi th├¡ch |
| Na+ |
Thử màu ngọn lửa |
Ngß╗ìn lß╗¡a c├│ m├áu v├áng tã░ãíi |
Ion Na+ hß║ºu nhã░ kh├┤ng kß║┐t tß╗ºa vß╗øi c├íc anion kh├íc |
| NH4+ |
Dung dịch kiềm |
Tạo khí NH3 có mùi khai |
\({\rm{NH}}_{\rm{4}}^{\rm{ + }}{\rm{ + O}}{{\rm{H}}^{\rm{ - }}} \to {\rm{N}}{{\rm{H}}_{\rm{3}}} \uparrow {\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}}\) |
| Ba2+ |
Dung dß╗ïch H2SO4 dã░ |
Kết tủa màu trắng | \({\rm{B}}{{\rm{a}}^{{\rm{2 + }}}}{\rm{ + SO}}_{\rm{4}}^{{\rm{2 - }}} \to {\rm{BaS}}{{\rm{O}}_{\rm{4}}} \downarrow\) |
| Al3+ |
Dd kiß╗üm hoß║Àc NH3 |
Kß║┐t tß╗ºa keo trß║»ng tan trong OH- dã░ |
\({\rm{A}}{{\rm{l}}^{{\rm{3 + }}}}{\rm{ + 3O}}{{\rm{H}}^{\rm{ - }}} \to {\rm{Al(OH}}{{\rm{)}}_{\rm{3}}} \downarrow\) \({\rm{Al(OH}}{{\rm{)}}_{\rm{3}}}{\rm{ + O}}{{\rm{H}}^{\rm{ - }}} \to {\rm{AlO}}_{\rm{2}}^{\rm{ - }}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}}\) |
| Fe3+ |
Dung dịch kiềm |
Kết tủa nâu đỏ |
\({\rm{F}}{{\rm{e}}^{{\rm{3 + }}}}{\rm{ + 3O}}{{\rm{H}}^{\rm{ - }}} \to {\rm{Fe(OH}}{{\rm{)}}_{\rm{3}}} \downarrow\) |
| Fe2+ |
Dung dịch kiềm |
Kß║┐t tß╗ºa trß║»ng xanhÔåÆ─æß╗Å n├óu |
\({\rm{F}}{{\rm{e}}^{{\rm{2 + }}}}{\rm{ + 2O}}{{\rm{H}}^{\rm{ - }}} \to {\rm{Fe(OH}}{{\rm{)}}_2} \downarrow\) \({\rm{4Fe(OH}}{{\rm{)}}_{\rm{2}}}{\rm{ + }}{{\rm{O}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{4Fe(OH}}{{\rm{)}}_{\rm{3}}} \downarrow\) |
| Cu2+ |
Dung dịch kiềm |
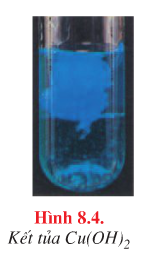
Kết tủa xanh |
\({\rm{C}}{{\rm{u}}^{{\rm{2 + }}}}{\rm{ + 2O}}{{\rm{H}}^{\rm{ - }}} \to {\rm{Cu(OH}}{{\rm{)}}_{\rm{2}}} \downarrow\) |
b. Màu sắc của một số kết tủa
2.3. Nhận biết một số Anion trong dung dịch
a. Bảng nhận biết
| Anion | Thuß╗æc thß╗¡ | Hiß╗çn tã░ß╗úng | Giß║úi th├¡ch |
|
NO3- |
Cu / H+ |
Dd có màu xanh, khí thoát ra hóa nâu trong không khí. |
\({\rm{3Cu + 2NO}}_{\rm{3}}^{\rm{ - }}{\rm{ + 8}}{{\rm{H}}^{\rm{ + }}} \to{\rm{3C}}{{\rm{u}}^{{\rm{2 + }}}}{\rm{ + 2NO}} \uparrow {\rm{ + 4}}{{\rm{H}}_{\rm{2}}}{\rm{O}}\) \({\rm{2NO + }}{{\rm{O}}_{\rm{2}}} \to {\rm{2N}}{{\rm{O}}_{\rm{2}}}\) nâu đỏ |
| SO42- |
Dd Ba2+/ H+ dã░ |
Kết tủa trắng |
\({\rm{B}}{{\rm{a}}^{{\rm{2 + }}}}{\rm{ + SO}}_{\rm{4}}^{{\rm{2 - }}} \to {\rm{BaS}}{{\rm{O}}_{\rm{4}}} \downarrow\) |
| Cl- | Dung dịch AgNO3 |
Kết tủa trắng |
\({\rm{A}}{{\rm{g}}^{\rm{ + }}}{\rm{ + C}}{{\rm{l}}^ - } \to {\rm{AgCl}} \downarrow\) |
| CO32- |
Dd axit mạnh/ Ca(OH)2 |
Kết tủa trắng |
\({\rm{CO}}_{\rm{3}}^{{\rm{2 - }}}{\rm{ + 2}}{{\rm{H}}^{\rm{ + }}} \to {\rm{C}}{{\rm{O}}_{\rm{2}}} \uparrow {\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}}\) \({\rm{C}}{{\rm{O}}_{\rm{2}}}{\rm{ + Ca(OH}}{{\rm{)}}_{\rm{2}}} \to {\rm{CaC}}{{\rm{O}}_{\rm{3}}} \downarrow {\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}}\) |
Bài tập minh họa
3.1. B├ái tß║¡p Nhß║¡n biß║┐t mß╗Öt sß╗æ ion trong dung dß╗ïch - Cãí bß║ún
Bài 1:
C├│ c├íc dung dß╗ïch kh├┤ng m├áu ─æß╗▒ng trong c├íc lß╗ì ri├¬ng biß╗çt, kh├┤ng d├ín nh├ún: ZnSO4, Cu(NO3)2, Al(NO3)3. ─Éß╗â ph├ón biß╗çt c├íc dung dß╗ïch tr├¬n c├│ thß╗â d├╣ng thuß╗æc thß╗¡ n├áo? N├¬u c├íc hiß╗çn tã░ß╗úng diß╗àn ra.
Hã░ß╗øng dß║½n:
Dùng dd Ba(OH)2 vì:
- ZnSO4 tạo kết tủa màu trắng.
\({\rm{Ba(OH}}{{\rm{)}}_{\rm{2}}}{\rm{ + ZnS}}{{\rm{O}}_{\rm{4}}} \to {\rm{BaS}}{{\rm{O}}_{\rm{4}}} \downarrow {\rm{ + Zn(OH}}{{\rm{)}}_{\rm{2}}}\)
- Cu(NO3)2 tạo kết tủa màu xanh.
\({\rm{Cu(N}}{{\rm{O}}_{\rm{3}}}{{\rm{)}}_{\rm{2}}}{\rm{ + Ba(OH}}{{\rm{)}}_{\rm{2}}} \to {\rm{Cu(OH}}{{\rm{)}}_{\rm{2}}} \downarrow {\rm{ + Ba(N}}{{\rm{O}}_{\rm{3}}}{{\rm{)}}_{\rm{2}}}\)
- Al(NO3)3 tạo kết tủa keo.
\({\rm{Al(N}}{{\rm{O}}_{\rm{3}}}{{\rm{)}}_{\rm{3}}}{\rm{ + Ba(OH}}{{\rm{)}}_{\rm{2}}} \to {\rm{Al(OH}}{{\rm{)}}_{\rm{3}}} \downarrow {\rm{ + Ba(N}}{{\rm{O}}_{\rm{3}}}{{\rm{)}}_{\rm{2}}}\)
Bài 2:
Tr├¼nh b├áy c├ích nhß║¡n biß║┐t c├íc dung dß╗ïch trong suß╗æt, trong lß╗ì mß║Ñt nh├ún sau: HCl,HNO3, H2SO4 bß║▒ng phã░ãíng ph├íp h├│a hß╗ìc?
Hã░ß╗øng dß║½n:
Tr├¡ch mß╗ùi chß║Ñt mß╗Öt ├¡t cho v├áo 3 ß╗æng nghiß╗çm kh├íc nhau v├á ─æ├ính sß╗æ thß╗® tß╗▒ (1), (2), (3).
Lấy dung dịch BaCl2 cho vào 3 ống nghiệm, ống nào cho kết tủa trắng là H2SO4:
\({\rm{BaC}}{{\rm{l}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{S}}{{\rm{O}}_{\rm{4}}} \to {\rm{BaS}}{{\rm{O}}_{\rm{4}}} \downarrow {\rm{ + 2HCl}}\)
Lß║Ñy dung dß╗ïch AgNO3 cho v├áo hai ß╗æng c├▓n lß║íi, ß╗æng n├áo cho kß║┐t tß╗ºa trß║»ng sau h├│a ─æen ngo├ái kh├┤ng kh├¡ l├á chß╗®a axit HCl.
\({\rm{AgN}}{{\rm{O}}_{\rm{3}}}{\rm{ + HCl}} \to {\rm{AgCl}} \downarrow {\rm{ + HN}}{{\rm{O}}_{\rm{3}}}\)
Dung dịch còn lại là HNO3.
Bài 3:
D├╣ng dung dß╗ïch Ba(OH)2 ─æß╗â ph├ón biß╗çt 6 dung dß╗ïch NaNO3, Fe(NO3)3, Al(NO3)3, Mg(NO3)2, NH4NO3, (NH4)2SO4 sau th├¼ hiß╗çn tã░ß╗úng diß╗àn ra l├á g├¼?
Hã░ß╗øng dß║½n:
- Fe(NO3)3 tạo kết tủa màu nâu đỏ.
- Al(NO3)3 tạo kết tủa keo.
- Mg(NO3)2 tạo kết tủa trắng.
- NH4NO3 tạo khí mùi khai.
- (NH4)2SO4 tß║ío kß║┐t tß╗ºa m├áu trß║»ng ─æß╗ông thß╗Øi c├│ kh├¡ m├╣i khai tho├ít ra.
3.2. Bài tập Nhận biết một số ion trong dung dịch - Nâng cao
Bài 1:
C├│ 5 dung dß╗ïch mß║Ñt nh├ún : Na2S, BaCl2, AlCl3, MgCl2, Na2CO3. Nß║┐u kh├┤ng d├╣ng th├¬m thuß╗æc thß╗¡ th├¼ c├│ thß╗â nhß║¡n biß║┐t ─æã░ß╗úc tß╗æi ─æa sß╗æ dung dß╗ïch l├á
Hã░ß╗øng dß║½n:
Cho tß╗½ng cß║Àp chß║Ñt trong b├¼nh phß║ún ß╗®ng tß╗½ng ─æ├┤i mß╗Öt, ta c├│ bß║úng sau:
|
|
Na2S |
BaCl2 |
AlCl3 |
MgCl2 |
Na2CO3 |
|
Na2S |
- |
- |
Ôåô keo trß║»ng Ôåæ m├╣i trß╗®ng thß╗æi |
Ôåô trß║»ng Ôåæ m├╣i trß╗®ng thß╗æi |
- |
|
BaCl2 |
- |
- |
- |
- |
Ôåô trß║»ng |
|
AlCl3 |
Ôåô keo trß║»ng Ôåæ m├╣i trß╗®ng thß╗æi |
- |
- |
- |
Ôåô keo trß║»ng Ôåæ kh├┤ng m├╣i |
|
MgCl2 |
Ôåô trß║»ng Ôåæ m├╣i trß╗®ng thß╗æi |
- |
- |
- |
Ôåô trß║»ng |
|
NaCO3 |
- |
|
Ôåô keo trß║»ng Ôåæ kh├┤ng m├╣i |
Ôåô trß║»ng |
- |
Vậy có thể nhận biết cả 5 chất trong 5 lọ mất nhãn.
4. Luyện tập Bài 40 Hóa học 12
4.1. Trắc nghiệm
B├ái kiß╗âm tra Trß║»c nghiß╗çm Ho├í hß╗ìc 12 B├ái 40 c├│ phã░ãíng ph├íp v├á lß╗Øi giß║úi chi tiß║┐t gi├║p c├íc em luyß╗çn tß║¡p v├á hiß╗âu b├ái.
-
- A. HCl
- B. Qùy tím
- C. NaOH
- D. BaCl2
-
- A. 1.
- B. 4.
- C. 2.
- D. 3.
-
- A. BaCl2
- B. NaHSO4.
- C. Ba(OH)2.
- D. NaOH.
-
- A. giß║Ñy quß╗│ t├¡m, dung dß╗ïch bazãí.
- B. muối tan Ba2+, Cu kim loại.
- C. Ba(OH)2 và dung dịch muối tan của Ag+
- D. dd phenolphtalein, giấy quỳ tím.
-
- A. Dung dịch KOH.
- B. Dung dịch Na2CO3.
- C. Dung dịch AgNO3.
- D. Dung dịch H2SO4.
-
- A. Dùng muối bari.
- B. Dùng quỳ tím và muối bari.
- C. Dùng dung dịch Ba(OH)2.
- D. Dùng dung dịch AgNO3 và quỳ tím.
-
- A. phã░ãíng ph├íp ─æß╗æt n├│ng thß╗¡ m├áu ngß╗ìn lß╗¡a.
- B. phã░ãíng ph├íp nhiß╗çt ph├ón ─æß╗â tß║ío kß║┐t tß╗ºa.
- C. thuß╗æc thß╗¡ ─æß╗â tß║ío vß╗øi ion mß╗Öt sß║ún phß║®m kß║┐t tß╗ºa, bay hãíi hoß║Àc c├│ sß╗▒ thay ─æß╗òi m├áu.
- D. phã░ãíng ph├íp th├¡ch hß╗úp ─æß╗â tß║ío ra sß╗▒ biß║┐n ─æß╗òi vß╗ü trß║íng th├íi, m├áu sß║»c tß╗½ c├íc ion trong dung dß╗ïch.
C├óu 8-20: Mß╗Øi c├íc em ─æ─âng nhß║¡p xem tiß║┐p nß╗Öi dung v├á thi thß╗¡ Online ─æß╗â cß╗ºng cß╗æ kiß║┐n thß╗®c vß╗ü b├ái hß╗ìc n├áy nh├®!
4.2. Bài tập SGK và Nâng cao
C├íc em c├│ thß╗â hß╗ç thß╗æng lß║íi nß╗Öi dung b├ái hß╗ìc th├┤ng qua phß║ºn hã░ß╗øng dß║½n Giß║úi b├ái tß║¡p Ho├í hß╗ìc 12 B├ái 40.
Bài tập 1 trang 174 SGK Hóa học 12
Bài tập 2 trang 174 SGK Hóa học 122
Bài tập 3 trang 174 SGK Hóa học 122
Bài tập 4 trang 174 SGK Hóa học 12
Bài tập 5 trang 174 SGK Hóa học 12
Bài tập 6 trang 174 SGK Hóa học 12
Bài tập 1 trang 233 SGK Hóa 12 Nâng cao
Bài tập 2 trang 233 SGK Hóa 12 Nâng cao
Bài tập 3 trang 233 SGK Hóa 12 Nâng cao
Bài tập 4 trang 223 SGK Hóa 12 Nâng cao
Bài tập 5 trang 233 SGK Hóa 12 Nâng cao
Bài tập 1 trang 236 SGK Hóa 12 Nâng cao
Bài tập 2 trang 236 SGK Hóa 12 Nâng cao
Bài tập 3 trang 236 SGK Hóa 12 Nâng cao
Bài tập 40.1 trang 95 SBT Hóa học 12
Bài tập 4 trang 236 SGK Hóa 12 Nâng cao
Bài tập 40.2 trang 95 SBT Hóa học 12
Bài tập 40.3 trang 95 SBT Hóa học 12
Bài tập 40.4 trang 95 SBT Hóa học 12
Bài tập 40.5 trang 95 SBT Hóa học 12
Bài tập 40.6 trang 95 SBT Hóa học 12
Bài tập 40.7 trang 95 SBT Hóa học 12
5. Hß╗Åi ─æ├íp vß╗ü B├ái 40 Chã░ãíng 8 Ho├í hß╗ìc 12
Trong qu├í tr├¼nh hß╗ìc tß║¡p nß║┐u c├│ bß║Ñt k├¼ thß║»c mß║»c g├¼, c├íc em h├úy ─æß╗â lß║íi lß╗Øi nhß║»n ß╗ƒ mß╗Ñc Hß╗Åi ─æ├íp ─æß╗â c├╣ng cß╗Öng ─æß╗ông H├│a HOC247 thß║úo luß║¡n v├á trß║ú lß╗Øi nh├®.




.PNG)
.PNG)
.PNG)