Nội dung bài giảng Luyện tập Dẫn xuất halogen, ancol, phenol củng cố kiến thức ,hệ thống hóa tính chất hóa học và phương pháp điều chế ancol, phenol. Giúp học sinh hiểu Mối liên quan giữa cấu trúc phân tử và tính chất hóa học đặc trưng của ancol, phenol. Phân biệt tính chất hóa học của ancol và phenol.
Tóm tắt lý thuyết
1.1. Dẫn xuất halogen
- Có công thức: CxHyX
- Tính chất hóa học:
- Có phản ứng thế X hoặc -OH: CxHyX → CxHyOH
- Có khả năng tách HX hoặc H2O: CnH2n+1X → CnH2n + HX
- Điều chế:
- Thế H của hidrocacbon bằng X
- Cộng HX hoặc X2 vào anken, ankin, ...
1.2. Ancol - Phenol
|
|
ANCOL |
PHENOL |
|
1. Công thức |
CnH2n+1OH (no, đơn chức) |
C6H5OH |
|
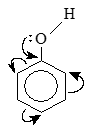
2. Cấu trúc |
|
|
|
3. Tính chất hóa học |
||
|
a. Thế nhóm OH |
\(\begin{array}{l} |
C6H5OH + HX → không xảy ra |
|
b. Thế H của nhóm OH |
\(RO - H + Na \to RO - Na + \frac{1}{2}{H_2}\) |
2C6H5OH + Na → 2C6H5ONa + H2 C6H5OH + NaOH → C6H5ONa + H2O |
|
c. Tách nước |
|
Không có |
|
d. Thế ở vòng benzen |
Không có |
C6H5OH + 3Br2 → (C6H2OH)Br3 i+ HBr C6H5OH +3HO-NO2 →C6H2OH(NO2)3 + 3H2O |
|
e. Phản ứng oxi hóa không hoàn toàn |
R-CH2-OH + CuO R-CHOH-R’+CuO Ancol bậc 3 không phản ứng |
Không có |
|
4.Điều chế |
- Cộng nước vào anken C2H4 + H2O - Thế X của dẫn xuất halogen C2H5Cl + KOH -Điều chế etanol từ glucozo C6H12O6 |
-Thế H của benzene sau đó thủy phân dẫn xuất halogen bằng NaOH đặc, p cao, t0 cao - Oxi hóa cumen C6H6 |
|
5. Ứng dụng |
- Nguyên liệu sản xuất andehit .axit .este. chất dẻo dung môi … |
- Thuốc nổ ,dược phẩm , sản xuất chất dẻo ……. |
Bài tập minh họa
Bài 1:
X mạch hở có CTPT C6H10 tác dụng với HBr cho 3 sản phẩm monobrom là đồng phân cấu tạo của nhau. Số đồng phân cấu tạo thỏa mãn X là:
Hướng dẫn:
3 hợp chất thỏa mãn là:
\(\\ 1. \ C=C=C-C-C\)
\(\\ \begin{matrix} 2. \\ \ \\ \ \end{matrix} \begin{matrix} \ C=C=C-C-C \ \ \ \ \ \ \ \ \ \ \ \ \ \ \\ ^| \\ C \end{matrix}\)
\(3. \ C-C=C=C-C-C\)
Bài 2:
Cho hỗn hợp X gồm C2H6, C2H4, C2H2. Lấy 11,4 gam X tác dụng hết với dung dịch brom dư thì khối lượng brom phản ứng là 48 gam. Mặt khác, nếu cho 13,44 lít (đktc) hỗn hợp khí X tác dụng với lượng dư dung dịch AgNO3 trong dd NH3, thu được 36 gam kết tủa. Thành phần phần trăm theo thể tích của C2H6 trong hỗn hợp X là:
Hướng dẫn:
Trong 11,4g X có a mol C2H6; b mol C2H4; c mol C2H2
⇒ mX = 30a + 28b + 26c = 11,4g(1)
Và \(n_{Br_{2}}\) = b + 2c = 0,3 mol (2)
Nếu trong 13,44 lit X có lượng chất gấp t lần 11,4g thì:
t(a + b + c) = 0,6 mol(3)
Lại có: \(n_{C_{2}H_{2}} = n_{Ag_{2}C_{2}}\) = 0,15 mol = t.c (4)
Từ (1, 2, 3, 4) ⇒ a = 0,2; b = 0,1; c = 0,1
\(\Rightarrow \%V_{C_{2}H_{6(X)}} = 50 \ \%\)
Bài 3:
Xét sáu nhận định sau:
(1) Phản ứng monobrom hóa propan (bằng Br2, đun nóng) tạo sản phẩm chính là n-propyl bromua.
(2) Phản ứng của isobutilen với hidro clorua tạo sản phẩm chính là t-butyl clorua.
(3) Phản ứng dehidrat hóa 2-metylpentan-3-ol tạo sản phẩm chính là 4-metylpent-2-en.
(4) Phản ứng của buta-1,3-đien với brom có thể tạo cả 3,4-đibrombut-1-en và 1,4-đibrombut-2-en.
(5) Điclo hóa benzen bằng Cl2 (xúc tác bột Fe, đun nóng) ưu tiên tạo sản phẩm là o-điclobenzen và p- điclobenzen.
(6) Monoclo hóa toluen bằng Cl2 (chiếu sáng) ưu tiên tạo sản phẩm là o-clotoluen và p-clotoluen.
Số nhận định đúng trong số sáu nhận định này bằng?
Hướng dẫn:
(1) Phản ứng monobrom hóa propan (bằng Br2, đun nóng) tạo sản phẩm chính là n-propyl bromua.
⇒ Sai. Sản phẩm chính là iso- propyl bromua.
(2) Phản ứng của isobutilen với hidro clorua tạo sản phẩm chính là t-butyl clorua.
⇒ Đúng.
(3) Phản ứng dehidrat hóa 2-metylpentan-3-ol tạo sản phẩm chính là 4-metylpent-2-en.
⇒ Sai. Sản phẩm chính là 2-metylpent-2-en.
(4) Phản ứng của buta-1,3-đien với brom có thể tạo cả 3,4-đibrombut-1-en và 1,4-đibrombut-2-en.
⇒ Đúng.
(5) Điclo hóa benzen bằng Cl2 (xúc tác bột Fe, đun nóng) ưu tiên tạo sản phẩm là o-điclobenzen và p- điclobenzen.
⇒ Đúng.
(6) Monoclo hóa toluen bằng Cl2 (chiếu sáng) ưu tiên tạo sản phẩm là o-clotoluen và p-clotoluen.
⇒ Sai. Đây là phản ứng thế Clo vào nhóm -CH3.
Bài 4:
Cho 23,4 gam hỗn hợp X gồm hai ancol đơn chức kế tiếp nhau trong dãy đồng đẳng tác dụng hết với 13,8 gam Na thu được 36,75 gam chất rắn. Nếu cho 20,8 gam X tách nước tạo ete (với hiệu suất 100%) thì khối lượng ete thu được là:
Hướng dẫn:
Ancol + Na → C.rắn + H2
Bảo toàn khối lượng ⇒ \(m_{H_{{2}}} = 23,4 + 13,8 - 36,75 = 0,45 \ gam\)
Do ancol đơn chức
\(\\ \Rightarrow n_{H_{{2}}} = \frac{1}{2}n_{{ancol}} = \frac{0,45}{2} \ mol \\ \Rightarrow n_{ancol}= 0,45 \ mol\)
\(\\ \Rightarrow \overline{M}_{{ancol}} = 23,4 : 0,45 = 52\)
Vì 2 ancol đơn chức kế tiếp nhau trong dãy đồng đẳng ⇒ chúng là C2H5OH và C3H7OH
\(\\ \Rightarrow n_{C_{2}H_{5}OH} = 3 : 35 \ (mol); \ n_{C_{3}H_{7}OH} = 27 : 140 \ (mol)\)
⇒ Trong 20,8 gam hỗn hợp:
\(\\ \left\{\begin{matrix} n_{C_{2}H_{5}OH} = \dfrac{9}{35}.\dfrac{20,8}{23,4} = \dfrac{8}{35} \ (mol) \\ n_{C_{3}H_{7}OH} = \dfrac{6}{35} \ (mol) \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \end{matrix}\right. \\ m_{ete} = m_{ ancol} - \frac{1}{2} n_{ ancol}. 18 = 20,8 - \frac{1}{2}( \frac{8}{35}+ \frac{6}{35} ) = 17,2 \ gam\)
3. Luyện tập Bài 42 Hóa học 11
Sau bài học cần nắm:
- Củng cố kiến thức ,hệ thống hóa tính chất hóa học và phương pháp điều chế ancol, phenol.
- Mối liên quan giữa cấu trúc phân tử và tính chất hóa học đặc trưng của ancol, phenol.
- Phân biệt tính chất hóa học của ancol và phenol.
3.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 11 Bài 42 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
- A. CH2Cl-CH2-CHCl2.
- B. CH3-CH2-CCl3.
- C. CH2Cl-CCl2-CH3.
- D. CH2Cl-CHCl-CH2Cl.
-
- A. ClCH2COOCH2CH3.
- B. CH3COOCH2CH2Cl.
- C. CH3COOCH(Cl)CH3.
- D. HCOOCH(Cl)CH2CH3.
-
- A. (c), (d), (f)
- B. (a), (b), (c)
- C. (a), (c), (d)
- D. (c), (d), (e)
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
3.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 11 Bài 42.
Bài tập 1 trang 195 SGK Hóa học 11
Bài tập 2 trang 195 SGK Hóa học 11
Bài tập 3 trang 195 SGK Hóa học 11
Bài tập 4 trang 195 SGK Hóa học 11
Bài tập 5 trang 195 SGK Hóa học 11
Bài tập 6 trang 195 SGK Hóa học 11
Bài tập 7 trang 195 SGK Hóa học 11
Bài tập 42.1 trang 66 SBT Hóa học 11
Bài tập 42.2 trang 66 SBT Hóa học 11
Bài tập 42.3 trang 66 SBT Hóa học 11
Bài tập 42.4 trang 67 SBT Hóa học 11
Bài tập 42.5 trang 67 SBT Hóa học 11
Bài tập 42.6 trang 67 SBT Hóa học 11
Bài tập 42.7 trang 67 SBT Hóa học 11
Bài tập 42.8 trang 67 SBT Hóa học 11
Bài tập 42.9 trang 67 SBT Hóa học 11
Bài tập 42.10 trang 68 SBT Hóa học 11
Bài tập 42.11 trang 68 SBT Hóa học 11
Bài tập 42.12 trang 68 SBT Hóa học 11
Bài tập 1 trang 235 SGK Hóa học 11 nâng cao
Bài tập 2 trang 235 SGK Hóa học 11 nâng cao
Bài tập 3 trang 235 SGK Hóa học 11 nâng cao
Bài tập 4 trang 235 SGK Hóa học 11 nâng cao
Bài tập 5 trang 235 SGK Hóa học 11 nâng cao
Bài tập 6 trang 235 SGK Hóa học 11 nâng cao
Bài tập 7 trang 235 SGK Hóa học 11 nâng cao
4. Hỏi đáp về Bài 42 Chương 8 Hóa học 11
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.





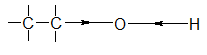
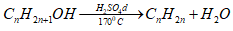
.PNG) R-CH=O +Cu + H2O
R-CH=O +Cu + H2O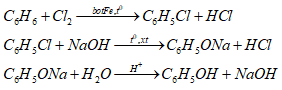
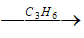 C6H5CH(CH3)2
C6H5CH(CH3)2 .PNG) C6H5OH
C6H5OH.PNG)




