Náŧi dung chi tiášŋt và hÆ°áŧng dášŦn giášĢi bà i tášp Bà i 10: HáŧĢp chášĨt háŧŊu cÆĄ và hoÃĄ háŧc háŧŊu cÆĄ mÃīn HÃģa háŧc 11 Kášŋt Náŧi Tri TháŧĐc ÄÆ°áŧĢc HOC247 biÊn soᚥn dÆ°áŧi ÄÃĒy sáš― giÚp cÃĄc em dáŧ dà ng nášŊm ÄÆ°áŧĢc kiášŋn tháŧĐc quan tráŧng váŧ háŧĢp chášĨt háŧŊu cÆĄ, bao gáŧm cÃĄc khÃĄi niáŧm, phÃĒn loᚥi và máŧt sáŧ nhÃģm cháŧĐc trong háŧĢp chášĨt háŧŊu cÆĄ.
HÃĢy cÃđng khÃĄm phÃĄ bà i háŧc nà y Äáŧ hiáŧu rÃĩ hÆĄn váŧ sáŧą liÊn háŧ mášt thiášŋt cáŧ§a hoÃĄ háŧc háŧŊu cÆĄ Äášŋn Äáŧi sáŧng cáŧ§a con ngÆ°áŧi và cÃĄc sinh vášt trÊn TrÃĄi ÄášĨt nhÃĐ. ChÚc cÃĄc em háŧc táŧt.
TÃģm tášŊt lÃ― thuyášŋt
1.1. HáŧĢp chášĨt háŧŊu cÆĄ và hoÃĄ háŧc háŧŊu cÆĄ
a. KhÃĄi niáŧm
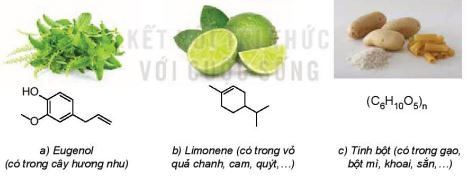
HÃŽnh 10.1. Máŧt sáŧ háŧĢp chášĨt háŧŊu cÆĄ trong táŧą nhiÊn
|
HáŧĢp chášĨt háŧŊu cÆĄ là háŧĢp chášĨt cáŧ§a carbon (tráŧŦ máŧt sáŧ cÃĄc háŧĢp chášĨt vÃī cÆĄ nhÆ° carbon monoxide, carbon dioxide, muáŧi carbonate, cyanide, carbide,...). |
- CÃĄc háŧĢp chášĨt cáŧ§a carbon váŧi cÃĄc nguyÊn táŧ khÃĄc trong bášĢng tuᚧn hoà n ÄÃĢ tᚥo nÊn hà ng cháŧĨc triáŧu háŧĢp chášĨt háŧŊu cÆĄ. Sáŧ lÆ°áŧĢng cÃĄc chášĨt háŧŊu cÆĄ máŧi vášŦn Äang tiášŋp táŧĨc tÄng lÊn.
- HoÃĄ háŧc háŧŊu cÆĄ là ngà nh hoÃĄ háŧc chuyÊn nghiÊn cáŧĐu cÃĄc háŧĢp chášĨt háŧŊu cÆĄ.
b. Äáš·c Äiáŧm chung cáŧ§a cÃĄc háŧĢp chášĨt háŧŊu cÆĄ
|
Thà nh phᚧn phÃĒn táŧ nhášĨt thiášŋt phášĢi cháŧĐa nguyÊn táŧ carbon, thÆ°áŧng cÃģ hydrogen, oxygen, nitrogen, halogen, sulfur, phosphorus,... |
- LiÊn kášŋt hoÃĄ háŧc cháŧ§ yášŋu là liÊn kášŋt cáŧng hoÃĄ tráŧ. CÃĄc nguyÊn táŧ carbon khÃīng nháŧŊng cÃģ khášĢ nÄng liÊn kášŋt váŧi nguyÊn táŧ cáŧ§a cÃĄc nguyÊn táŧ khÃĄc mà cÃēn cÃģ tháŧ liÊn kášŋt váŧi nhau tᚥo thà nh mᚥch carbon.
- Nhiáŧt Äáŧ nÃģng chášĢy thášĨp, nhiáŧt Äáŧ sÃīi thášĨp (dáŧ bay hÆĄi) và thÆ°áŧng khÃīng tan hoáš·c Ãt tan trong nÆ°áŧc, tan trong cÃĄc dung mÃīi háŧŊu cÆĄ.
- Dáŧ chÃĄy, kÃĐm báŧn váŧi nhiáŧt nÊn dáŧ báŧ nhiáŧt phÃĒn huáŧ·.
- PhášĢn áŧĐng cáŧ§a cÃĄc háŧĢp chášĨt háŧŊu cÆĄ thÆ°áŧng xášĢy ra chášm, theo nhiáŧu hÆ°áŧng và tᚥo ra háŧn háŧĢp cÃĄc sášĢn phášĐm. Äáŧ tÄng táŧc Äáŧ phášĢn áŧĐng thÆ°áŧng cᚧn Äun nÃģng và cÃģ xÚc tÃĄc.
1.2. PhÃĒn loᚥi háŧĢp chášĨt háŧŊu cÆĄ
- Dáŧąa và o thà nh phᚧn nguyÊn táŧ, háŧĢp chášĨt háŧŊu cÆĄ cÃģ tháŧ phÃĒn thà nh hai loᚥi:
|
Hydrocarbon và dášŦn xuášĨt cáŧ§a hydrocarbon. |
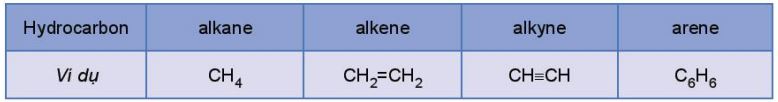
- Hydrocarbon là nháŧŊng háŧĢp chášĨt ÄÆ°áŧĢc tᚥo thà nh cháŧ táŧŦ hai nguyÊn táŧ carbon và hydrogen. Máŧt sáŧ hydrocarbon tiÊu biáŧu:
- Khi máŧt hay nhiáŧu nguyÊn táŧ hydrogen trong phÃĒn táŧ hydrocarbon ÄÆ°áŧĢc thay thášŋ bášąng máŧt hay nhiáŧu nguyÊn táŧ hay nhÃģm nguyÊn táŧ khÃĄc (thÆ°áŧng cháŧĐa oxygen, nitrogen, sulfur, halogen,...), thu ÄÆ°áŧĢc dášŦn xuášĨt cáŧ§a hydrocarbon. DášŦn xuášĨt cáŧ§a hydrocarbon ÄÆ°áŧĢc phÃĒn thà nh nhiáŧu loᚥi:
1.3. NhÃģm cháŧĐc trong phÃĒn táŧ háŧĢp chášĨt háŧŊu cÆĄ
a. KhÃĄi niáŧm
|
NhÃģm cháŧĐc là nguyÊn táŧ hoáš·c nhÃģm nguyÊn táŧ trong phÃĒn táŧ gÃĒy ra nháŧŊng tÃnh chášĨt hoÃĄ háŧc Äáš·c trÆ°ng cáŧ§a háŧĢp chášĨt háŧŊu cÆĄ. |
Và dáŧĨ: Dimethyl ether (H3CâOâCH3) và ethanol (C2H5âOH) cÃģ cÃđng cÃīng tháŧĐc phÃĒn táŧ C2H6O nhÆ°ng cÃģ cÃĄc tÃnh chášĨt khÃĄc nhau. Dimethyl ether khÃīng phášĢn áŧĐng váŧi sodium, trong khi ethanol phášĢn áŧĐng váŧi sodium giášĢi phÃģng hydrogen.
2C2H5OH + 2Na â 2C2H5ONa + H2
- NhÃģm âOH ÄÃĢ gÃĒy ra cÃĄc phášĢn áŧĐng Äáš·c trÆ°ng, phÃĒn biáŧt ethanol váŧi dimethyl ether và váŧi cÃĄc loᚥi háŧĢp chášĨt khÃĄc nÊn nhÃģm âOH ÄÆ°áŧĢc gáŧi là nhÃģm cháŧĐc alcohol.
b. Máŧt sáŧ loᚥi nhÃģm cháŧĐc cÆĄ bášĢn
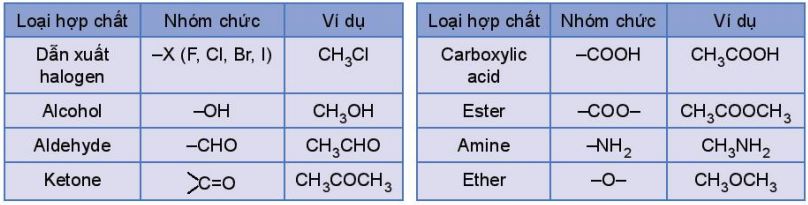
BášĢng 10.1. Máŧt sáŧ nhÃģm cháŧĐc cÆĄ bášĢn và cÃīng tháŧĐc cášĨu tᚥo
c. Pháŧ háŧng ngoᚥi và nhÃģm cháŧĐc
|
PhÆ°ÆĄng phÃĄp pháŧ háŧng ngoᚥi (Infrared Spectroscopy, ÄÆ°áŧĢc viášŋt tášŊt là IR) là phÆ°ÆĄng phÃĄp vášt là rášĨt quan tráŧng và pháŧ biášŋn Äáŧ nghiÊn cáŧĐu cášĨu tᚥo phÃĒn táŧ háŧĢp chášĨt háŧŊu cÆĄ. |
- Máŧi liÊn kášŋt trong phÃĒn táŧ háŧĢp chášĨt háŧŊu cÆĄ hášĨp tháŧĨ máŧt và i báŧĐc xᚥ háŧng ngoᚥi Äáš·c trÆ°ng cho liÊn kášŋt ÄÃģ.
- Pháŧ háŧng ngoᚥi cáŧ§a máŧt chášĨt ÄÆ°áŧĢc mÃĄy pháŧ ghi lᚥi táŧą Äáŧng khi cho nguáŧn báŧĐc xᚥ háŧng ngoᚥi Äi qua chášĨt nghiÊn cáŧĐu.
- Pháŧ háŧng ngoᚥi thÆ°áŧng biáŧu tháŧ sáŧą pháŧĨ thuáŧc cáŧ§a Äáŧ truyáŧn qua (%) cáŧ§a báŧĐc xᚥ háŧng ngoᚥi và o sáŧ sÃģng (cmâ1).
- CÃĄc cáŧąc tiáŧu truyáŧn qua (hoáš·c cáŧąc Äᚥi hášĨp tháŧĨ) áŧĐng váŧi dao Äáŧng cáŧ§a cÃĄc liÊn kášŋt trong phÃĒn táŧ chášĨt nghiÊn cáŧĐu ÄÆ°áŧĢc gáŧi là cÃĄc tÃn hiáŧu (hoáš·c peak).
- Dáŧąa và o cÃĄc sáŧ sÃģng hášĨp tháŧĨ Äáš·c trÆ°ng trÊn pháŧ IR cÃģ tháŧ dáŧą ÄoÃĄn nhÃģm cháŧĐc trong phÃĒn táŧ chášĨt nghiÊn cáŧĐu.
VÃ dáŧĨ:
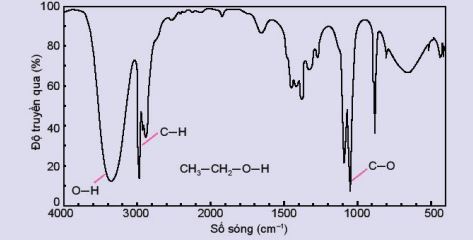
HÃŽnh 10.2. Pháŧ háŧng ngoᚥi cáŧ§a ethanol
- BášĢng 10.2 là sáŧ sÃģng Äáš·c trÆ°ng cáŧ§a máŧt sáŧ nhÃģm cháŧĐc cÆĄ bášĢn (pháŧ háŧng ngoᚥi).
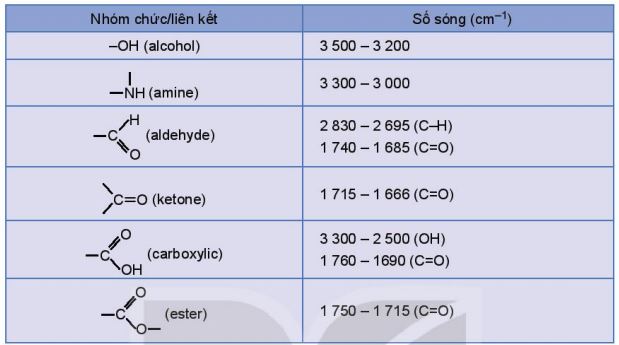
BášĢng 10.2. Sáŧ sÃģng hášĨp tháŧĨ Äáš·c trÆ°ng trÊn pháŧ háŧng ngoᚥi cáŧ§a máŧt sáŧ nhÃģm cháŧĐc cÆĄ bášĢn
BÃ i tášp minh háŧa
BÃ i 1. Cho máŧt sáŧ phÃĄt biáŧu váŧ Äáš·c Äiáŧm chung cáŧ§a cÃĄc phÃĒn táŧ háŧĢp chášĨt háŧŊu cÆĄ
1. Thà nh phᚧn nguyÊn táŧ cháŧ§ yášŋu là C và H.
2. CÃģ tháŧ cháŧĐa nguyÊn táŧ khÃĄc nhÆ° Cl, N, P, O.
3. LiÊn kášŋt hÃģa háŧc cháŧ§ yášŋu là liÊn kášŋt cáŧng hÃģa tráŧ.
4. LiÊn kášŋt hÃģa háŧc cháŧ§ yášŋu là liÊn kášŋt ion.
5. Dáŧ bay hÆĄi, khÃģ chÃĄy.
6. PhášĢn áŧĐng hÃģa háŧc xášĢy ra nhanh.
7. PhášĢn áŧĐng xášĢy ra theo nhiáŧu hÆ°áŧng
CÃĄc cÃĒu ÄÚng lÃ
A. 1, 2, 5, 6.
B. 1, 2, 3, 5.
C. 1, 2, 3, 7.
D. 1, 2, 4, 6.
HÆ°áŧng dášŦn giášĢi
CÃĄc phÃĒn táŧ háŧĢp chášĨt háŧŊu cÆĄ cÃģ Äáš·c Äiáŧm chung là :
1. Thà nh phᚧn nguyÊn táŧ cháŧ§ yášŋu là C và H.
2. CÃģ tháŧ cháŧĐa nguyÊn táŧ khÃĄc nhÆ° Cl, N, P, O.
3. LiÊn kášŋt hÃģa háŧc cháŧ§ yášŋu là liÊn kášŋt cáŧng hÃģa tráŧ.
7. PhášĢn áŧĐng xášĢy ra theo nhiáŧu hÆ°áŧng, tᚥo háŧn háŧĢp sášĢn phášĐm
â ÄÃĄp ÃĄn: C
Bà i 2. ChášĨt nà o sau ÄÃĒy là hydrocarbon ?
A. CH2O
B. C2H5Br
C. C6H6
D. CH3COOH.
HÆ°áŧng dášŦn giášĢi
Hydrocarbon là nháŧŊng háŧĢp chášĨt ÄÆ°áŧĢc tᚥo thà nh cháŧ táŧŦ hai nguyÊn táŧ carbon và hydrogen
â ÄÃĄp ÃĄn: C
Bà i 3. ChášĨt nà o sau ÄÃĒy là dášŦn xuášĨt cáŧ§a hydrocarbon ?
A. CO2
B. C2H6
C. C6H6
D. C3H6Br.
HÆ°áŧng dášŦn giášĢi
Khi máŧt hay nhiáŧu nguyÊn táŧ hydrogen trong phÃĒn táŧ hydrocarbon ÄÆ°áŧĢc thay thášŋ bášąng máŧt hay nhiáŧu nguyÊn táŧ hay nhÃģm nguyÊn táŧ khÃĄc (thÆ°áŧng cháŧĐa oxygen, nitrogen, sulfur, halogen,...), thu ÄÆ°áŧĢc dášŦn xuášĨt cáŧ§a hydrocarbon.
â ÄÃĄp ÃĄn: D
Luyáŧn tášp BÃ i 10 HÃģa 11 Kášŋt Náŧi Tri TháŧĐc
Háŧc xong bà i háŧc nà y, em cÃģ tháŧ:
- NÊu ÄÆ°áŧĢc khÃĄi niáŧm háŧĢp chášĨt háŧŊu cÆĄ và hoÃĄ háŧc háŧŊu cÆĄ; Äáš·c Äiáŧm chung cáŧ§a cÃĄc háŧĢp chášĨt háŧŊu cÆĄ; nhÃģm cháŧĐc và máŧt sáŧ loᚥi nhÃģm cháŧĐc cÆĄ bášĢn.
- PhÃĒn loᚥi ÄÆ°áŧĢc háŧĢp chášĨt háŧŊu cÆĄ (hydrocarbon và dášŦn xuášĨt).
- Sáŧ dáŧĨng ÄÆ°áŧĢc bášĢng tÃn hiáŧu pháŧ háŧng ngoᚥi (IR) Äáŧ xÃĄc Äáŧnh máŧt sáŧ nhÃģm cháŧĐc cÆĄ bášĢn.
3.1. TrášŊc nghiáŧm BÃ i 10 HÃģa 11 Kášŋt Náŧi Tri TháŧĐc
CÃĄc em cÃģ tháŧ háŧ tháŧng lᚥi náŧi dung kiášŋn tháŧĐc ÄÃĢ háŧc ÄÆ°áŧĢc thÃīng qua bà i kiáŧm tra TrášŊc nghiáŧm HÃģa háŧc 11 KNTT Bà i 10 cáŧąc hay cÃģ ÄÃĄp ÃĄn và láŧi giášĢi chi tiášŋt.
-
CÃĒu 1:
HáŧĢp chášĨt háŧŊu cÆĄ lÃ
- A. HáŧĢp chášĨt khÃģ tan trong nÆ°áŧc.
- B. HáŧĢp chášĨt cáŧ§a carbon và máŧt sáŧ nguyÊn táŧ khÃĄc tráŧŦ N, Cl, O.
- C. HáŧĢp chášĨt cáŧ§a carbon tráŧŦ CO, CO2, H2CO3, muáŧi carbonate kim loᚥiâĶ
- D. HáŧĢp chášĨt cÃģ nhiáŧt Äáŧ sÃīi cao.
-
- A. CO2
- B. CO
- C. K2CO3
- D. CH4
-
- A. 30%
- B. 40%
- C. 50%
- D. 60%
CÃĒu 4-10: Máŧi cÃĄc em ÄÄng nhášp xem tiášŋp náŧi dung và thi tháŧ Online Äáŧ cáŧ§ng cáŧ kiášŋn tháŧĐc váŧ bà i háŧc nà y nhÃĐ!
3.2. BÃ i tášp SGK BÃ i 10 HÃģa 11 Kášŋt Náŧi Tri TháŧĐc
CÃĄc em cÃģ tháŧ xem thÊm phᚧn hÆ°áŧng dášŦn GiášĢi bà i tášp HÃģa háŧc 11 KNTT Bà i 10 Äáŧ giÚp cÃĄc em nášŊm váŧŊng bà i háŧc và cÃĄc phÆ°ÆĄng phÃĄp giášĢi bà i tášp.
Máŧ Äᚧu trang 57 SGK HÃģa háŧc 11 Kášŋt náŧi tri tháŧĐc â KNTT
GiášĢi CÃĒu háŧi 1 trang 58 SGK HÃģa háŧc 11 Kášŋt náŧi tri tháŧĐc â KNTT
GiášĢi CÃĒu háŧi 2 trang 58 SGK HÃģa háŧc 11 Kášŋt náŧi tri tháŧĐc â KNTT
GiášĢi CÃĒu háŧi 3 trang 58 SGK HÃģa háŧc 11 Kášŋt náŧi tri tháŧĐc â KNTT
GiášĢi CÃĒu háŧi 4 trang 59 SGK HÃģa háŧc 11 Kášŋt náŧi tri tháŧĐc â KNTT
GiášĢi CÃĒu háŧi 5 trang 60 SGK HÃģa háŧc 11 Kášŋt náŧi tri tháŧĐc â KNTT
Hoᚥt Äáŧng trang 60 SGK HoÃĄ háŧc 11 Kášŋt náŧi tri tháŧĐc â KNTT
GiášĢi CÃĒu háŧi 6 trang 61 SGK HÃģa háŧc 11 Kášŋt náŧi tri tháŧĐc â KNTT
GiášĢi CÃĒu háŧi 7 trang 61 SGK HÃģa háŧc 11 Kášŋt náŧi tri tháŧĐc â KNTT
GiášĢi CÃĒu háŧi 8 trang 62 SGK HÃģa háŧc 11 Kášŋt náŧi tri tháŧĐc â KNTT
Háŧi ÄÃĄp BÃ i 10 HÃģa 11 Kášŋt Náŧi Tri TháŧĐc
Trong quÃĄ trÃŽnh háŧc tášp nášŋu cÃģ thášŊc mášŊc hay cᚧn tráŧĢ giÚp gÃŽ thÃŽ cÃĄc em hÃĢy comment áŧ máŧĨc Háŧi ÄÃĄp, Cáŧng Äáŧng HÃģa háŧc HOC247 sáš― háŧ tráŧĢ cho cÃĄc em máŧt cÃĄch nhanh chÃģng!
ChÚc cÃĄc em háŧc tášp táŧt và luÃīn Äᚥt thà nh tÃch cao trong háŧc tášp!