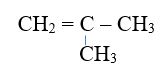Thông qua nội dung lý thuyết và bài tập Bài 13: Cấu tạo hoá học hợp chất hữu cơ môn Hóa học 11 Kết Nối Tri Thức được biên soạn và tóm tắt bởi HOC247, các em sẽ nắm được Thuyết cấu tạo hoá học, công thức cấu tạo, đồng đẳng, đồng phân của các hợp chất hữu cơ. Hãy cùng bắt đầu khám phá bài học này để tìm hiểu thêm nhiều điều kì thú về hoá học hữu cơ nhé!
Tóm tắt lý thuyết
1.1. Thuyết cấu tạo hoá học
Năm 1861, Butlerov (Bút-lê-rốp) đưa ra khái niệm cấu tạo hoá học và thuyết cấu tạo hoá học bao gồm những luận điểm chính sau:
1. Trong phân tử chất hữu cơ, các nguyên tử liên kết với nhau theo đúng hoá trị và theo một thứ tự nhất định. Thứ tự liên kết đó được gọi là cấu tạo hoá học. Sự thay đổi thủ tự liên kết đó sẽ tạo ra chất khác.
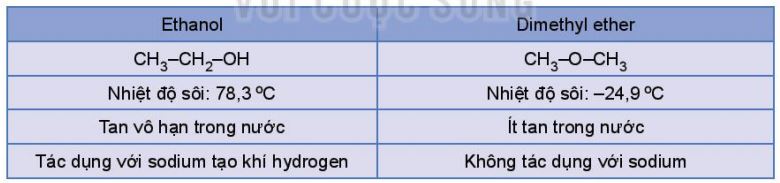
Ví dụ: Ethanol và dimethyl ether đều có công thức phân tử C2H6O nhưng có tính chất vật lí và tính chất hoá học rất khác nhau do chúng có cấu tạo khác nhau.
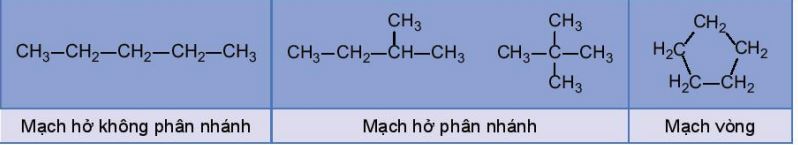
2. Trong phân tử chất hữu cơ, carbon có hoá trị IV. Các nguyên tử carbon không những liên kết với nguyên tử của các nguyên tố khác mà còn có thể liên kết trực tiếp với nhau tạo thành mạch carbon (mạch hở không phân nhánh, mạch hở phân nhánh hoặc mạch vòng).
Ví dụ:
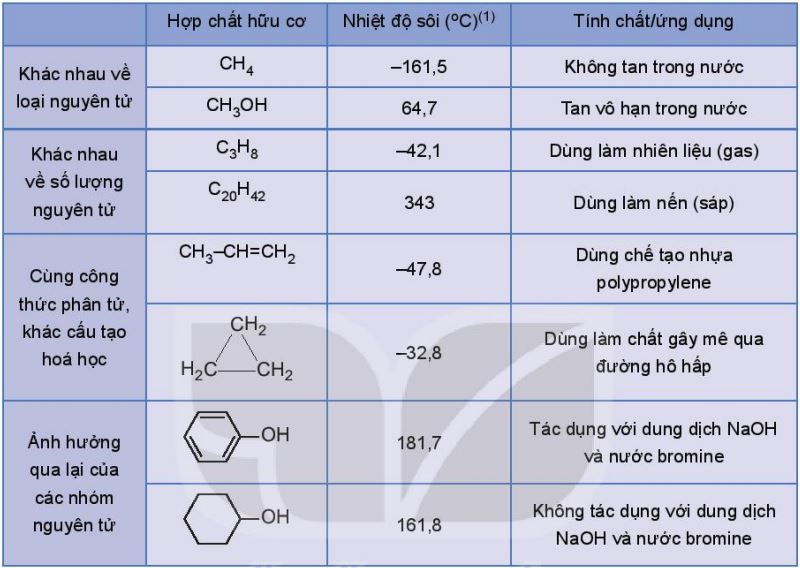
3. Tính chất của các chất phụ thuộc vào thành phần phân tử (bản chất và số lượng các nguyên tử) và cấu tạo hoá học. Các nguyên tử trong phân tử có ảnh hưởng qua lại lẫn nhau.
Ví dụ:
|
Thuyết cấu tạo hoá học giúp giải thích được hiện tượng đồng phân, hiện tượng đồng đẳng trong hoá học hữu cơ. |
1.2. Công thức cấu tạo
a. Khái niệm
|
Công thức biểu diễn cách liên kết và thứ tự liên kết giữa các nguyên tử trong phân tử được gọi là công thức cấu tạo. |
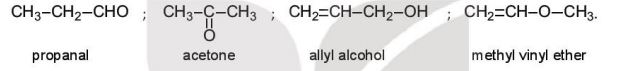
Ví dụ: Ứng với công thức phân tử C3H6O có bốn công thức cấu tạo mạch hở như sau:
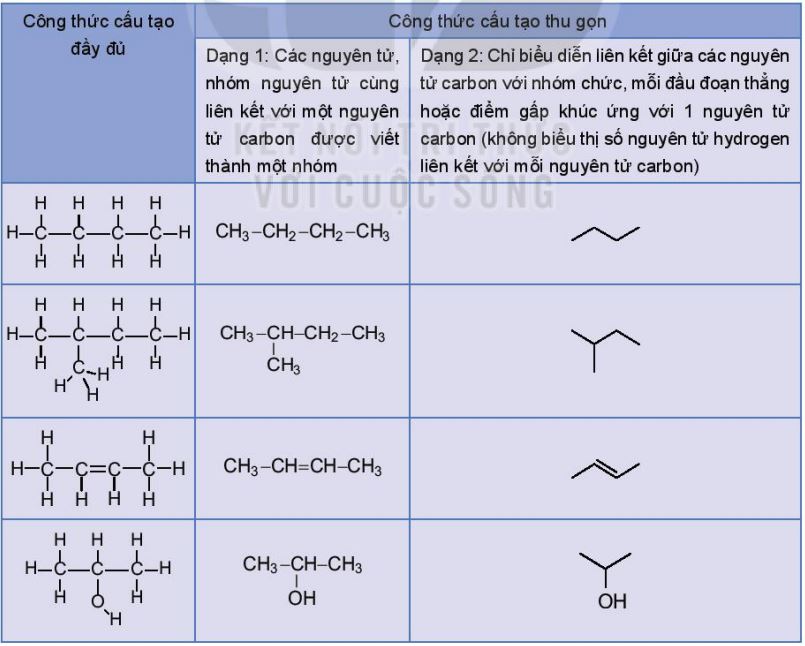
b. Cách biểu diễn cấu tạo phân tử hợp chất hữu cơ
1.3. Đồng phân
Hình 13.1. Ba hợp chất có cùng công thức phân tử Colis
- Ba hợp chất pinene, ocimene, myrcene có tính chất khác nhau nhưng lại có cùng công thức phân tử là C10H16 nên chúng là những chất đồng phân của nhau.
|
Những hợp chất hữu cơ khác nhau nhưng có cùng công thức phân tử được gọi là các chất đồng phân |
- Các chất này có cùng công thức phân tử nhưng có tinh chất khác nhau là do chúng có cấu tạo hoá học khác nhau.
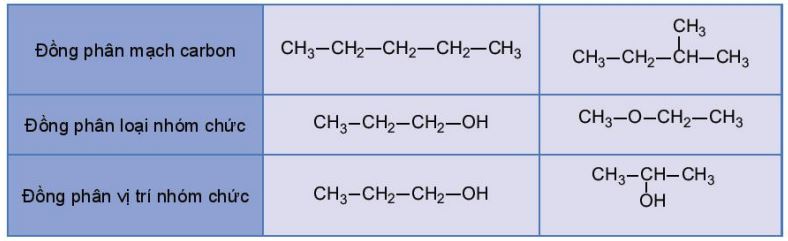
- Ứng với một công thức phân tử có thể có các đồng phân cấu tạo về mạch carbon, loại nhóm chức, vị trí nhóm chức.
Ví dụ:
1.4. Đồng đẳng
|
Các chất hữu cơ có tính chất hoá học tương tự nhau và thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 được gọi là các chất đồng đẳng của nhau, chúng hợp thành một dãy đồng đẳng. |
Ví dụ:
Bài tập minh họa
Hợp chất X có CTPT C4H8. Xác định các đông phân cấu tạo của X
Hướng dẫn giải
- Xác định độ bất bão hòa của phân tử hợp chất hữu cơ qua công thức:
- Xét CTPT của hợp chất hữu cơ có dạng: CxHyOzNtClu
- Độ bất bão hòa: \(\Delta =\frac{2x+2-y+t-u}{2}\)
Biết Δ = số \(\pi \) + số vòng từ đó xác định được dạng công thức của hợp chất.
Ta có: Δ = (2.4+2-8)/2= 1 ⇒ có 1 lk \(\pi \) hoặc 1 vòng ⇒ có 2 dạng mạch cacbon:
- Mạch hở có 1 liên kết đôi trong phân tử
+ Mạch chính 4C: C-C-C-C viết được 2 công thức đồng phân vị trí nối đôi:
CH2 = CH-CH2 –CH3 và CH3 - CH=CH –CH3
+ Mạch chính 3C: viết được 1 đồng phân
- Mạch vòng và chỉ có liên kết đơn
+ Vòng 4 cạnh
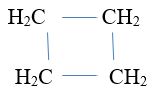
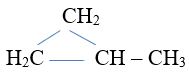
+ Vòng 3 cạnh
⇒ Công thức C4H8 có 5 đồng phân.
Luyện tập Bài 13 Hóa 11 Kết Nối Tri Thức
Học xong bài học này, em có thể:
- Trình bày được nội dung thuyết cấu tạo hoá học trong hoá học hữu cơ.
- Giải thích được hiện tượng đồng phân trong hoá học hữu cơ.
- Nêu được khái niệm chất đồng đẳng và dãy đồng đẳng; chất đồng đẳng, chất đồng phân dựa vào công thức cấu tạo cụ thể của các hợp chất hữu cơ.
Viết được công thức cấu tạo của một số hợp chất hữu cơ đơn giản (công thức cấu tạo đầy đủ, công thức cấu tạo thu gọn).
3.1. Trắc nghiệm Bài 13 Hóa 11 Kết Nối Tri Thức
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Hóa học 11 KNTT Bài 13 cực hay có đáp án và lời giải chi tiết.
-
- A. Ion
- B. Hydrogen
- C. Kim loại
- D. Cộng hóa trị
-
Câu 2:
Phân loại mạch carbon gồm
- A. Mạch không phân nhánh (mạch thẳng)
- B. Mạch nhánh
- C. Mạch vòng
- D. Cả A, B, C đều đúng
-
- A. Thành phần phân tử
- B. Trật tự liên kết giữa các nguyên tử trong phân tử
- C. Thành phần phân tử và trật tự liên kết giữa các nguyên tử trong phân tử
- D. Thành phần phân tử và sự tham gia liên kết với các hợp chất khác
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
3.2. Bài tập SGK Bài 13 Hóa 11 Kết Nối Tri Thức
Các em có thể xem thêm phần hướng dẫn Giải bài tập Hóa học 11 KNTT Bài 13 để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Mở đầu trang 70 SGK Hóa học 11 Kết nối tri thức – KNTT
Giải Câu hỏi 1 trang 75 SGK Hóa học 11 Kết nối tri thức – KNTT
Giải Câu hỏi 2 trang 75 SGK Hóa học 11 Kết nối tri thức – KNTT
Giải Câu hỏi 3 trang 77 SGK Hóa học 11 Kết nối tri thức – KNTT
Giải Câu hỏi 4 trang 78 SGK Hóa học 11 Kết nối tri thức – KNTT
Giải Câu hỏi 5 trang 78 SGK Hóa học 11 Kết nối tri thức – KNTT
Hoạt động trang 78 SGK Hoá học 11 Kết nối tri thức – KNTT
Giải Câu hỏi 6 trang 79 SGK Hóa học 11 Kết nối tri thức – KNTT
Giải Câu hỏi 7 trang 79 SGK Hóa học 11 Kết nối tri thức – KNTT
Hỏi đáp Bài 13 Hóa 11 Kết Nối Tri Thức
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học HOC247 sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!