Bài tập 39.8 trang 87 SBT Hóa học 10
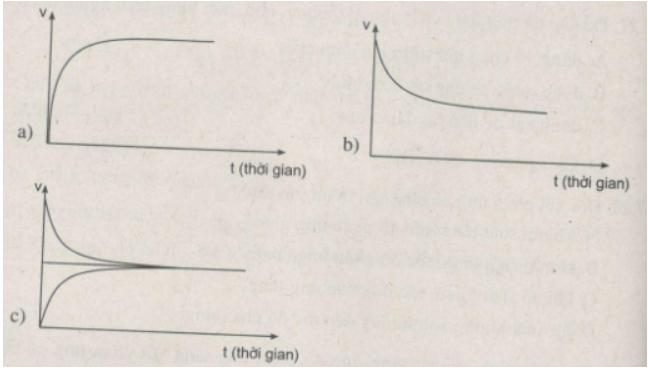
Đồ thị nào sau đây biểu diễn sự biến đổi tốc độ phản ứng thuận theo thời gian ? Sự biến đổi tốc độ phản ứng nghịch theo thời gian ? Trạng thái cân bằng hoá học ?
Hướng dẫn giải chi tiết bài 39.8
Đồ thị a biểu diễn sự biến đổi tốc độ phản ứng thuận theo thời gian.
Đồ thị b biểu diễn sự biến đổi tốc độ phản ứng nghịch theo thời gian.
Đồ thị c biểu diễn trạng thái cân bằng hoá học.
-- Mod Hóa Học 10 HỌC247
Bài tập SGK khác
Bài tập 39.6 trang 86 SBT Hóa học 10
Bài tập 39.7 trang 87 SBT Hóa học 10
Bài tập 39.9 trang 87 SBT Hóa học 10
Bài tập 39.10 trang 87 SBT Hóa học 10
Bài tập 39.11 trang 88 SBT Hóa học 10
Bài tập 39.12 trang 88 SBT Hóa học 10
Bài tập 39.13 trang 88 SBT Hóa học 10
Bài tập 39.14 trang 88 SBT Hóa học 10
Bài tập 39.15 trang 88 SBT Hóa học 10
Bài tập 39.16 trang 88 SBT Hóa học 10
Bài tập 39.17 trang 88 SBT Hóa học 10
Bài tập 1 trang 216 SGK Hóa học 10 nâng cao
Bài tập 2 trang 216 SGK Hóa học 10 nâng cao
Bài tập 3 trang 216 SGK Hóa học 10 nâng cao
Bài tập 4 trang 216 SGK Hóa học 10 nâng cao
Bài tập 5 trang 216 SGK Hóa học 10 nâng cao
-


Cho phản ứng: \(Na_{2}S_{2}O_{3} (l) + H_{2}SO_{4} (l) \xrightarrow[]{\ \ \ \ \ \ }Na_{2}SO_{4} (l) + SO_{2} (k) + S (r) + H_{2}O (l).\) Khi thay đổi một trong các yếu tố: (1) tăng nhiệt độ; (2) tăng nồng độ Na2S2O3; (3) giảm nồng độ H2SO4; (4) giảm nồng độ Na2SO4; (5) giảm áp suất của SO2; (6) dùng chất xúc tác; có bao nhiêu yếu tố làm tăng tốc độ của phản ứng đã cho?
bởi Hồng Hạnh
 10/03/2022
Theo dõi (0) 1 Trả lời
10/03/2022
Theo dõi (0) 1 Trả lời -


Cho cân bằng hóa học sau: N2 + 3H2 ⇄ 2NH3 ∆H = -92kJ Tác động làm cân bằng chuyển dịch theo chiều thuận là?
bởi Nguyễn Thị Thu Huệ
 11/03/2022
Theo dõi (0) 1 Trả lời
11/03/2022
Theo dõi (0) 1 Trả lời -


Cho phương trình hóa học của phản ứng: X + 2Y Z + T. Ở thời điểm ban đầu, nồng độ của chất X là 0,01 mol/l. Sau 20 giây, nồng độ của chất X là 0,008 mol/l. Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên là?
bởi Thụy Mây
 10/03/2022
Theo dõi (0) 1 Trả lời
10/03/2022
Theo dõi (0) 1 Trả lời -


Cho các cân bằng sau trong các bình riêng biệt: H2 (k, không màu) + I2 (k, tím) ⇄ 2HI (k, không màu) (1) 2NO2 (k, nâu đỏ) ⇄ N2O4 (k, không màu) (2) Nếu làm giảm thể tích bình chứa của cả 2 hệ trên, so với ban đầu thì màu của?
bởi Bình Nguyen
 10/03/2022
Theo dõi (0) 1 Trả lời
10/03/2022
Theo dõi (0) 1 Trả lời -
ADMICRO


Trong công ngiệp, sản xuất NH3, phản ứng xảy ra tạo thành một cân bằng hóa học. Cân bằng hóa học này phải thực hiện ở áp suất cao, nhiệt độ thấp nhưng không quá thấp (khoảng 4500C). Từ đó suy ra đặc điểm của phản ứng là gì?
bởi Lan Anh
 10/03/2022
Theo dõi (0) 1 Trả lời
10/03/2022
Theo dõi (0) 1 Trả lời -


Thực hiện thí nghiệm hòa tan đá vôi (CaCO3) bằng dung dịch HCl, biện pháp nào sau đây có thể làm tăng tốc độ phản ứng?
bởi Nguyen Nhan
 10/03/2022
10/03/2022
A. Tăng thể tích của dung dịch HCl
B. Giảm nồng độ của dung dịch HCl
C. Hạ nhiệt độ xuống
D. Nghiền nhỏ đá vôi
Theo dõi (0) 1 Trả lời -


Trong số các yếu tố sau: nồng độ, nhiệt độ, áp suất, diện tích tiếp xúc và chất xúc tác. Có nhiều nhất bao nhiêu yếu tố có thể ảnh hưởng tới một cân bằng hóa học?
bởi hà trang
 10/03/2022
Theo dõi (0) 1 Trả lời
10/03/2022
Theo dõi (0) 1 Trả lời -


Cho phương trình hóa học của phản ứng : X + 2Y → Z + T. Ở thời điểm ban đầu, nồng độ của chất X là 0,2 mol/l. Sau 40s, nồng độ của chất X là 0,04 mol/l. Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên là?
bởi Quế Anh
 11/03/2022
Theo dõi (0) 1 Trả lời
11/03/2022
Theo dõi (0) 1 Trả lời