NαΜôi dung bΟ†i giαΚΘng SΤΓ lΤΑαΜΘc vαΜ¹ hαΜΘp chαΚΞt cΟ≥ oxi cαΜßa clo tΟ§m hiαΜÉu nΤΑαΜ¦c Javen vΟ† Clorua vΟ¥i cΟ≥ thΟ†nh phαΚßn, tΟ≠nh chαΚΞt, cαΚΞu tαΚΓo nhΤΑ thαΚΩ nΟ†o? ChΟΚng ΡëΤΑαΜΘc dΟΙng lΟ†m gΟ§ vΟ† ΡëΤΑαΜΘc ΡëiαΜ¹u chαΚΩ bαΚ±ng cΟΓch nΟ†o?
TΟ≥m tαΚ·t lΟΫ thuyαΚΩt
1.1. ThΟ†nh phαΚßn, tΟ≠nh chαΚΞt vΟ† αΜ©ng dαΜΞng cαΜßa nΤΑαΜ¦c Javel vΟ† clorua vΟ¥i
| NΤΑαΜ¦c Javel | Clorua vΟ¥i | |
| ThΟ†nh phαΚßn |
Dung dαΜ΄ch: NaCl vΟ† NaClO. NaClO β΅î HClO natri hipoclorit axit hipoclorΤΓ |
- CTPT: CaOCl2 - CTCT:
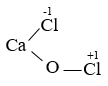 βÜ£ muαΜëi hαΜ½n tαΚΓp. |
| TΟ≠nh chαΚΞt |
- TΟ≠nh tαΚ©y mΟ†u, sΟΓt trΟΙng. - NaClO lΟ† muαΜëi cαΜßa axit yαΚΩu:
NaClO + CO2 + H2O βÜ£ HClO + NaHCO3 - NaClO, HClO: cΟ≥ tΟ≠nh oxi hΟ≥a rαΚΞt mαΚΓnh. |
- ChαΚΞt bαΜôt, mΟ†u trαΚ·ng, xαΜëp. - TΟ≠nh oxi hΟ≥a mαΚΓnh:
CaOCl2 + 2HCl βÜ£CaCl2 + Cl2+ H2O - TΟΓc dαΜΞng vαΜ¦i CO2 trong khΟ¥ng khΟ≠ αΚ©m: 2CaOCl2 + CO2 + H2O βÜ£ 2HClO + CaCO3 + CaCl2 |
| αΜ®ng dαΜΞng |
- TαΚ©y trαΚ·ng vαΚΘi, sαΜΘi, giαΚΞy, ... - TαΚ©y uαΚΩ chuαΜ™ng trαΚΓi chΡÉn nuΟ¥i, nhΟ† vαΜ΅ sinh |
- TαΚ©y trαΚ·ng, tαΚ©y uαΚΩ. - Tinh chαΚΩ dαΚßu mαΜè. - XαΜ≠ lΟ≠ cΟΓc chαΚΞt ΡëαΜôc, bαΚΘo vαΜ΅ mΟ¥i trΤΑαΜùng. |
1.1.1 NΤΑαΜ¦c Javel
- NΤΑαΜ¦c Javel lΟ† dung dαΜ΄ch hαΜ½n hαΜΘp muαΜëi NaCl vΟ† NaClO.
- MuαΜëi NaClO cΟ≥ tΟ≠nh oxi hΟ≥a rαΚΞt mαΚΓnh, do vαΚ≠y nΤΑαΜ¦c Javel cΟ≥ tΟ≠nh tαΚ©y mΟ†u, sΟΓt trΟΙng, tαΚ©y trαΚ·ng vαΚΘi, sαΜΘi, giαΚΞy vΟ† dΟΙng sΟΓt trΟΙng chuαΜ™ng trαΚΓi chΡÉn nuΟ¥i, nhΟ† vαΜ΅ sinh.
- NaClO lΟ† muαΜëi cαΜßa axit rαΚΞt yαΚΩu, yαΚΩu hΤΓn axit cacbonic nΟΣn dαΜÖ tΟΓc dαΜΞng vαΜ¦i CO2 cαΜßa khΟ¥ng khΟ≠ tαΚΓo thΟ†nh axit HClO cΟ≥ tΟ≠nh oxi hΟ≥a mαΚΓnh.
β΅£ nΤΑαΜ¦c Javel khΟ¥ng ΡëαΜÉ ΡëΤΑαΜΘc lΟΔu trong khΟ¥ng khΟ≠.
1.1.2. Clorua vΟ¥i CaOCl2
- Clorua vΟ¥i lΟ† chαΚΞt bαΜôt mΟ†u trαΚ·ng, xαΜëp, mΟΙi xαΜëc, cΟ≥ tΟ≠nh oxi hΟ≥a mαΚΓnh.
- TΟΓc dαΜΞng vαΜ¦i axit clohidric cho Cl2¬≠
CaOCl2 + 2HCl βÜ£ CaCl2 + Cl2 + H2O
- Trong khΟ¥ng khΟ≠ αΚ©m, clorua vΟ¥i tΟΓc dαΜΞng vαΜ¦i CO2 tαΚΓo ra axit hipoclorΤΓ
1.2. ΡêiαΜ¹u chαΚΩ nΤΑαΜ¦c Javel vΟ† clorua vΟ¥i
1.2.1. ΡêiαΜ¹u chαΚΩ nΤΑαΜ¦c Javel
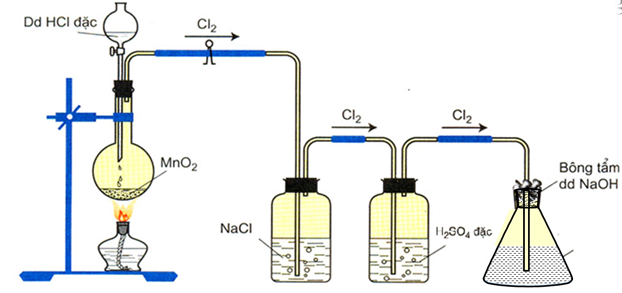
- Trong phΟ≤ng thΟ≠ nghiαΜ΅m:
Cho khΟ≠ clo tΟΓc dαΜΞng vαΜ¦i NaOH loΟΘng αΜü nhiαΜ΅t ΡëαΜô thΤΑαΜùng:
Cl2 + 2NaOH βÜ£ NaCl + NaClO + H2O
HΟ§nh 1: SΤΓ ΡëαΜ™ ΡëiαΜ¹u chαΚΩ nΤΑαΜ¦c Javel trong phΟ≤ng thΟ≠ nghiαΜ΅m
- Trong cΟ¥ng nghiαΜ΅p:
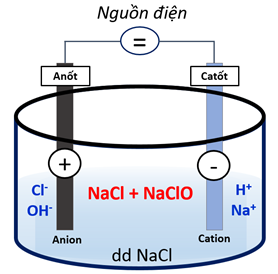
βÄ΄ΡêiαΜ΅n phΟΔn dung dαΜ΄ch NaCl nαΜ™ng ΡëαΜô 15 βÄ™ 20% trong thΟΙng ΡëiαΜ΅n phΟΔn khΟ¥ng cΟ≥ mΟ†ng ngΡÉn.
\(2NaCl + 2{H_2}O \to 2NaOH + {H_2} \uparrow + C{l_2} \uparrow \)
\(C{l_2} + 2NaOH \to NaCl + NaClO + H{}_2O\)
HΟ§nh 2: ΡêiαΜ¹u chαΚΩ nΤΑαΜ¦c Javel trong cΟ¥ng nghiαΜ΅p
1.2.2. ΡêiαΜ¹u chαΚΩ clorua vΟ¥i
Cho clo tΟΓc dαΜΞng vαΜ¦i vΟ¥i tΟ¥i (sαΜ·a vΟ¥i) αΜü 30oC thu ΡëΤΑαΜΘc clorua vΟ¥i:
Cl2 + Ca(OH)2 βÜ£ CaOCl2 + H2O (to = 30OC)

Hϧnh 3: Clorua vϥi
BΟ†i tαΚ≠p minh hαΜça
Bφi 1:
ViαΚΩt phΤΑΤΓng trΟ§nh phαΚΘn αΜ©ng biαΜÉu diαΜÖn sΤΓ ΡëαΜ™ chuyαΜÉn hΟ≥a sau:
HΤΑαΜ¦ng dαΚΪn:
(1) \(2KMn{O_4} + 16HCl \to 2KCl + 2MnC{l_2} + 5C{l_2} \uparrow + 8{H_2}O\)
(2) \(C{l_2} + 2NaOH \to NaCl + NaClO + {H_2}O\)
(3) \(Mn{O_2} + 4HCl \to MnC{l_2} + C{l_2} \uparrow + 2{H_2}O\)
(4) \(C{l_2} + Ca{(OH)_2} \to CaOC{l_2} + {H_2}O\) ΡêK: αΜû 30oC
(5) \(CaOC{l_2} + 2HCl \to CaC{l_2} + C{l_2} + {H_2}O\)
HoαΚΖc \(CaOC{l_2} \to CaC{l_2} + \frac{1}{2}{O_2}\) ΡêK: toc
Bφi 2:
ViαΚΩt cΟΓc phΤΑΤΓng trΟ§nh phαΚΘn αΜ©ng ΡëiαΜ¹u chαΚΩ nΤΑαΜ¦c Javel tαΜΪ cΟΓc chαΚΞt cΟ≥ trong phΟ≤ng thΟ≠ nghiαΜ΅m: NaCl, MnO2, H2SO4 ΡëαΚΖc, NaOH
HΤΑαΜ¦ng dαΚΪn:
- ΡêiαΜ¹u chαΚΩ axit HCl tαΜΪ NaCl, H2SO4 ΡëαΚΖc, H2O
NaCl (r) + H2SO4 (ΡëαΚΖc) βÜ£ NaHSO4 + HCl ΡêK: tOC
- TαΜΪ HCl vaΧÄ MnO2 ΡëiαΜ¹u chαΚΩ khiΧ¹ Cl2
MnO2 + 4HCl (ΡëαΚΖc) βÜ£ MnCl2 + Cl2 + 2H2O ΡêK: tOC
- TαΜΪ Cl2 vaΧÄ dung dαΜ΄ch NaOH loΟΘng nguαΜôi ΡëiαΜ¹u chαΚΩ nΤΑαΜ¦c Javel
Cl2+ 2NaOH βÜ£ NaCl + NaClO + H2O
Bφi 3:
ChαΜâ dΟΙng mαΜôt thuαΜëc thαΜ≠, hΟΘy nhαΚ≠n biαΚΩt cΟΓc dung dαΜ΄ch mαΚΞt nhΟΘn sau: HCl, HClO, NaCl, NaClO
HΤΑαΜ¦ng dαΚΪn:
SαΜ≠ dαΜΞng quαΜ≥ tΟ≠m:
- HCl βÜ£ QΟΙy tΟ≠m hΟ≥a ΡëαΜè
- HClO βÜ£ QΟΙy tΟ≠m khΟ¥ng ΡëαΜïi mΟ†u
- NaCl βÜ£ QΟΙy tΟ≠m mαΚΞt mΟ†u
- NaClO βÜ£ QΟΙy tΟ≠m hΟ≥a ΡëαΜè rαΜ™i mαΚΞt mΟ†u
3. LuyαΜ΅n tαΚ≠p BΟ†i 24 HΟ≥a hαΜçc 10
Sau bΟ†i hαΜçc cαΚßn nαΚ·m: ThΟ†nh phαΚßn hΟ≥a hαΜçc, αΜ©ng dαΜΞng, nguyΟΣn tαΚ·c sαΚΘn xuαΚΞt c≈©ng nhΤΑ tΟ≠nh oxi hΟ≥a mαΚΓnh cαΜßa mαΜôt sαΜë hαΜΘp chαΚΞt cΟ≥ oxi cαΜßa clo (nΤΑαΜ¦c Gia-ven, clorua vΟ¥i).
3.1. TrαΚ·c nghiαΜ΅m
BΟ†i kiαΜÉm tra TrαΚ·c nghiαΜ΅m HΟ≥a hαΜçc 10 BΟ†i 24 cΟ≥ phΤΑΤΓng phΟΓp vΟ† lαΜùi giαΚΘi chi tiαΚΩt giΟΚp cΟΓc em luyαΜ΅n tαΚ≠p vΟ† hiαΜÉu bΟ†i.
-
- A. Oxi nguyΟΣn tΤΑΧâ coΧ¹ tiΧ¹nh oxi hoΧ¹a maΧΘnh.
- B. Cl+ coΧ¹ tiΧ¹nh oxi hoΧ¹a maΧΘnh.
- C. Cl- vaΧÄ oxi nguyΟΣn tΤΑΧâ coΧ¹ taΧ¹c duΧΘng phaΧ¹ huΧây maΧΘnh.
- D. Do caΧ¹c muΟ¥Χ¹i tΤΑΧΘ phΟΔn huΧây.
-
- A. Clorua vΟ¥i reΧâ tiΟΣΧÄn hΤΓn.
- B. Clorua vΟ¥i coΧ¹ haΧÄm lΤΑΤΓΧΘng hipoclorit cao hΤΓn.
- C. Clorua vΟ¥i ΡëΟΣΧâ baΧâo quaΧân vaΧÄ dΟΣΧÉ chuyΟΣn chΤΓΧâ hΤΓn.
- D. CaΧâ A, B, C.
-
- A. Clorua vΟ¥i lΟ† muαΜëi tαΚΓo bαΜüi mαΜôt kim loαΚΓi liΟΣn kαΚΩt vαΜ¦i mαΜôt loαΚΓi gαΜëc axit
- B. Clorua vΟ¥i lΟ† muαΜëi tαΚΓo bαΜüi mαΜôt kim loαΚΓi liΟΣn kαΚΩt vαΜ¦i hai loαΚΓi gαΜëc axit
- C. Clorua vΟ¥i lΟ† muαΜëi tαΚΓo bαΜüi hai kim loαΚΓi liΟΣn kαΚΩt vαΜ¦i mαΜôt loαΚΓi gαΜëc axit
- D. Clorua vΟ¥i khΟ¥ng phαΚΘi lΟ† muαΜëi
CΟΔu 4-10: MαΜùi cΟΓc em ΡëΡÉng nhαΚ≠p xem tiαΚΩp nαΜôi dung vΟ† thi thαΜ≠ Online ΡëαΜÉ cαΜßng cαΜë kiαΚΩn thαΜ©c vαΜ¹ bΟ†i hαΜçc nΟ†y nhΟ©!
3.2. BΟ†i tαΚ≠p SGK vΟ† NΟΔng cao
CΟΓc em cΟ≥ thαΜÉ hαΜ΅ thαΜëng lαΚΓi nαΜôi dung bΟ†i hαΜçc thΟ¥ng qua phαΚßn hΤΑαΜ¦ng dαΚΪn GiαΚΘi bΟ†i tαΚ≠p HΟ≥a hαΜçc 10 BΟ†i 24.
BΟ†i tαΚ≠p 1 trang 108 SGK HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 2 trang 108 SGK HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 3 trang 108 SGK HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 4 trang 108 SGK HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 5 trang 108 SGK HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 24.1 trang 56 SBT HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 24.2 trang 57 SBT HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 24.3 trang 57 SBT HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 24.4 trang 57 SBT HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 24.5 trang 57 SBT HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 24.6 trang 57 SBT HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 24.7 trang 57 SBT HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 24.8 trang 58 SBT HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 24.9 trang 58 SBT HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 24.10 trang 58 SBT HΟ≥a hαΜçc 10
BΟ†i tαΚ≠p 1 trang 134 SGK HΟ≥a hαΜçc 10 nΟΔng cao
BΟ†i tαΚ≠p 2 trang 134 SGK HΟ≥a hαΜçc 10 nΟΔng cao
BΟ†i tαΚ≠p 3 trang 134 SGK HΟ≥a hαΜçc 10 nΟΔng cao
BΟ†i tαΚ≠p 4 trang 134 SGK HΟ≥a hαΜçc 10 nΟΔng cao
BΟ†i tαΚ≠p 5 trang 134 SGK HΟ≥a hαΜçc 10 nΟΔng cao
4. HαΜèi ΡëΟΓp vαΜ¹ BΟ†i 24 ChΤΑΤΓng 5 HΟ≥a hαΜçc 10
Trong quΟΓ trΟ§nh hαΜçc tαΚ≠p nαΚΩu cΟ≥ bαΚΞt kΟ§ thαΚ·c mαΚ·c gΟ§, cΟΓc em hΟΘy ΡëαΜÉ lαΚΓi lαΜùi nhαΚ·n αΜü mαΜΞc HαΜèi ΡëΟΓp ΡëαΜÉ cΟΙng cαΜông ΡëαΜ™ng HΟ≥a HOC247 thαΚΘo luαΚ≠n vΟ† trαΚΘ lαΜùi nhΟ©.