Để giúp các em ôn tập lại kiến thức cũ và chuẩn bị kì thi giữa HK2 môn Hóa 12 sắp tới. Hoc247 xin giới thiệu đến các em Bộ 5 đề thi giữa HK2 môn Hóa học 12 năm 2021 có đáp án Trường THPT Lộc Thanh để các em tham khảo. Chúc các em học tập tốt và đạt kết quả cao trong kì thi này.
|
TRƯỜNG THPT LỘC THANH |
ĐỀ THI GIỮA HỌC KÌ 2 MÔN HÓA HỌC 12 THỜI GIAN 45 PHÚT |
ĐỀ SỐ 1
Câu 31. Nguyên liệu chính dùng để sản xuất nhôm là:
A. quặmg manhetit. B. quặng pirit. C. quặng đôlômit. D. quặng boxit.
Câu 32. Đem hỗn hợp X gồm Na2O và Al2O3 hòa tan hoàn toàn trong nước, thu được dung dịch Y chỉ chứa một chất tan. Sục khí CO2 đến dư vào dung dịch Y, thu được một kết tủa và dung dịch Z. Dung dịch Z có chứa
A. NaHCO3. B. Na2CO3. C. NaAlO2. D. NaOH.
Câu 33. Phương pháp thích hợp điều chế kim loại Ca từ CaCl2 là
A. nhiệt phân CaCl2.
B. điện phân dung dịch CaCl2.
C. điện phân CaCl2 nóng chảy.
D. dùng Na khử Ca2+ trong dung dịch CaCl2.
Câu 34. Cho 0,5 gam một kim loại hóa trị II phản ứng hết với dung dịch HCl dư, thu được 0,28 lít H2 (đktc). Kim loại đó là
A. Ca. B. Sr. C. Mg. D. Ba.
Câu 35. Cho dung dịch NaOH dư vào dung dịch có CuCl2, FeCl2, AlCl3. Lọc lấy kết tủa, đem nung trong không khí đến khối lượng không đổi thu được chất rắn X. Chất rắn X gồm:
A. CuO, Fe2O3 B. Fe2O3, NaCl.
C. CuO, Fe2O3, NaCl. D. CuO, FeO, Al2O3.
Câu 36. Hỗn hợp X gồm 2 kim loại kiềm và 1 kim loại kiềm thổ tan hết trong nước tạo ra dung dịch Y và 0,12 mol H2 .Thể tích dung dịch H2SO4 0,5M cần để trung hòa dung dịch Y là:
A. 240ml. B. 1,20 lít. C. 120ml. D. 60ml.
Câu 37. Natri hidrocacbonat có công thức phân tử là
A. KHCO3 B. KNO3 C. Na2CO3 D. NaHCO3
Câu 38. Kim loại có thể tạo peoxit là:
A. Fe B. Mg C. Al D. Na
Câu 39. Dãy chỉ gồm các kim loại kiềm là
A. Na, K, H, Li B. Li, Na, Be, K C. Na, K, Rb, Cs D. Li, Na, K , Ba
Câu 40. Dãy gồm các kim loại có cùng kiểu mạng tinh thể lập phương tâm khối là:
A. Na, K, Ba B. Na, K , Ca C. Li , Na, Mg D. Mg, Ca, Ba
Câu 41. Cho m gam hỗn hợp K và Ba vào nước dư thu được dung dịch X và V lít khí (đktc). Sục từ từ đến dư khí CO2 vào X, kết quả thí nghiệm được biễu diễn trên đồ thị sau:
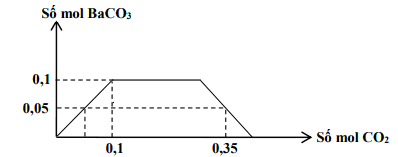
Khối lượng của K trong m gam hỗn hợp là:
A. 13,8 B. 7,8 C. 31,2 D. 11,7
Câu 42. Cho các chất rắn: Al, Al2O3, Na2O, Mg, Ca , MgO. Dãy chất nào tan hết trong dung dịch NaOH dư?
A. Al, Al2O3, Ca , MgO. B. Al, Al2O3, Na2O, Ca.
C. Al2O3, Mg, Ca , MgO. D. Al, Al2O3, Na2O, Ca , Mg.
Câu 43. Để sát trùng, tẩy uế tạp xung quanh khu vực bị ô nhiễm, người ta thường rải lên đó những chất bột màu trắng đó là chất gì ?
A. CaO B. Ca(OH)2 C. CaOCl2 D. CaCO3
Câu 44. Phương pháp điều chế kim loại phân nhóm chính nhóm II là :
A. Phương pháp thủy luyện. B. Phương pháp điện phân nóng chảy.
C. Phương pháp nhiệt luyện. D. Phương pháp điện phân dung dịch
Câu 45. Cho từ từ tới dư dung dịch chất X vào dung dịch AlCl3 thu được kết tủa keo trắng. Chất X là
A. HCl. B. NaOH. C. NH3. D. KOH.
Câu 46. Hỗn hợp X gồm Na, Ba, Na2O và BaO. Hòa tan hoàn toàn 21,9 gam X vào nước, thu được 1,12 lít khí H2 (đktc) và dung dịch Y, trong đó có 20,52 gam Ba(OH)2. Hấp thụ hoàn toàn 6,72 lít khí CO2 (đktc) vào Y, thu được m gam kết tủa. Giá trị của m là (cho Na=23, Ba=137, C=12, O=16)
A. 15,76. B. 39,40. C. 21,92. D. 23,64.
Câu 47. Chất không có tính chất lưỡng tính là:
A. Al2O3. B. NaHCO3. C. Al(OH)3. D. AlCl3.
Câu 48. Cho dung dịch Na2CO3 vào dung dịch Ca(HCO3)2 thấy
A. có bọt khí thoát ra B. có kết tủa trắng và bọt khí
C. không có hiện tượng gì D. có kết tủa trắng
Câu 49. Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo ra dung dịch có môi trường kiềm là:
A. Na,Ba,K. B. Ba,Fe,K. C. Na,Fe,K. D. Be,Na,Ca.
Câu 50. Tính chất nào sau đây không phải là của muối NaHCO3.
A. Dung dịch có môi trường axit. B. Dễ bị nhiệt phân.
C. Tác dụng với HCl . D. Tính lưỡng tính.
Câu 51. Nung mg hỗn hợp NaHCO3 và Na2CO3 đến khối lượng không đổi thì thu được 69 gam chất rắn và 11,2 lít CO2 (đktc). % khối lượng của Na2CO3 trong hỗn hợp ban đầu là
A. 84,1 B. 84,0 C. 15,9 D. 16,0
Câu 52. Dãy gồm các kim loại được xếp theo chiều tăng dần tính khử là
A. Li, Na, K, Cs B. K, Na, Li, Cs C. Cs, Na, K, Li D. Li, Na, K, Be
Câu 53. Cho phương trình hóa học của 2 phản ứng sau:
Al(OH)3 + 3H2SO4 ---> Al2(SO4)3 + 6H2O
Al(OH)3 + KOH ---> KAlO2 + 2H2O
Hai phản ứng trên chứng tỏ Al(OH)3 là chất:
A. vừa có tính oxi hóa vừa có tính khử.
B. có tính axit và tính khử.
C. có tính lưỡng tính.
D. có tính bazơ và tính khử.
Câu 54. Hòa tan hoàn toàn 8,94g hỗn hợp gồm Na, K, Ba với nước, thu được dd X và 2,688 lít khí H2 (đktc). Dung dịch Y gồm HCl và H2SO4, tỉ lệ mol tương ứng là 4:1. Trung hòa dd X bởi dd Y, tổng khối lượng các muối được tạo ra là?
A. 14,62g B. 13,7g C. 18,46g D. 12,78g
Câu 55. Chỉ dùng thêm một hóa chất hãy nhận biết các kim loại Cu, Al, Ba trong các bình mất nhãn:
A. H2O B. AgNO3 C. NaOH D. HCl
Câu 56. Cho 1,56 gam hỗn hợp gồm Al và Al2O3 phản ứng hết với dung dịch HCl (dư), thu được V lít khí H2 (đktc) và dung dịch X. Nhỏ từ từ dung dịch NH3 đến dư vào dung dịch X thu được kết tủa, lọc hết lượng kết tủa, nung đến khối lượng không đổi thu được 2,04 gam chất rắn. Giá trị của V là (cho Al=27, O=16, H=1)
A. 0,224. B. 1,344. C. 0,672. D. 0,448.
Câu 57. Cho m gam hỗn hợp Na, Ba vào nước thu được dung dịch A và 6,72 lít khí ở (đktc). Thể tích dung dịch hỗn hợp H2SO4 0,5M và HCl 1M để trung hoà vừa đủ dung dịch A là:
A. 0,1 lít. B. 0,2 lít. C. 0,4 lít. D. 0,3 lít.
Câu 58. Hòa tan hết 0,54 gam Al trong 70ml dung dịch HCl 1M thu được dung dịch X. Cho 75ml dung dịch NaOH 1M vào X, sau khi các phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Giá trị của m là (cho Al=27, O=16, H=1)
A. 1,56. B. 0,39. C. 0,78. D. 1,17.
Câu 59. Các kim loại kiềm đều có cấu trúc mạng tinh thể
A. Lục phương B. Lập phương tâm diện
C. Lập phương tâm khối D. Cả ba kiểu mạng trên
Câu 60. Kim loại Al không phản ứng với dung dịch
A. H2SO4 đặc, nóng. B. NaOH loãng. C. HNO3 đặc, nguội. D. H2SO4 loãng.
Câu 61. Kim loại không phản ứng được với nước ở nhiệt độ thường là
A. Li B. Ca C. K D. Be
Câu 62. Hòa tan hoàn toàn m gam Al bằng dung dịch HNO3 loãng, thu được 5,376 lít (đktc) hỗn hợp khí X gồm N2, N2O và dung dịch chứa 8m gam muối. Tỉ khối của X so với H2 bằng 18. Giá trị của m là (cho Al=27, O=16, H=, N=14)
A. 19,44. B. 21,60. C. 17,28. D. 18,90.
ĐÁP ÁN ĐỀ SỐ 1
|
31 |
D |
39 |
C |
47 |
D |
55 |
A |
|
32 |
A |
40 |
A |
48 |
D |
56 |
C |
|
33 |
C |
41 |
B |
49 |
A |
57 |
D |
|
34 |
A |
42 |
B |
50 |
A |
58 |
D |
|
35 |
A |
43 |
C |
51 |
D |
59 |
C |
|
36 |
A |
44 |
B |
52 |
A |
60 |
C |
|
37 |
D |
45 |
C |
53 |
C |
61 |
D |
|
38 |
D |
46 |
A |
54 |
C |
62 |
B |
ĐỀ SỐ 2
Câu 41. Dẫn mẫu khí thải của một nhà máy qua dung dịch Pb(NO3)2 dư, thấy xuất hiện kết tủa màu đen. Hiện tượng đó chứng tỏ trong khí thải nhà máy có chứa khí nào sau đây?
A. NH3. B. CO2. C. SO2. D. H2S.
Câu 42. Hợp chất hữu cơ tham gia phản ứng tráng gương là
A. CH3COOH. B. CH3COOCH3. C. C2H5OH. D. CH3CHO.
Câu 43. Chất NH2CH2COOH có tên gọi là
A. Glyxin. B. Valin. C. Alanin. D. Lysin.
Câu 44. Cho sơ đồ phản ứng: KHCO3 + X → K2CO3 + H2O. X là hợp chất
A. K2CO3. B. NaOH. C. KOH. D. HCl.
Câu 45. Polime nào sau đây trong thành phần nguyên tố chứa nitơ?
A. Cao su buna. B. Poli(vinyl clorua).
C. Tơ nilon-7. D. Polietilen.
Câu 46. Chất nào sau đây không tham gia phản ứng thủy phân?
A. Xenlulozơ. B. Fructozơ. C. Chất béo. D. Saccarozơ.
Câu 47. Cho 5,4 gam Al tác dụng với 100 ml dung dịch NaOH 1M đến khi phản ứng xảy ra hoàn toàn, thu được V lít khí H2 (đktc). Giá trị của V là
A. 4,48. B. 2,24. C. 3,36. D. 6,72
Câu 48. Chất nào sau đây có tính lưỡng tính?
A. Al. B. Fe(OH)2. C. NaHCO3. D. KOH.
Câu 49. Hiđrocacbon nào dưới đây không làm mất màu nước brom?
A. Butađien. B. Etilen. C. Axetilen. D. Toluen.
Câu 50. Chất nào sau đây là chất điện li mạnh?
A. CaSO4. B. C12H22O11. C. H2O. D. NaNO3.
Câu 51. Kim loại nào sau đây không tan được trong dung dịch HCl?
A. Ag. B. Zn. C. Al. D. Fe.
Câu 52. Nhúng thanh kim loại X vào dung dịch muối CuSO4, sau một thời gian lấy thanh kim loại ra cân lại, thấy khối lượng thanh kim loại giảm m gam. Kim loại X là
A. Al. B. Zn. C. Mg. D. Fe.
Câu 53. Kim loại Fe không tác dụng với dung dịch nào đây?
A. Fe(NO3)3. B. Fe(NO3)2. C. AgNO3. D. Cu(NO3)2.
Câu 54. Metyl fomat có công thức là
A. HCOOCH3. B. CH3COOC2H5. C. HCOOC2H5. D. CH3COOCH3.
Câu 55. Trong công nghiệp, Na được điều chế bằng cách điện phân nóng chảy hợp chất nào?
A. NaCl. B. NaOH. C. NaNO3. D. NaHCO3.
---(Nội dung chi tiết từ câu 56 đến câu 80 của đề thi số 2 vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 2
|
41 |
D |
51 |
A |
61 |
A |
71 |
C |
|
42 |
D |
52 |
B |
62 |
B |
72 |
B |
|
43 |
A |
53 |
B |
63 |
C |
73 |
A |
|
44 |
C |
54 |
A |
64 |
D |
74 |
A |
|
45 |
C |
55 |
A |
65 |
A |
75 |
C |
|
46 |
B |
56 |
D |
66 |
B |
76 |
D |
|
47 |
D |
57 |
D |
67 |
C |
77 |
B |
|
48 |
C |
58 |
B |
68 |
A |
78 |
B |
|
49 |
D |
59 |
C |
69 |
B |
79 |
C |
|
50 |
D |
60 |
D |
70 |
D |
80 |
C |
ĐỀ SỐ 3
Câu 31. Đốt cháy hoàn toàn 17,4 gam hỗn hợp Mg và Al trong khí oxi (dư) thu được 30,2 gam hỗn hợp oxit. Thể tích khí oxi (đktc) đã tham gia phản ứng là:
A. 17,92 lít. B. 4,48 lít. C. 11,20 lít. D. 8,96 lít.
Câu 32. Nhiệt phân hoàn toàn 50,0 gam CaCO3 thu được V lít khí CO2 (đktc). Giá trị của V là
A. 33,6. B. 5,6. C. 11,2. D. 22,4.
Câu 33. Trường hợp nào dưới đây tạo ra kết tủa sau khi phản ứng xảy ra hoàn toàn ?
A. Thêm dư AlCl3 vào dung dịch NaOH. B. Thêm dư HCl vào dung dịch NaAlO2.
C. Thêm dư NaOH vào dung dịch AlCl3. D. Thêm dư CO2 vào dung dịch NaOH.
Câu 34. Cho hỗn hợp gồm Na và Al có tỉ lệ số mol tương ứng là 1 : 2 vào nước (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (ở đktc) và m gam chất rắn không tan. Giá trị của m là (cho Na=23, Al=27)
A. 5,4. B. 7,8. C. 10,8. D. 43,2.
Câu 35. Kim loại có thể tạo peoxit là:
A. Mg B. Na C. Fe D. Al
Câu 36. Phèn chua được dùng để làm trong nước đục. Công thức của phèn chua là
A. (NH4)2SO4.Al2(SO4)3.24H2O. B. K2SO4.Cr2(SO4)3.24H2O.
C. KAl(SO4)2.12H2O. D. NH4Fe(SO4)2.12H2O.
Câu 37. Cho mẩu Al vào dung dịch NaOH dư thu được dung dịch X. Trong dung dịch X có các chất tan là ?
A. NaAlO2, NaOH, H2O. B. NaOH, H2O.
C. NaAlO2, H2O. D. NaAlO2, NaOH.
Câu 38. Nguyên tố có năng lượng ion hóa nhỏ nhất là:
A. Li B. K C. Na D. Cs
Câu 39. Dãy gồm các kim loại được điều chế trong công nghiệp bằng phương pháp điện phân hợp chất nóng chảy của chúng là:
A. Fe, Ca, Al. B. Na, Ca, Zn. C. Na, Ca, Al. D. Na, Cu, Al.
Câu 40. Hỗn hợp X gồm Al, Ca, Al4C3 và CaC2. Cho 40,3 gam X vào H2O dư, chỉ thu được dung dịch Y và hỗn hợp khí Z (C2H2, CH4, H2). Đốt cháy Z thu được 20,16 lít khí CO2 (đktc) và 20,7 gam H2O. Nhỏ từ từ V lít dung dịch HCl xM vào Y, được kết quả biểu diễn theo hình vẽ dưới:
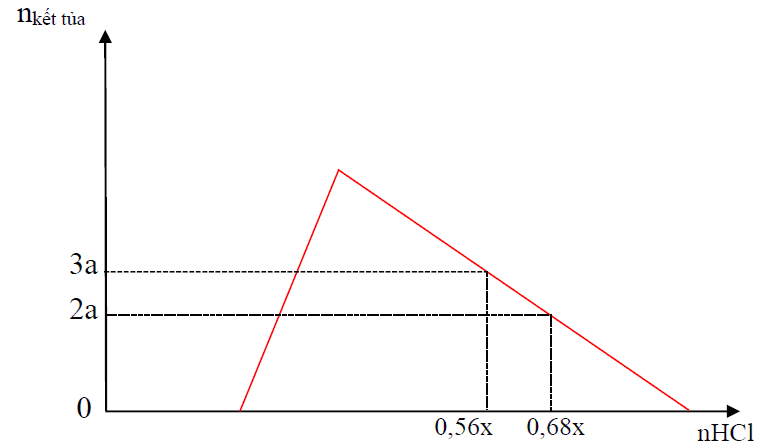
Nếu nhỏ từ từ 100ml dung dịch HCl xM đến hết vào 100ml dd chứa Na2CO31M và NaHCO3 1M, sau phản ứng thu được số mol CO2 là?
A. 0,1 B. 0,25 C. 0,2 D. 0,15
---(Nội dung chi tiết từ câu 41 đến câu 62 của đề thi số 3 vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 3
|
31 |
D |
39 |
C |
47 |
D |
55 |
A |
|
32 |
C |
40 |
D |
48 |
C |
56 |
A |
|
33 |
A |
41 |
D |
49 |
C |
57 |
A |
|
34 |
A |
42 |
C |
50 |
B |
58 |
D |
|
35 |
B |
43 |
C |
51 |
A |
59 |
C |
|
36 |
C |
44 |
A |
52 |
A |
60 |
B |
|
37 |
D |
45 |
D |
53 |
B |
61 |
B |
|
38 |
D |
46 |
D |
54 |
C |
62 |
B |
ĐỀ SỐ 4
Câu 41. Dẫn mẫu khí thải của một nhà máy qua dung dịch Pb(NO3)2 dư, thấy xuất hiện kết tủa màu đen. Hiện tượng đó chứng tỏ trong khí thải nhà máy có chứa khí nào sau đây?
A. NH3. B. H2S. C. SO2. D. CO2.
Câu 42. Chất nào sau đây có tính lưỡng tính?
A. Al. B. KOH. C. NaHCO3. D. Fe(OH)2.
Câu 43. Chất nào sau đây tác dụng với dung dịch HCl giải phóng khí CO2?
A. Fe2O3. B. FeCO3. C. Fe(OH)2. D. Fe.
Câu 44. Công thức hóa học của kali hiđroxit là
A. NaOH. B. KCl. C. KOH. D. KHCO3.
Câu 45. Trong công nghiệp, Na được điều chế bằng cách điện phân nóng chảy hợp chất nào?
A. NaNO3. B. NaCl. C. NaHCO3. D. NaOH.
Câu 46. Hiđrocacbon nào dưới đây không làm mất màu nước brom?
A. Toluen. B. Axetilen. C. Butađien. D. Etilen.
Câu 47. Cho 5,4 gam Al tác dụng với 100 ml dung dịch NaOH 1M đến khi phản ứng xảy ra hoàn toàn, thu được V lít khí H2 (đktc). Giá trị của V là
A. 6,72 B. 4,48. C. 3,36. D. 2,24.
Câu 48. Metyl fomat có công thức là
A. CH3COOCH3. B. HCOOC2H5. C. CH3COOC2H5. D. HCOOCH3.
Câu 49. Kim loại sắt tác dụng với dung dịch nào sau đây tạo ra muối sắt(II)?
A. HNO3 đặc, nóng, dư. B. MgSO4.
C. H2SO4 đặc, nóng, dư D. CuSO4.
Câu 50. Phèn chua là muối sunfat kép của nhôm và kim loại kiềm ngậm nước. Công thức của kim loại kiềm trong phèn chua là
A. K. B. Rb. C. Li. D. Na.
---(Nội dung chi tiết từ câu 51 đến câu 80 của đề thi số 4 vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 4
|
41 |
B |
51 |
C |
61 |
D |
71 |
D |
|
42 |
C |
52 |
A |
62 |
A |
72 |
B |
|
43 |
B |
53 |
B |
63 |
B |
73 |
B |
|
44 |
C |
54 |
D |
64 |
C |
74 |
A |
|
45 |
B |
55 |
D |
65 |
D |
75 |
D |
|
46 |
A |
56 |
C |
66 |
D |
76 |
B |
|
47 |
A |
57 |
B |
67 |
A |
77 |
C |
|
48 |
D |
58 |
C |
68 |
C |
78 |
C |
|
49 |
D |
59 |
C |
69 |
C |
79 |
A |
|
50 |
A |
60 |
D |
70 |
B |
80 |
A |
ĐỀ SỐ 5
Câu 31. Dãy gồm các kim loại có cùng kiểu mạng tinh thể lập phương tâm khối là:
A. Mg, Ca, Ba B. Na, K, Ba C. Li , Na, Mg D. Na, K , Ca
Câu 32. Cho m gam hỗn hợp K và Ba vào nước dư thu được dung dịch X và V lít khí (đktc). Sục từ từ đến dư khí CO2 vào X, kết quả thí nghiệm được biễu diễn trên đồ thị sau:
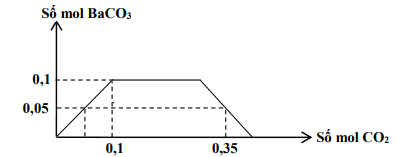
Khối lượng của K trong m gam hỗn hợp là:
A. 13,8 B. 31,2 C. 11,7 D. 7,8
Câu 33. Nguyên liệu chính dùng để sản xuất nhôm là:
A. quặng đôlômit. B. quặng pirit. C. quặng boxit. D. quặmg manhetit.
Câu 34. Dãy gồm các kim loại được xếp theo chiều tăng dần tính khử là
A. Li, Na, K, Be B. K, Na, Li, Cs C. Cs, Na, K, Li D. Li, Na, K, Cs
Câu 35. Kim loại có thể tạo peoxit là:
A. Fe B. Mg C. Al D. Na
Câu 36. Natri hidrocacbonat có công thức phân tử là
A. KHCO3 B. Na2CO3 C. NaHCO3 D. KNO3
Câu 37. Hỗn hợp X gồm 2 kim loại kiềm và 1 kim loại kiềm thổ tan hết trong nước tạo ra dung dịch Y và 0,12 mol H2 .Thể tích dung dịch H2SO4 0,5M cần để trung hòa dung dịch Y là:
A. 1,20 lít. B. 240ml. C. 60ml. D. 120ml.
Câu 38. Cho từ từ tới dư dung dịch chất X vào dung dịch AlCl3 thu được kết tủa keo trắng. Chất X là
A. KOH. B. NH3. C. NaOH. D. HCl.
Câu 39. Cho m gam hỗn hợp Na, Ba vào nước thu được dung dịch A và 6,72 lít khí ở (đktc). Thể tích dung dịch hỗn hợp H2SO4 0,5M và HCl 1M để trung hoà vừa đủ dung dịch A là:
A. 0,3 lít. B. 0,4 lít. C. 0,2 lít. D. 0,1 lít.
Câu 40. Kim loại không phản ứng được với nước ở nhiệt độ thường là
A. Ca B. Li C. K D. Be
---(Nội dung chi tiết từ câu 41 đến câu 62 của đề thi số 5 vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 5
|
31 |
B |
39 |
A |
47 |
B |
55 |
A |
|
32 |
D |
40 |
D |
48 |
A |
56 |
C |
|
33 |
C |
41 |
A |
49 |
B |
57 |
A |
|
34 |
D |
42 |
C |
50 |
A |
58 |
B |
|
35 |
D |
43 |
D |
51 |
C |
59 |
C |
|
36 |
C |
44 |
A |
52 |
C |
60 |
A |
|
37 |
B |
45 |
B |
53 |
A |
61 |
A |
|
38 |
B |
46 |
C |
54 |
C |
62 |
D |
Trên đây là một phần trích dẫn nội dung Bộ 5 đề thi giữa HK2 môn Hóa học 12 năm 2021 có đáp án Trường THPT Lộc Thanh. Để xem toàn bộ nội dung các em đăng nhập vào trang hoc247.net để tải tài liệu về máy tính.
Hy vọng tài liệu này sẽ giúp các em học sinh ôn tập tốt và đạt thành tích cao trong học tập.
Ngoài ra các em có thể tham khảo thêm một số tư liệu cùng chuyên mục tại đây:
- Bộ 5 đề thi giữa HK2 môn Hóa học 12 năm 2021 có đáp án Trường THPT Nguyễn Huệ
- Bộ 5 đề thi giữa HK2 môn Hóa học 12 năm 2021 có đáp án Trường THPT Y Đôn
Chúc các em học tốt!
Tư liệu nổi bật tuần
-
Đề thi minh họa môn Hóa học tốt nghiệp THPT năm 2025
22/10/20242103 -
Đề thi minh họa môn Tin học tốt nghiệp THPT năm 2025
22/10/2024771 -
Đề thi minh họa môn Toán tốt nghiệp THPT năm 2025
22/10/20241496 - Xem thêm
ERROR:connection to 10.20.1.101:9312 failed (errno=111, msg=Connection refused)
ERROR:connection to 10.20.1.101:9312 failed (errno=111, msg=Connection refused)




