Nếu các em có những khó khăn nào về Hóa học 10 Bài 39 Tốc độ phản ứng và Cân bằng hóa học các em vui lòng đặt câu hỏi để được giải đáp. Các em có thể đặt câu hỏi nằm trong phần bài tập SGK, bài tập nâng cao, cộng đồng Hóa HỌC247 sẽ sớm giải đáp cho các em.
Danh sách hỏi đáp (234 câu):
-
Cho phản ứng: H2 (k) + I2 (k) ⇄ 2HI (k). Ở nhiệt độ 4300C, hằng số cân bằng KC của phản ứng trên bằng 53,96. Đun nóng một bình kín dung tích không đổi 10 lít chứa 4,0 gam H2 và 406,4 gam I2. Khi hệ phản ứng đạt trạng thái cân bằng ở 4300C, nồng độ của HI là?
10/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Trong một bình kín có chứa 10 lít nitơ và 10 lít hiđro ở nhiệt độ 00C và áp suất 10 atm. Sau phản ứng tổng hợp amoniac, đưa nhiệt độ bình về 00C. Có 60% hiđro tham gia phản ứng thì áp suất trong bình sau phản ứng là?
10/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Một bình kín có dung tích không đổi, chứa hỗn hợp khí N2 và H2 với nồng độ tương ứng là 0,3M và 0,7M. Sau khi phản ứng tổng hợp NH3 đạt trạng thái cân bằng ở t0C, H2 chiếm 50% thể tích hỗn hợp thu được. Hằng số cân bằng KC ở t0C của phản ứng có giá trị là?
11/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Cho phản ứng : N2 (k) + 3H2 (k) ⇄ 2NH3 (k); ∆H = -92 kJ. Hai biện pháp đều làm cân bằng chuyển dịch theo chiều thuận là?
10/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -

Cho vào bình kính dung tích không đổi hai chất khí H2 và N2 với chất xúc tác thích hợp ở nhiệt độ t. Áp suất ban đầu trong bình là P1. Giữ nguyên nhiệt độ t một thời gian cho đến hệ thống đạt cân bằng thì áp suất của hệ là P2. So sánh độ lớn của P1 và P2?
11/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Theo dõi (0)Gửi câu trả lời Hủy
-
Nén 1 mol N2 và 4 mol H2 vào bình kín có thể tích 0,5 lít (chứa sẵn chất xt) và giữ cho t0 không đổi. Khi phản ứng trong bình đạt đến trạng thái cân bằng áp suất các khí trong bình bằng 0,8 lần áp suất lúc đầu. Tính hằng số cân bằng?
11/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Cho cân bằng: C(r) + CO2(k) \(\leftrightarrow\) 2CO(k). Ở 550oC, hằng số cân bằng KC của phản ứng trên bằng 2.10-3. Người ta cho 0,2 mol C và 1 mol CO2 vào bình kín dung tích 22,4 lít (không chứa không khí). Nâng dần nhiệt độ trong bình lên đến 550oC và giữ nhiệt độ đó để cho cân bằng được thiết lập. Số mol CO trong bình là?
11/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Cho cân bằng hóa học sau: 2SO2 (k) + O2 (k) ⇄ 2SO3 (k); ∆H Cho các biện pháp: (1) tăng nhiệt độ, (2) tăng áp suất chung của hệ phản ứng, (3) hạ nhiệt độ, (4) dùng thêm chất xúc tác V2O5, (5) giảm nồng độ SO3, (6) giảm áp suất chung của hệ phản ứng. Những biện pháp nào làm cân bằng trên chuyển dịch theo chiều thuận?
10/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Cho các cân bằng hóa học sau: (1) 2HI (k) \(\rightleftharpoons\) H2 (k) + I2 (k) (2) CaCO3 (r) \(\rightleftharpoons\) CaO (r) + CO2 (k) (3) FeO (r) + CO (k) \(\rightleftharpoons\) Fe (r) + CO2 (k) (4) 2SO2 (k) + O2 (k) \(\rightleftharpoons\) 2SO3 (k) Khi tăng áp suất của hệ, số cân bằng bị chuyển dịch theo chiều thuận là?
10/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Xét phân hủy N2O5 trong dung môi CCl4 ở 450C: N2O5 → N2O4 + \(\frac{1}{2}\)O2. Ban đầu nồng độ của N2O5 là 2,33M, sau 184 giây nồng độ của N2O5 là 2,08M. Tốc độ trung bình của phản ứng tính theo N2O5 là?
10/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Thực hiện phản ứng este hoá 2 mol C2H5OH với 1 mol HCOOH ở nhiệt độ không đổi (xúc tác H2SO4 đặc) khi hệ cân bằng thu đuợc 0,8 mol este, ở cùng điều kiện trên, este hoá 1 mol C2H5OH và X mol HCOOH, khi hệ cân bằng thu đuợc 0,7 mol este. Giá trị của X là?
10/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Cho phản ứng: \(Na_{2}S_{2}O_{3} (l) + H_{2}SO_{4} (l) \xrightarrow[]{\ \ \ \ \ \ }Na_{2}SO_{4} (l) + SO_{2} (k) + S (r) + H_{2}O (l).\) Khi thay đổi một trong các yếu tố: (1) tăng nhiệt độ; (2) tăng nồng độ Na2S2O3; (3) giảm nồng độ H2SO4; (4) giảm nồng độ Na2SO4; (5) giảm áp suất của SO2; (6) dùng chất xúc tác; có bao nhiêu yếu tố làm tăng tốc độ của phản ứng đã cho?
10/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Cho cân bằng hóa học sau: N2 + 3H2 ⇄ 2NH3 ∆H = -92kJ Tác động làm cân bằng chuyển dịch theo chiều thuận là?
11/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Cho phương trình hóa học của phản ứng: X + 2Y Z + T. Ở thời điểm ban đầu, nồng độ của chất X là 0,01 mol/l. Sau 20 giây, nồng độ của chất X là 0,008 mol/l. Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên là?
10/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Cho các cân bằng sau trong các bình riêng biệt: H2 (k, không màu) + I2 (k, tím) ⇄ 2HI (k, không màu) (1) 2NO2 (k, nâu đỏ) ⇄ N2O4 (k, không màu) (2) Nếu làm giảm thể tích bình chứa của cả 2 hệ trên, so với ban đầu thì màu của?
10/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Trong công ngiệp, sản xuất NH3, phản ứng xảy ra tạo thành một cân bằng hóa học. Cân bằng hóa học này phải thực hiện ở áp suất cao, nhiệt độ thấp nhưng không quá thấp (khoảng 4500C). Từ đó suy ra đặc điểm của phản ứng là gì?
10/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Thực hiện thí nghiệm hòa tan đá vôi (CaCO3) bằng dung dịch HCl, biện pháp nào sau đây có thể làm tăng tốc độ phản ứng?
10/03/2022 | 1 Trả lời
A. Tăng thể tích của dung dịch HCl
B. Giảm nồng độ của dung dịch HCl
C. Hạ nhiệt độ xuống
D. Nghiền nhỏ đá vôi
Theo dõi (0)Gửi câu trả lời Hủy -
Trong số các yếu tố sau: nồng độ, nhiệt độ, áp suất, diện tích tiếp xúc và chất xúc tác. Có nhiều nhất bao nhiêu yếu tố có thể ảnh hưởng tới một cân bằng hóa học?
10/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Cho phương trình hóa học của phản ứng : X + 2Y → Z + T. Ở thời điểm ban đầu, nồng độ của chất X là 0,2 mol/l. Sau 40s, nồng độ của chất X là 0,04 mol/l. Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên là?
11/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Một phản ứng thuận nghịch ở trạng thái cân bằng thì tốc độ phản ứng thuận (vt) bằng tốc độ phản ứng nghịch (vn). Khi thay đổi các yếu tố nồng độ, áp suất, nhiệt độ… thì có thể xẩy ra các trường hợp sau:
11/03/2022 | 1 Trả lời
1. vt tăng, vn giảm
2. vt và vn đều giảm nhưng vn giảm nhiều hơn vt
3. vt và vn đều tăng nhưng vn tăng nhiều hơn vt
4. vn tăng, vt không đổi
5. vn và vt đều không đổi
Trong số các trường hợp trên, có bao nhiêu trường hợp làm cân bằng dịch chuyển theo chiều thuận?
Theo dõi (0)Gửi câu trả lời Hủy -
Cho cân bằng hóa học (trong bình kín) sau: N2(khí) + 3H2(khí) \(\leftrightarrow\) 2NH3 (ΔH= -92kJ/mol) Trong các yếu tố: (1) Thêm một lượng N2 hoặc H2. (2) Thêm một lượng NH3. (3) Tăng nhiệt độ của phản ứng. (4) Tăng áp suất của phản ứng. (5) Dùng thêm chất xuc tác. Có bao nhiêu yếu tố làm cho tỉ khối của hỗn hợp khí trong bình so với H2 tăng lên?
11/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Cho cân bằng: 2A(k) + B(k) \(\leftrightarrow\) C(k) biết rằng ở 1500C và 2000C, tỉ khối hơi của hỗn hợp khí so với H2 lần lượt là d1 và d2, biết d21. Nhận xét nào sau đây đúng:
10/03/2022 | 1 Trả lời
A. Cân bằng chuyển dịch theo chiều nghịch khi tăng áp suất
B. Tăng nồng độ chất B, cân bằng chuyển dịch theo chiều nghịch
C. Phản ứng thuận thu nhiệt
D. Phản ứng thuận tỏa nhiệt
Theo dõi (0)Gửi câu trả lời Hủy -
Xét phản ứng hoá học: A(khí) + 2B(khí) → C(khí) + D(khí). Tốc độ của phản ứng được tính theo biểu thức: \(v{\rm{ }} = {\rm{ }}k\left[ A \right].{\left[ B \right]^2}\), trong đó k là hằng số tốc độ phản ứng; [A] và [B] nồng độ mol/lít của các chất A, B tương ứng. Khi nồng độ của chất B tăng 3 lần, nồng độ của chất A giảm 6 lần thì tốc độ phản ứng so với trước là:
11/03/2022 | 1 Trả lời
Theo dõi (0)Gửi câu trả lời Hủy -
Cho các phản ứng sau, khi giảm nhiệt độ hoặc tăng áp suất các cân bằng nào trên đây đều chuyển dịch theo chiều thuận?
11/03/2022 | 1 Trả lời
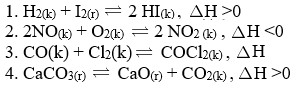 Theo dõi (0)Gửi câu trả lời Hủy
Theo dõi (0)Gửi câu trả lời Hủy



