Giải bài 5.16 trang 16 SBT Hóa học 10 Cánh Diều
Tại một khu vực của Úc, gia súc không phát triển mạnh mặc dù có thức ăn thô xanh thích hợp. Một cuộc điều tra cho thấy nguyên nhân là do không có đủ cobalt trong đất. Cobalt tạo thành cation ở hai dạng là Co2+ và Co3+ (Z = 27). Viết cấu hình electron của hai cation này và sơ đồ phân bố các electron vào các ô orbital. Cho biết số electron độc thân trong mỗi ion.
Hướng dẫn giải chi tiết bài 5.16
Phương pháp giải:
B1: Xác định số e của ion O2- và Al3+
B2: Viết cấu hình e của các ion đó theo quy tắc Hund và nguyên lí vững bền
B3: Xác định các phân lớp và biểu diễn AO theo quy tắc: mỗi AO chứa tối đa 2 e
B4: Xác định số e độc thân (e độc thân là e đứng 1 mình trong AO, không ghép cặp với e khác)
Lời giải chi tiết:
Co có Z = 27 nên có cấu hình electron là: 1s22s22p63s23p63d74s2 hoặc [Ar]3d74s2
Khi Co mất đi 2 electron và 3 electron sẽ lần lượt tạo ra: Co2+ và Co3+. Cấu hình electron của hai ion này là:
Co2+: 1s22s22p63s23p63d7
Co3+: 1s22s22p63s23p63d6
Sơ đồ phân bố electron vào các ô orbital:
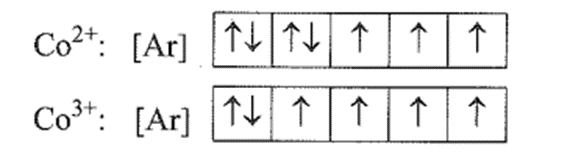
Số electron độc thân trong Co2+ và Co3+ lần lượt là 3 và 4.
-- Mod Hóa Học 10 HỌC247
Bài tập SGK khác
Chưa có câu hỏi nào. Em hãy trở thành người đầu tiên đặt câu hỏi.





