Bài tập 8 trang 61 SGK Hóa học 10 nâng cao
Hai nguyên tố A, B đứng kế tiếp nhau trong một chu kì của bảng tuần hoàn có tổng số đơn vị điện tích hạt nhân là 25.
a) Viết cấu hình electron để xác định hai nguyên tố A và B thuộc chu kì nào, nhóm nào.
b) So sánh tính chất hóa học của chúng.
Hướng dẫn giải chi tiết bài 8
a) Gọi số điện tích hạt nhân của nguyên tố A là ZA, số điện tích hạt nhân của nguyên tố B là ZB. Theo đề bài ta có
ZA - ZB = 1 và ZA + ZB = 25
Suy ra: ZA = 13 (Al) và ZB = 12 (Mg)
b) Cấu hình electron của Al: 1s22s22p63s23p1. Al thuộc chu kì 3, nhóm IIIA
Cấu hình electron của Mg: 1s22s22p63s2. Mg thuộc chu kì 3, nhóm IIA
c) Al và Mg thuộc cùng chu kì. Theo quy luật, Mg có tính kim loại mạnh hơn Al
-- Mod Hóa Học 10 HỌC247
Bài tập SGK khác
-


Xác định tên kim loại?
bởi Quynh Ni
 26/11/2019
26/11/2019
 Theo dõi (0) 0 Trả lời
Theo dõi (0) 0 Trả lời -


Oxit đã cho là gì?
bởi NT Huỳnh Hân
 21/11/2019
Một oxit có công thức X2O có tổng số hạt proton notron electron của phân tử là 92 trong đó số hạt mang điện nhiều hơn số hạt ko mang điện là 28. Oxit đã cho là gìTheo dõi (0) 1 Trả lời
21/11/2019
Một oxit có công thức X2O có tổng số hạt proton notron electron của phân tử là 92 trong đó số hạt mang điện nhiều hơn số hạt ko mang điện là 28. Oxit đã cho là gìTheo dõi (0) 1 Trả lời -


Cho 3,2g hỗn hợp 1 kim loại kiềm thổ và oxit của nó tác dụng HCl dư thu 9,5g muối. Xác định tên kim loại?
bởi Isave Hạnh
 16/11/2019
Giúp mình câu này vớiTheo dõi (0) 0 Trả lời
16/11/2019
Giúp mình câu này vớiTheo dõi (0) 0 Trả lời -


Xác định kim loại M?
bởi Ngọc Trần Bảo
 12/11/2019
Giúp mình vớiTheo dõi (0) 0 Trả lời
12/11/2019
Giúp mình vớiTheo dõi (0) 0 Trả lời -
ADMICRO

 X có tổng số hạt là 24 và thuộc nhóm VIA tính số khối nguyên tố XTheo dõi (0) 1 Trả lời
X có tổng số hạt là 24 và thuộc nhóm VIA tính số khối nguyên tố XTheo dõi (0) 1 Trả lời -


Số sau sắp xếp các nguyên tố C, S, N, P, O, H, Cl theo chiều tăng dần tính phi kim?
bởi Nguyễn Oanh
 10/11/2019
Số sau sắp xếp các nguyên tố sau các bon lưu huỳnh Nitơ Photpho oxi hidro Clo theo chiều tăng dần tính phi kimTheo dõi (0) 2 Trả lời
10/11/2019
Số sau sắp xếp các nguyên tố sau các bon lưu huỳnh Nitơ Photpho oxi hidro Clo theo chiều tăng dần tính phi kimTheo dõi (0) 2 Trả lời -


Tính nồng độ phần trăm dung dịch Y?
bởi Nek Văn
 09/11/2019
09/11/2019
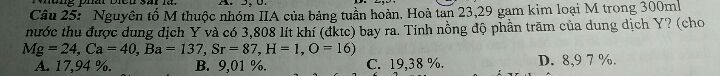 Theo dõi (0) 3 Trả lời
Theo dõi (0) 3 Trả lời -


Xác định chất khí thu được sau phản ứng?
bởi Trang Títt
 07/11/2019
Cho 32.5 g Zn tan vừa đủ trong 200 ml dung dịch HNO3 6M thu được khí X duy nhất. X là?Theo dõi (0) 2 Trả lời
07/11/2019
Cho 32.5 g Zn tan vừa đủ trong 200 ml dung dịch HNO3 6M thu được khí X duy nhất. X là?Theo dõi (0) 2 Trả lời -


Xác định cấu hionhf electron của nguyên tố S và Ca?
bởi Chi Cao
 07/11/2019
07/11/2019
 Theo dõi (0) 1 Trả lời
Theo dõi (0) 1 Trả lời -


Tính % khối lượng mỗi kim loại trong hỗn hợp?
bởi Nguyễn Mạnh Dũng
 05/11/2019
05/11/2019
cho 4,6 g 1 kim loại M thuộc nhóm 1a vào 200g H2O thu được 22 X và 2.24 H2 đktc
a) xác định M
b) xác định C% dung dịch X
c) cho 1.5 g là 2 kim loại kiềm X, M vào dung dịch Hcl từ sau phản ứng thu đc 1.12 lít H2O đktc
xác định 2 kim loại kiềm , % khối lượng mỗi kim loại trong hỗn hợpTheo dõi (0) 0 Trả lời -


Xác định tên hai kim loại tham gia phản ứng?
bởi Thanh Hoang
 04/11/2019
Giúp mk B4,5 vs
04/11/2019
Giúp mk B4,5 vs Theo dõi (0) 0 Trả lời
Theo dõi (0) 0 Trả lời -


A,B là 2 nguyên tố thuộc cùng 1 phân nhóm và thuộc 2 chu kỳ liên tiếp, tổng số proton trong hạt nhân 2 nguyên tử là 30 . A , B là nguyên tố nào
bởi Nguyễn Danh
 03/11/2019
03/11/2019
 Theo dõi (0) 2 Trả lời
Theo dõi (0) 2 Trả lời -


Tìm giá trị của m để V lớn nhất?
bởi Trần Thư
 03/11/2019
Hợp chất khí của R với hidro có dạng RH. Trong oxit cao nhất có chứa 41.176% oxi về khối lượng.a. Tìm tên nguyên tố R b, cho m gam Na tác dụng với 100g dd RH 8.1% thu được V (l) H2. Tìm giá trị của m để V lớn nhất.Theo dõi (0) 1 Trả lời
03/11/2019
Hợp chất khí của R với hidro có dạng RH. Trong oxit cao nhất có chứa 41.176% oxi về khối lượng.a. Tìm tên nguyên tố R b, cho m gam Na tác dụng với 100g dd RH 8.1% thu được V (l) H2. Tìm giá trị của m để V lớn nhất.Theo dõi (0) 1 Trả lời -


Xác định R?
bởi Thoại Dương Thị Kim
 28/10/2019
Hoà tận hoàn toàn 15,76g một kim loại R thuộc nhóm IIA vào cốc chứa m gam dd HCl 7.3%. Kết thúc phản ứng thấy khối lượng dd thu đc là (m 15.6)g. Biết khối lượng HCl phản ứng bằng 20% HLC ban đầu . Xác định RTheo dõi (0) 0 Trả lời
28/10/2019
Hoà tận hoàn toàn 15,76g một kim loại R thuộc nhóm IIA vào cốc chứa m gam dd HCl 7.3%. Kết thúc phản ứng thấy khối lượng dd thu đc là (m 15.6)g. Biết khối lượng HCl phản ứng bằng 20% HLC ban đầu . Xác định RTheo dõi (0) 0 Trả lời -


Thể tích clo(đkc)cần dùng là?
bởi Oanh Kiều
 27/10/2019
Cho 0.02g hỗn hợp 2 kim loại kali và natri tác dụng vừa đủ với clo,thu được 4.15g muối clorua.Thể tích clo(đkc)cần dùng làTheo dõi (0) 0 Trả lời
27/10/2019
Cho 0.02g hỗn hợp 2 kim loại kali và natri tác dụng vừa đủ với clo,thu được 4.15g muối clorua.Thể tích clo(đkc)cần dùng làTheo dõi (0) 0 Trả lời -

 Caâu 2: Cho 3,1 gam hỗn hợp 2 kim loại kiềm ở hai chu kì liên tiếp tác dụng hết với nước, ta thu được 1,12 lít khí ở dktc. Xác định 2 kim loại và % theo khối lượng của chúng trong hh?Theo dõi (0) 0 Trả lời
Caâu 2: Cho 3,1 gam hỗn hợp 2 kim loại kiềm ở hai chu kì liên tiếp tác dụng hết với nước, ta thu được 1,12 lít khí ở dktc. Xác định 2 kim loại và % theo khối lượng của chúng trong hh?Theo dõi (0) 0 Trả lời




