Dưới đây là Bộ đề thi chọn HSG môn Hóa học 12 năm 2021 có đáp án Trường THPT Thái Phiên. Đề thi gồm có các câu tự luận sẽ giúp các bạn ôn tập nắm vững các kiến thức, các dạng bài tập để chuẩn bị cho kỳ thi sắp đến. Các bạn xem và tải về ở dưới.
|
TRƯỜNG THPT THÁI PHIÊN |
ĐỀ THI CHỌN HỌC SINH GIỎI MÔN HÓA HỌC 12 NĂM HỌC 2020-2021 |
ĐỀ SỐ 1
Câu 1. (4,0 điểm)
1. Nêu hiện tượng và viết phương trình phản ứng xảy ra dạng ion trong các thí nghiệm sau:
a) Cho từ từ đến dư dung dịch KHSO4 vào dung dịch chứa NaAlO2 và Na2CO3.
b) Cho dung dịch H2SO4 loãng vào dung dịch Fe(NO3)2.
c) Cho Fe3O4 tác dụng với dung dịch HI dư.
d) Sục khí CO2 đến dư vào dung dịch Ca(OH)2.
2. Hợp chất khí của nguyên tố R với hiđro có dạng H2R. Trong oxit cao nhất, R chiếm 40% về khối lượng. Ở trạng thái cơ bản, nguyên tử của nguyên tố M có 4 lớp electron và 4 electron độc thân. Hãy xác định tên các nguyên tố R và M.
3. Trong một bình nước có chứa 0,01 mol Na+, 0,02 mol Ca2+, 0,005 mol Mg2+, 0,05 mol HCO3- và 0,01 mol Cl-.
a) Hãy cho biết nước trong bình có tính cứng tạm thời hay vĩnh cửu. Vì sao?
b) Đun sôi nước trong bình cho đến phản ứng hoàn toàn, hãy cho biết tính cứng của nước có thay đổi không?
4. Hòa tan hoàn toàn 66,2 gam hỗn hợp X gồm Fe3O4, Fe(NO3)2 và Al trong dung dịch chứa 3,1 mol KHSO4 (loãng). Sau phản ứng, thu được dung dịch Y chỉ chứa 466,6 gam muối sunfat trung hòa và 10,08 lít (đktc) khí Z gồm 2 khí trong đó có một khí hóa nâu ngoài không khí, tỉ khối của Z so với He là 23/18. Tính phần trăm khối lượng của Al trong hỗn hợp X.
Câu 2. (4,0 điểm)
1. Hoàn thành các phương trình phản ứng sau (biết tỉ lệ mol các chất đều là 1:1):
a) Dung dịch BaCl2 tác dụng với dung dịch NaHSO4.
b) Dung dịch Ba(HCO3)2 tác dụng với dung dịch KHSO4.
c) Dung dịch Ca(H2PO4)2 tác dụng với dung dịch KOH.
d) Dung dịch Ca(OH)2 tác dụng với dung dịch NaHCO3.
2. Hoà tan hoàn toàn 5,4 gam một kim loại R bằng dung dịch H2SO4 đặc nóng dư, thu được SO2 (sản phẩm khử duy nhất). Cho toàn bộ lượng khí này hấp thụ hết vào 350 ml dung dịch NaOH 2M. Sau phản ứng, cô cạn dung dịch thì thu được 41,8 gam chất rắn khan. Xác định R.
3. Sục khí A vào dung dịch chứa chất B ta được chất C rắn, màu vàng và dung dịch D. Khí X có màu vàng lục tác dụng với khí A tạo ra chất C và F. Nếu X tác dụng với khí A trong nước thì tạo ra chất Y và F, rồi thêm BaCl2 vào dung dịch thì có kết tủa trắng. A tác dụng với dung dịch chứa chất G là muối nitrat kim loại tạo ra kết tủa H màu đen. Đốt cháy chất H bởi oxi ta được chất lỏng I màu trắng bạc. Viết các phương trình phản ứng xảy ra.
4. Dung dịch A1 chứa NaOH 1M và Ba(OH)2 0,5M. Dung dịch B1 chứa AlCl3 1M và Al2(SO4)3 0,5M. Cho V1 lít dung dịch A1 vào V2 lít dung dịch B1 thu được 56,916 gam kết tủa. Nếu cho dung dịch BaCl2 dư vào V2 lít dung dịch B1 thu được 41,94 gam kết tủa.
Viết các phương trình phản ứng xảy ra dạng ion và tính giá trị của V1 và V2.
Câu 3. (4,0 điểm)
1. Hỗn hợp A gồm FexOy, FeCO3, RCO3 (R thuộc nhóm IIA). Hoà tan m gam A dùng vừa hết 245 ml dung dịch HCl 2 M. Mặt khác, đem hoà tan hết m gam A bằng dung dịch HNO3 được dung dịch B và 2,8 lít khí C (đktc) gồm NO (sản phẩm khử duy nhất) và CO2. Cho dung dịch B tác dụng hoàn toàn với dung dịch NaOH dư, thu được 21,69 gam kết tủa D. Chia D thành 2 phần bằng nhau. Nung phần 1 trong không khí đến khối lượng không đổi thu được 8,1 gam chất rắn chỉ gồm 2 oxit. Hoà tan hết phần 2 bằng dung dịch H2SO4 loãng vừa đủ được dung dịch G. Cho 23,1 gam bột Cu vào một nửa dung dịch G, sau khi phản ứng hoàn toàn lọc tách được 21,5 gam chất rắn.
Viết các phương trình phản ứng xảy ra và xác định FexOy, RCO3.
2. Aspirin (axit axetyl salixilic, o-CH3COO-C6H4-COOH) có tính axit yếu, hằng số cân bằng là 10-3,49, độ tan trong nước ở nhiệt độ phòng là 0,355 gam/100 gam H2O. Tính pH của dung dịch Aspirin bão hòa ở nhiệt độ phòng.
3. Trong bình kín thể tích là 10 lít chứa không khí (20% O2 và 80% N2 theo thể tích) và 1,54 gam chất X (chứa C, H, O, N; tương ứng với 0,02 mol, thể khí) ở áp suất P, nhiệt độ 54,60C. Bật tia lửa điện để đốt cháy hết X. Sau đó cho toàn bộ sản phẩm cháy qua lần lượt bình 1 đựng P2O5 dư, bình 2 đựng 400 ml dung dịch Ba(OH)2 0,075M và bình 3 đựng photpho dư đun nóng, khí còn lại là N2 có thể tích là 5,6 lít (đktc). Cho các phản ứng xảy ra hoàn toàn, hãy xác định giá trị của P. Biết bình 1 tăng 1,26 gam, bình 2 tạo 3,94 gam kết tủa và khi đun nóng dung dịch sau phản ứng lại có kết tủa xuất hiện, bình 3 tăng 0,16 gam.
Câu 4. (4,0 điểm)
1. Cho các chất: C6H5OH, C2H5OH, CH3COOH, C6H5ONa, C2H5ONa. Viết các phương trình phản ứng xảy ra (nếu có, trong điều kiện thích hợp) khi trộn các chất với nhau từng đôi một.
2. Hoàn thành các phương trình phản ứng theo sơ đồ chuyển hoá sau:
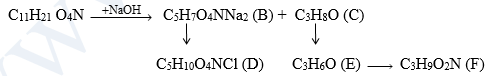
Biết B là muối của một a- aminoaxit có mạch cacbon không phân nhánh.
3. Thủy phân hết 1 lượng pentapeptit X trong môi trường axit thu được 32,88 gam Ala–Gly–Ala–Gly, 10,85 gam Ala–Gly–Ala, 16,24 gam Ala–Gly–Gly, 26,28 gam Ala–Gly, 8,9 gam alanin còn lại là Gly–Gly và glyxin. Tỉ lệ số mol Gly–Gly:Gly là 10:1. Tính tổng khối lượng Gly–Gly và glyxin.
4. Đốt cháy hoàn toàn 7,6 gam hỗn hợp gồm một axit cacboxylic no, đơn chức, mạch hở và một ancol đơn chức thu được 0,3 mol CO2 và 0,4 mol H2O. Thực hiện phản ứng este hóa 7,6 gam hỗn hợp trên với hiệu suất 80% thu được m gam este. Viết các phương trình phản ứng và tính giá trị của m.
Câu 5. (4,0 điểm)
1. Bằng phương pháp hoá học, hãy nhận biết các dung dịch riêng biệt mất nhãn chứa các chất sau: HCOOH, CH3COOH, CH2=CH-COOH, H2N-CH2-COOH, C6H5NH2.
2. Hoàn thành các phương trình phản ứng theo sơ đồ chuyển hoá sau:
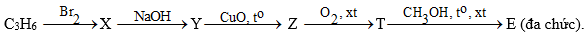
3. Viết các phương trình hoá học trực tiếp điều chế các loại tơ sau: axetat, nilon-6,6, lapsan.
4. Thủy phân hoàn toàn hỗn hợp A gồm 2 este no, mạch hở (trong phân tử mỗi chất chỉ chứa nhóm chức este) bằng dung dịch NaOH vừa đủ. Chưng cất dung dịch sau phản ứng, thu được 12,3 gam muối khan B của một axit hữu cơ và hỗn hợp C gồm 2 ancol (số nguyên tử cacbon trong mỗi phân tử ancol không vượt quá 3). Đốt cháy hoàn toàn muối B trên, thu được 7,95 gam muối Na2CO3. Mặt khác, đốt cháy hoàn toàn hỗn hợp C trên, thu được 3,36 lít CO2 (đktc) và 4,32 gam H2O. Xác định công thức cấu tạo của 2 este.
---(Nội dung đầy đủ, chi tiết phần đáp án của đề thi vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐỀ SỐ 2
Câu 1 (2 điểm):
a. Em hãy trình bày cách tráng một lớp bạc mỏng lên mặt trong một ống nghiệm. Nêu rõ hóa chất cần dùng và viết phương trình hóa học xẩy ra.
b. Cho biết bộ dụng cụ trong hình vẽ bên được sử dụng để điều chế chất nào trong số các chất: HNO3, N2O, N2? Hãy cho biết các hợp chất A, B tương ứng? Viết phương trình hóa học xẩy ra trong quá trình điều chế, nêu vai trò của chất C?
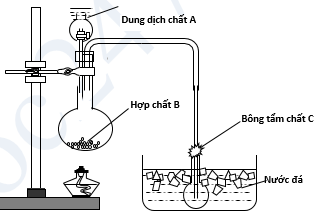
Câu 2 (2 điểm):
a. So sánh lực bazơ của các chất có vòng benzen sau: m-CH3C6H4NH2, p-CH3C6H4NH2,
o-CH3C6H4NH2, p-O2NC6H4NH2, p-ClC6H4NH2. Giải thích?
b. So sánh lực axit của các chất sau:
(CH3)3CCOOH; CH3CH=CHCH2COOH; CH3CH2CH=CHCOOH; (CH3)2CHCOOH;
CH2=CHCH2CH2COOH. Giải thích?
Câu 3 (4 điểm):
1. Viết các phương trình phản ứng xảy ra khi dùng dung dịch Ca(OH)2 dư để loại bỏ các khí độc sau đây ra khỏi không khí: Cl2, SO2, H2S, NO2.
2. Viết các phương trình phản ứng xảy ra dạng ion trong các thí nghiệm sau:
a) Hoà tan CuS bằng dung dịch HNO3 dư thu được dung dịch X và khí Y không màu hoá nâu trong không khí. Cho X tác dụng với dung dịch NH3 dư thu được dung dịch Z.
b) Cho Ag2S tác dụng với dung dịch NaCN thu được dung dịch T. Cho T tác dụng với Zn.
3. Cho các chất rắn riêng biệt: MgO, Al, Al2O3, BaO, Na2SO4 và (NH4)2SO4. Nếu chỉ dùng nước thì có thể phân biệt được bao nhiêu chất rắn. Trình bày cách phân biệt và viết phương trình hóa học xảy ra.
4. Hòa tan hoàn toàn m gam hỗn hợp gồm Fe và MgCO3 bằng dung dịch HCl dư được hỗn hợp khí A gồm H2 và CO2. Nếu cũng m gam hỗn hợp trên tác dụng với dung dịch H2SO4 đặc nóng dư, thì thu được hỗn hợp khí B gồm SO2 và CO2, tỉ khối hơi của B đối với A là 3,6875.
Viết các phương trình phản ứng và tính % khối lượng mỗi chất trong hỗn hợp đầu
Câu 4 (1 điểm):
Cho 11,2 gam Fe vào 300 ml dung dịch chứa (HNO3 0,5M và HCl 2M) thu được khí NO (sản phẩm khử duy nhất) và dung dịch X. Cho dung dịch X tác dụng với lượng dư dung dịch KMnO4 / H2SO4 loãng. Biết các phản ứng xảy ra hoàn toàn.
a. Cô cạn dung dịch X thu được bao nhiêu gam chất rắn khan.
b. Tính khối lượng KMnO4 đã bị khử.
Câu 5 (1 điểm):
Hỗn hợp D gồm etan, etilen, propin. Cho 12,24 gam D tác dụng với lượng dư dung dịch AgNO3/NH3, phản ứng xong thu được 14,7 gam kết tủa. Mặt khác 4,256 lít D (đktc) phản ứng vừa đủ 140 ml dung dịch Br2 1M. Tính số mol mỗi chất có trong 12,24 gam D.
---(Nội dung đầy đủ, chi tiết phần đáp án của đề thi vui lòng xem tại online hoặc đăng nhập để tải về máy)---
...
Trên đây là toàn bộ nội dung Bộ đề thi chọn HSG môn Hóa học 12 năm 2021 có đáp án Trường THPT Thái Phiên, để xem toàn thêm nhiều tài liệu tham khảo hữu ích khác, mời các bạn cùng quý thầy cô vui lòng đăng nhập để tải về máy.
Chúc các em đạt điểm số thật cao trong kì thi sắp đến!
Ngoài ra các em có thể tham khảo thêm một số tài liệu cùng chuyên mục tại đây:
Tư liệu nổi bật tuần
- Xem thêm
ERROR:connection to 10.20.1.101:9312 failed (errno=111, msg=Connection refused)
ERROR:connection to 10.20.1.101:9312 failed (errno=111, msg=Connection refused)


