Giải bài 7.10 trang 25 SBT Hóa học 10 Chân trời sáng tạo
Oxide cao nhất của một nguyên tố R chúa 72,73% oxygen. Tuy không phải là khí quá độc nhưng với nồng độ lớn thì sẽ làm giảm nồng độ oxygen trong không khí, gây ra các tác hại như mệt mỏi, khó thở, kích thích thần kinh, tăng nhịp tim và các rối loạn khác. Hợp chất khí với hydrogen chứa 75% nguyên tố đó. Hợp chất này thường được sử dụng làm nhiên liệu cho các lò nướng, nhà cửa, máy nước nóng, lò nung, xe ô tô. Viết công thức oxide cao nhất và hợp chất khí với hydrogen của nguyên tố R.
Hướng dẫn giải chi tiết bài 7.10
Phương pháp giải:
- Công thức oxide cao nhất và hợp chất khí với hydrogen của các nguyên tố từ IA đến VIIA
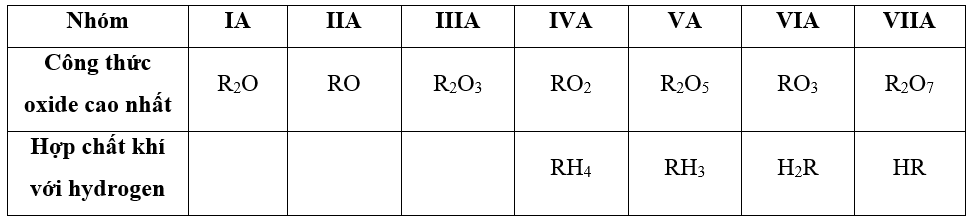
=> Xác định nhóm của nguyên tố
- Công thức thành phần phần trăm khối lượng của một nguyên tố trong hợp chất XaYb:
\(\% {m_X} = \frac{{a.{A_X}}}{{{A_{{X_a}{Y_b}}}}}.100\% = \frac{{a.{A_X}}}{{a.{A_X} + b.{A_Y}}}.100\% \)
Lời giải chi tiết:
- Gọi hợp chất với hydrogen của R là RHx
=> Hợp chất oxide cao nhất của R là R2O8-x
\(\% {m_O} = \frac{{(8 - x).{A_O}}}{{2.{A_R} + (8 - x).{A_O}}}.100\% = \frac{{(8 - x).16}}{{2.{A_R} + (8 - x).16}}.100\% = 72,73\% \)(1)
\(\% {m_R} = \frac{{1.{A_R}}}{{1.{A_R} + x.{A_H}}}.100\% = \frac{{1.{A_R}}}{{1.{A_R} + x.1}}.100\% = 75\% \) (2)
=> Từ (1) và (2) giải hệ hai phương trình hai ẩn ta có: R = 12 và x = 4
=> Vậy R là nguyên tố carbon (C). Hợp chất của carbon với hydrogen là CH4 và công thức oxide cao nhất của carbon là CO2
-- Mod Hóa Học 10 HỌC247
Bài tập SGK khác
Chưa có câu hỏi nào. Em hãy trở thành người đầu tiên đặt câu hỏi.





