Bài tập 7 trang 104 SGK Hóa học 10 nâng cao
Điiot pentaoxit (I2O5) tác dụng với cacbon monoxit tạo ra cacbon đioxit và iot.
a) Lập phương trình hóa học của phản ứng oxi hóa - khử trên.
b) Khi cho một lít hỗn hợp có chứa CO và CO2 tham gia phản ứng thì khối lượng điiot pentaoxit bị khử là 0,5 gam. Tính thành phần phần trăm về thể tích của CO trong hỗn hợp khí. Biết rằng ở điều kiện thí nghiệm, thể tích mol của chất khí V = 24 lít.
Hướng dẫn giải chi tiết bài 7
Câu a:
Phương trình phản ứng
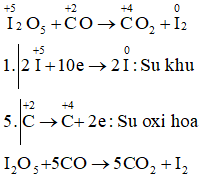
Câu b:
Tính phần trăm về thể tích CO trong hỗn hợp khí:
Chỉ có CO tham gia phản ứng. Theo phương trình phản ứng:
nCO = 5nI2O5 = (5.0,5)/334 = 5/668 mol
VCO = (24. 5)/668 ≈ 0,18 lit
⇒ %VCO = 0,18.100% ≈ 18%
-- Mod Hóa Học 10 HỌC247
Bài tập SGK khác
-


Cân bằng phương trình sau:CuCl3+K3PO4 ---> Cu3(PO4)2+KCl
bởi Sasu ka
 15/10/2018
15/10/2018
Cân bằng phương trình sau:
CuCl3+K3PO4 ---> Cu3(PO4)2+KCl
Theo dõi (0) 1 Trả lời -


Số oxi hóa và hóa trị của N trong các axit HNO3 và HNO2 lần lượt là bao nhiêu?
bởi Bánh Mì
 17/10/2018
17/10/2018
Số oxi hóa và hóa trị của N trong các axit HNO3 và HNO2 lần lượt là:
A.+5 và V; +3 và III
B.+5 và IV; +3 và IV
C.+5 và IV; +3 và III
D.+5 và V; -3 và III
Theo dõi (0) 1 Trả lời -


Tính khối lượng Al tham gia phản ứng.
bởi đào trường
 08/07/2017
08/07/2017
hòa tan hết m gam bôt kim lịa nhôm trong dung dịch HNO3 thu được 13,44 lít hỗn hợp 3 khí NO,N20,N2 tỉ lệ 3:2:2 tính m
Theo dõi (0) 2 Trả lời




