Bộ 5 đề thi HK1 môn Hóa học 11 năm 2021-2022 có đáp án Trường THPT Bình Giang đã được HOC247 biên soạn một cách đầy đủ, chi tiết bên dưới đây. Đề thi không quá khó, nội dung kiến thức nằm trọn trong chương trình Hóa lớp 11 học kì 1, chính vì vậy đối với những học sinh đã nắm chắc kiến thức trong SGK chắc chắn sẽ làm bài thi tốt và đạt điểm từ khá trở lên. mời các bạn cùng tham khảo!
|
TRƯỜNG THPT BÌNH GIANG |
ĐỀ THI HỌC KÌ 1 MÔN HÓA HỌC 11 THỜI GIAN 45 PHÚT NĂM HỌC 2021-2022 |
ĐỀ THI SỐ 1
I. TRẮC NGHIỆM KHÁCH QUAN
Câu 1: Một dung dịch có môi trường axit thì có
A. [H+] > [OH-]. B. [H+] = [OH-]. C. [H+] < 10-7M. D. [H+] = 10-7M.
Câu 2: Bản chất của phản ứng trong dung dịch các chất điện li là
A. phản ứng giữa các ion. B. sự phân li thành các ion trong dung dịch.
C. phản ứng tạo thành các chất kết tủa. D. phản ứng giữa chất oxi hóa và chất khử.
Câu 3: Chất nào sau đây không phải là chất điện li?
A. Natri clorua (NaCl). B. Axit clo hiđric (HCl).
C. Ancol etylic (C2H5OH). D. Kali hiđroxit (KOH).
Câu 4: Theo thuyết A-rê-ni-ut, chất nào sau đây là axit?
A. HNO3. B. NH3. C. NaHCO3. D. NaOH.
Câu 5: Trong các muối sau, muối nào là muối trung hòa?
A. NaHCO3. B. NH4HCO3. C. KHSO4. D. Na2SO4.
Câu 6: Kim loại nào sau đây phản ứng được với dung dịch HNO3 đặc nguội?
A. Al. B. Fe. C. Cu. D. Pt.
Câu 7: Trong phòng thí nghiệm, người ta điều chế khí NH3 bằng cách
A. nhiệt phân NH4Cl. B. nhiệt phân NH4NO3.
C. tổng hợp từ N2 và H2 (t0, xt, p). D. đun nóng NH4Cl với Ca(OH)2.
Câu 8: Số oxi hóa của C trong CO2 là
A. -4. B. +4. C. -2. D. +2.
Câu 9: Muối nào sau đây không tan trong nước?
A. NaNO3. B. BaCO3. C. K2SO4. D. (NH4)2CO3.
Câu 10: Muối nào sau đây là muối nitrat?
A. KNO3. B. MgCl2. C. NH4Cl. D. Na2SO4.
Câu 11: Nguyên tố nitơ ở nhóm nào trong bảng tuần hoàn?
A. VB. B. VA. C. IIIA. D. IIIB.
Câu 12: Chất tan trong nước phân li ra ion được gọi là chất
A. dễ tan. B. điện li. C. điện phân. D. oxi hóa.
Câu 13: Nồng độ mol/lít của ion trong dung dịch Ba(NO3)2 0,1 M là
A. 1,0. B. 0,4. C. 0,1. D. 0,2.
Câu 14: Phản ứng giữa NH3 và HNO3 tạo thành sản phẩm có tên gọi là
A. amoni nitrit. B. amoni clorua. C. axit nitric. D. amoni nitrat.
Câu 15: Sản phẩm của phản ứng nhiệt phân hoàn toàn muối AgNO3 là
A. AgNO2, O2. B. Ag, NO2, O2. C. AgO, NO2, O2. D. Ag, NO, O2.
Câu 16: Đặc điểm nào sau đây sai đối với N2?
A. Thể hiện tính oxi hóa khi tác dụng với H2.
B. Tương đối trơ ở nhiệt độ thường.
C. Phân tử có liên kết ba kém bền.
D. Thể hiện tính khử khi tác dụng với O2.
Câu 17: Cho sơ đồ phản ứng: Fe(NO3)3 + KOH → X + KNO3. Chất X là
A. Fe(NO3)2. B. Fe. C. Fe(OH)2. D. Fe(OH)3.
Câu 18: Cho dãy chuyển hóa: N2 → X→ (Y)→ (Z) → T. Các chất Y và T lần lượt là
A. NO và NO2. B. NO2 và HNO3. C. NO và HNO3. D. N2 và N2O5.
Câu 19: Cặp chất nào sau đây (trong dung dịch) phản ứng được với nhau?
A. Na2CO3 và KNO3.
B. Fe2(SO4)3 và NaNO3.
C. NaOH và HCl.
D. KCl và NaNO3.
Câu 20: Dung dịch HNO3 0,001 M có pH là
A. 1. B. 2. C. 11. D. 3.
Câu 21: Phản ứng nào sau đây C (cacbon) có tính oxi hóa?
A. 3C + 4Al → Al4C3.
B. C + 2CuO → 2Cu + CO2.
C. C + O2 → CO2.
D. C + H2O → CO + H2.
II. TỰ LUẬN
Câu 1.
a. Viết phương trình phân tử và phương trình ion thu gọn của phản ứng xảy ra (nếu có) khi:
- Cho lượng dư dung dịch natri hiđroxit (NaOH) vào dung dịch amoni sunfat ((NH4)2SO4).
- Thêm từ từ đến dư dung dịch axit clo hiđric (HCl) loãng vào dung dịch kali cacbonat (K2CO3).
b. Tính khối lượng H2 cần dùng để tổng hợp 150 tấn NH3 (từ N2 và H2) với hiệu suất của toàn bộ quá trình đạt 96% (kết quả làm tròn đến 1 chữ số thập phân).
Câu 2. Hỗn hợp X gồm 0,24 gam Mg và 0,56 gam Fe. Cho X phản ứng hoàn toàn với dung dịch HNO3 (đun nóng, dư 10% so với lượng phản ứng), thu được dung dịch Y (chỉ chứa 2 muối và axit dư), khí NO2 (sản phẩm khử duy nhất). Thêm dung dịch chứa 3,4 gam NaOH vào dung dịch Y, thu được kết tủa và 250 ml dung dịch Z. Cho các phản ứng xảy ra hoàn toàn. Xác định giá trị pH của dung dịch Z.
ĐÁP ÁN ĐỀ SỐ 1
A/ TRẮC NGHIỆM
|
1 |
A |
8 |
B |
15 |
B |
|
2 |
A |
9 |
B |
16 |
C |
|
3 |
C |
10 |
A |
17 |
D |
|
4 |
A |
11 |
B |
18 |
C |
|
5 |
D |
12 |
B |
19 |
C |
|
6 |
C |
13 |
D |
20 |
D |
|
7 |
D |
14 |
D |
21 |
A |
B/ TỰ LUẬN:
Câu 1
a. 2NaOH + (NH4)2SO4 → Na2SO4 + 2NH3 + 2H2O
OH- + NH4+ → NH3 + H2O
HCl + K2CO3 → KHCO3 + KCl
H+ + CO32- → HCO3-
HCl + KHCO3 → KCl + CO2 + H2O
H+ + HCO3- → CO2 + H2O
b. N2 + 3H2 2NH3
Khối lượng H2 cần dùng nếu H= 100%: 150*3/17= 26,5 tấn.
Khối lượng H2 cần dùng khi H= 96%: 26,5*100/96= 27,6 tấn.
Câu 2
n (Mg) = n(Mg2+) = 0,24/24 = 0,01 mol.
n(Fe) = n(Fe3+) = 0,56/56 = 0,01 mol.
nHNO3 (pư) = 0,1 mol => nHNO3 (dư) = 0,01 mol
n(NaOH) = n(OH-) ban đầu = 3,4/40 = 0,085 mol.
n(OH-) phản ứng = 0,01 + 2*0,01+ 3* 0,01 = 0,06 mol.
n(OH-) dư = 0,085 - 0,06 = 0,025 mol.
[OH-] trong Z: 0,025/0,25 = 0,1 M
pH= 13.
ĐỀ THI SỐ 2
ĐỀ THI HỌC KÌ 1 MÔN HÓA HỌC 11- TRƯỜNG THPT BÌNH GIANG- ĐỀ 02
I. TRẮC NGHIỆM KHÁCH QUAN
Câu 1: Bản chất của phản ứng trong dung dịch các chất điện li là
A. sự phân li thành các ion trong dung dịch.
B. phản ứng tạo thành các chất kết tủa.
C. phản ứng giữa các ion.
D. phản ứng giữa chất oxi hóa và chất khử.
Câu 2: Sự điện li là quá trình
A. hòa tan các chất tan vào nước.
B. phân li các chất trong nước ra ion.
C. oxi hóa các chất thành ion.
D. nhiệt phân các chất thành ion.
Câu 3: Trong các muối sau, muối nào là muối axit?
A. CuSO4. B. NH4Cl C. NaHCO3. D. NaNO3.
Câu 4: Muối nào sau đây dễ tan trong nước?
A. CaCO3. B. BaSO4. C. NH4Cl. D. AgCl.
Câu 5: Chất nào sau đây không phải là chất điện li?
A. Natri hiđroxit (NaOH). B. Kali clorua (KCl).
C. Axit nitric (HNO3). D. Glixerol (C3H5(OH)3).
Câu 6: Trong công nghiệp, người ta điều chế khí NH3 bằng cách
A. tổng hợp từ N2 và H2 (t0, xt, p). B. nhiệt phân NH4Cl.
C. nhiệt phân NH4NO3. D. đun nóng NH4Cl với Ca(OH)2.
Câu 7: Số electron lớp ngoài cùng của nguyên tử nitơ là
A. 7. B. 3. C. 2. D. 5.
Câu 8: Nguyên tố cacbon ở nhóm nào trong bảng tuần hoàn?
A. IVA. B. IIA. C. IIB. D. IVB.
Câu 9: Theo thuyết A-rê-ni-ut, chất nào sau đây là bazơ?
A. HNO3. B. NaOH. C. C2H5OH. D. NaHCO3.
Câu 10: Một dung dịch có môi trường bazơ thì có
A. [H+] = [OH-]. B. [H+] = 10-7M. C. [H+] > 10-7M. D. [H+] < [OH-].
---(Để xem tiếp nội dung từ câu số 11 đến câu 21 phần trắc nghiệm và phần tự luận của đề thi số 2 các em vui lòng xem Online hoặc Đăng nhập vào HOC247 để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 2
A/ TRẮC NGHIỆM
|
1 |
C |
8 |
A |
15 |
A |
|
2 |
B |
9 |
B |
16 |
D |
|
3 |
C |
10 |
D |
17 |
D |
|
4 |
C |
11 |
A |
18 |
C |
|
5 |
D |
12 |
B |
19 |
D |
|
6 |
A |
13 |
B |
20 |
B |
|
7 |
D |
14 |
C |
21 |
A |
B/ TỰ LUẬN:
Câu 22:
a. KOH + NH4Cl → KCl + NH3 + H2O
OH- + NH4+ → NH3 + H2O
HNO3 + Na2CO3 → NaHCO3 + KNO3
H+ + CO32- → HCO3-
HNO3 + NaHCO3 → NaNO3 + CO2 + H2O
H+ + HCO3- → CO2 + H2O
b. N2 + 3H2 2NH3
Khối lượng N2 cần dùng nếu H= 100%: 150*14/17= 123,5 tấn.
Khối lượng N2 cần dùng khi H= 96%: 123,5*100/96= 128,6 tấn.
Câu 23:
n (Mg)= n(Mg2+) = 0,36/24= 0,015 mol.
n(Fe)= n(Fe3+) = 1,12/56= 0,02 mol.
nHNO3 (pư) = 0,18 => nHNO3 (dư)= 0,018
n(NaOH)= n(OH-) ban đầu = 4,42/40= 0,1105 mol.
n(OH-) phản ứng = 0,018 + 2*0,015+ 3* 0,02= 0,108 mol.
n(OH-) dư= 0,1105- 0,108= 0,0025 mol.
[OH-] trong Z: 0,0025/0,25= 0,01 M
pH= 12.
ĐỀ THI SỐ 3
ĐỀ THI HỌC KÌ 1 MÔN HÓA HỌC 11- TRƯỜNG THPT BÌNH GIANG- ĐỀ 03
I/ PHẦN TRẮC NGHIỆM
Câu 1: Với 30 ml dung dịch HNO3 2,0 M có thể hòa tan tối đa bao nhiêu gam kim loại Cu? Giả sử phản ứng chỉ tạo thành sản phẩm khử duy nhất là khí NO.
A. 1,44. B. 0,36. C. 3,84. D. 0,96.
Câu 2: Khí X không màu, không mùi, rất độc, sinh ra trong quá trình đốt than không hoàn toàn. Khí X là
A. CO2. B. SO2. C. NO2. D. CO.
Câu 3: Photpho trắng không có đặc điểm nào sau đây?
A. Màu trắng, mềm. B. Dễ nóng chảy.
C. Rất độc, dễ cháy. D. Dễ tan trong nước.
Câu 4: Một dung dịch có chứa: 0,05 mol Al3+, a mol K+ và 0,15 mol SO42-. Bỏ qua sự điện li của nước và sự thủy phân của ion. Giá trị của a là
A. 0,20. B. 0,10. C. 0,15. D. 0,25.
Câu 5: Một học sinh đề nghị sơ đồ thiết bị để điều chế khí CO2 trong phòng thí nghiệm từ đá vôi (CaCO3) và loại bỏ tạp chất (khí HCl, hơi H2O) như sau:
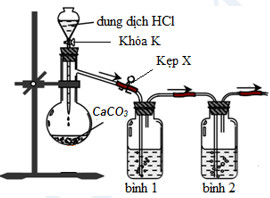
Cho các phát biểu:
(a) Để kiểm soát tốc độ khí thoát ra, nên điều chỉnh kẹp X thay vì điều chỉnh khóa K.
(b) Nên thay dung dịch HCl bằng dung dịch H2SO4 hoặc HNO3 vì các axit này không bay hơi.
(c) Bình 1 và bình 2 có thể lần lượt chứa lượng dư các dung dịch Na2CO3 bão hòa và H2SO4 đậm đặc.
(d) Khí CO2 thoát ra có thể được thu vào bình tam giác bằng cách đẩy không khí để úp bình thu.
Số phát biểu đúng là
A. 1. B. 2. C. 3. D. 4.
Câu 6: Cho m gam Ca(OH)2 vào 200 ml dung dịch HCl 2,0 M. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch có pH = 7. Giá trị của m là
A. 29,6. B. 7,4. C. 14,8. D. 59,2.
Câu 7: Chất nào sau đây được dùng làm phân đạm?
A. NH4Cl. B. Ca(H2PO4)2. C. K2CO3. D. CaSO4.
Câu 8: Cách nào sau đây không được dùng để điều chế H3PO4 trong công nghiệp?
A. Đốt P trong O2 dư, cho sản phẩm tác dụng với H2O.
B. Cho axit sunfuric đặc tác dụng với photpho.
C. Cho axit sunfuric đặc tác dụng với quặng photphorit.
D. Cho axit sunfuric đặc tác dụng với quặng apatit.
Câu 9: Đơn chất N2 thể hiện tính khử trong phản ứng với chất nào dưới đây?
A. Al. B. H2. C. O2. D. Mg.
Câu 10: Cho phương trình hóa học: Kim loại M trong phương trình hóa học trên là
A. Cu. B. Na. C. K. D. Ag.
---(Để xem tiếp nội dung từ câu 11 đến câu 19 của đề thi số 3 các em vui lòng xem Online hoặc Đăng nhập vào HOC247 để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 3
|
1 |
A |
6 |
C |
11 |
C |
|
2 |
D |
7 |
A |
12 |
D |
|
3 |
D |
8 |
B |
13 |
A |
|
4 |
C |
9 |
C |
14 |
D |
|
5 |
A |
10 |
A |
15 |
B |
Câu 16:
a/ NaOH → Na+ + OH-.
b/ NH4NO3 → N2O + 2H2O.
c/ Na2HPO4
d/ Canxi cacbonat.
Câu 17:
+ Hiện tượng:
- Dung dịch Na2CO3: Có kết tủa trắng.
- Dung dịch NH4Cl: Thoát ra khí có mùi khai (hoặc có mùi khai bay ra).
- Dung dịch NaNO3: Không có hiện tượng gì.
+ PTHH:
Ba(OH)2 + Na2CO3 → BaCO3↓ + 2NaOH
Ba(OH)2 + 2NH4Cl → BaCl2+ 2NH3↑+ 2H2O
Câu 18: Số mol KOH = 11,2/56 = 0,2 mol, số mol H3PO4 = 0,5.0,2 = 0,1 mol
Tính đúng số mol cả 2 chất mới tính điểm
→ tạo muối K2HPO4
PTHH: 2KOH + H3PO4 → K2HPO4 + 2H2O
Tính được số mol và nồng độ mol/l của muối K2HPO4
[K2HPO4] = 0,1/0,2 = 0,5M.
Câu 19: Như ống nghiệm 4. Vì dung dịch HCl loãng (môi trường axit) không làm đổi màu phenolphtalein (dung dịch thu được không màu), hỗn hợp thu được đồng nhất.
ĐỀ THI SỐ 4
ĐỀ THI HỌC KÌ 1 MÔN HÓA HỌC 11- TRƯỜNG THPT BÌNH GIANG- ĐỀ 04
I/ PHẦN TRẮC NGHIỆM KHÁCH QUAN
Câu 1: Theo thuyết A-rê-ni-ut, chất nào sau đây là bazơ?
A. HCl. B. NaCl. C. C3H5(OH)3. D. NaOH.
Câu 2: Cho phương trình hóa học: Kim loại M trong phương trình hóa học trên là
A. K. B. Al. C. Ag. D. Cu.
Câu 3: Hợp chất NH3 thể hiện tính khử trong phản ứng với chất nào dưới đây?
A. H2O. B. H3PO4. C. O2. D. HCl.
Câu 4: Chất nào sau đây được dùng làm phân đạm?
A. K2SO4. B. NaNO3. C. CaHPO4. D. CaCO3.
Câu 5: Hình dưới đây là một mẫu bao bì phân bón hóa học được bán trên thị trường:

Số 20 (được khoanh tròn) trên mẫu bao bì đó biểu thị hàm lượng dinh dưỡng của
A. đạm. B. lân. C. nguyên tố vi lượng. D. kali.
Câu 6: Photpho đỏ không có đặc điểm nào sau đây?
A. Không tan trong nước. B. Bền ở nhiệt độ thường.
C. Phát quang trong bóng tối. D. Dễ hút ẩm và chảy rữa.
Câu 7: Trong công nghiệp, người ta dùng cách nào sau đây để điều chế H3PO4 có độ tinh khiết cao?
A. Cho axit sunfuric đặc tác dụng với quặng apatit.
B. Cho axit sunfuric đặc tác dụng với quặng photphorit.
C. Cho axit nitric đặc tác dụng với photpho.
D. Đốt P trong O2 dư, cho sản phẩm tác dụng với H2O.
Câu 8: Với 45 ml dung dịch HNO3 2,0 M có thể hòa tan tối đa bao nhiêu gam kim loại Cu? Giả sử phản ứng chỉ tạo thành sản phẩm khử duy nhất là khí NO.
A. 0,54. B. 5,76. C. 1,44. D. 2,16.
Câu 9: Phát biểu nào sau đây sai đối với Na2CO3?
A. Có phản ứng với dung dịch axit clohiđric. B. Dễ tan trong nước và bền với nhiệt.
C. Được dùng trong công nghiệp thủy tinh. D. Có phản ứng với dung dịch natri hiđroxit.
Câu 10: Để khử hết 28 gam Fe2O3 thành Fe, cần vừa đủ V lít khí CO (đktc). Giá trị của V là
A. 3,92. B. 1,31. C. 7,84. D. 11,76.
---(Để xem tiếp nội dung từ câu 11 đến câu 15 phần trắc nghiệm và phần tự luận của đề thi số 4 các em vui lòng xem Online hoặc Đăng nhập vào HOC247 để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 4
|
1 |
D |
6 |
C |
11 |
A |
|
2 |
A |
7 |
D |
12 |
C |
|
3 |
C |
8 |
D |
13 |
C |
|
4 |
B |
9 |
D |
14 |
A |
|
5 |
D |
10 |
D |
15 |
A |
ĐỀ THI SỐ 5
ĐỀ THI HỌC KÌ 1 MÔN HÓA HỌC 11- TRƯỜNG THPT BÌNH GIANG- ĐỀ 05
Câu 1: Một dung dịch có [H+] = 10-7 M thì có môi trường
A. lưỡng tính. B. trung tính. C. axit. D. bazơ.
Câu 2: Chất nào sau đây được dùng làm phân đạm?
A. KCl. B. CaSO4. C. (NH2)2CO. D. Ca3(PO4)2.
Câu 3: Khí X không màu, không mùi, được dùng để dập tắt các đám cháy. Khí X là
A. CO2. B. CO. C. H2. D. O2.
Câu 4: Cho phương trình hóa học: Kim loại M trong phương trình hóa học trên là
A. Na. B. Al. C. Ag. D. Cu.
Câu 5: Phát biểu nào sau đây sai đối với NaHCO3?
A. Được dùng trong công nghiệp thực phẩm.
B. Dùng làm thuốc giảm đau dạ dày do thừa axit.
C. Không phản ứng với dung dịch natri hiđroxit.
D. Tan trong nước và dễ bị nhiệt phân hủy.
Câu 6: Một dung dịch có chứa: 0,15 mol Al3+, a mol K+ và 0,45 mol SO42-. Bỏ qua sự điện li của nước và sự thủy phân của ion. Giá trị của a là
A. 0,75. B. 0,60. C. 0,30. D. 0,45.
Câu 7: Hình dưới đây là một mẫu bao bì phân bón hóa học được bán trên thị trường:

Số 20 (được khoanh tròn) trên mẫu bao bì đó biểu thị hàm lượng dinh dưỡng của
A. đạm. B. nguyên tố vi lượng.
C. kali. D. lân.
Câu 8: Cách nào sau đây không được dùng để điều chế H3PO4 trong công nghiệp?
A. Đốt P trong O2 dư, cho sản phẩm tác dụng với H2O.
B. Cho axit sunfuric đặc tác dụng với quặng apatit.
C. Cho axit sunfuric đặc tác dụng với quặng photphorit.
D. Cho axit nitric đặc tác dụng với photpho.
Câu 9: Cho m gam Ca(OH)2 vào 100 ml dung dịch HCl 2,0 M. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch có pH = 7. Giá trị của m là
A. 3,7. B. 29,6. C. 14,8. D. 7,4.
Câu 10: Với 75 ml dung dịch HNO3 2,0 M có thể hòa tan tối đa bao nhiêu gam kim loại Cu? Giả sử phản ứng chỉ tạo thành sản phẩm khử duy nhất là khí NO.
A. 3,60. B. 2,40. C. 9,60. D. 0,90.
---(Để xem tiếp nội dung từ câu 11 đến câu 15 phần trắc nghiệm và phần tự luận của đề thi số 5 các em vui lòng xem Online hoặc Đăng nhập vào HOC247 để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 5
|
1 |
B |
6 |
D |
11 |
C |
|
2 |
C |
7 |
A |
12 |
B |
|
3 |
A |
8 |
D |
13 |
D |
|
4 |
C |
9 |
D |
14 |
C |
|
5 |
C |
10 |
A |
15 |
A |
Trên đây là một phần trích dẫn nội dung Bộ 5 đề thi HK1 môn Hóa học 11 năm 2021-2022 có đáp án Trường THPT Bình Giang. Để xem toàn bộ nội dung các em đăng nhập vào trang hoc247.net để tải tài liệu về máy tính.
Hy vọng tài liệu này sẽ giúp các em học sinh ôn tập tốt và đạt thành tích cao trong học tập.
Ngoài ra các em có thể tham khảo thêm một số tư liệu cùng chuyên mục tại đây:
- Bộ 4 đề thi HK1 môn Hóa học 11 có đáp án năm 2021-2022 Trường THPT Phan Ngọc Hiển
- Bộ 5 đề thi HK1 môn Hóa học 11 có đáp án năm 2021-2022 Trường THPT Mạc Đỉnh Chi
Thi online
Tài liệu liên quan
Tư liệu nổi bật tuần
-
Đề thi minh họa môn Hóa học tốt nghiệp THPT năm 2025
22/10/20242022 -
Đề thi minh họa môn Tin học tốt nghiệp THPT năm 2025
22/10/2024754 -
Đề thi minh họa môn Toán tốt nghiệp THPT năm 2025
22/10/20241455 - Xem thêm




