Gửi đến các bạn học sinh Bộ 5 đề thi giữa HK1 môn Hóa học 11 năm 2021-2022 có đáp án Trường THPT Phụ Dực được chia sẻ dưới đây nhằm giúp các em có thêm tư liệu để tham khảo cũng như củng cố kiến thức trước khi bước vào kì thi. Cùng tham gia giải đề thi để ôn tập kiến thức và làm quen với cấu trúc đề thi các em nhé, chúc các em thi tốt!
|
TRƯỜNG THPT PHỤ DỰC |
ĐỀ THI GIỮA HỌC KÌ 1 MÔN HÓA HỌC 11 THỜI GIAN 45 PHÚT NĂM HỌC 2021-2022 |
ĐỀ SỐ 1
Câu 41: Các electron của nguyên tử nguyên tố X được phân bố trên 3 lớp, lớp thứ 3 có 5 electron. Số đơn vị điện tích hạt nhân nguyên tử của nguyên tố X là
A. 18. B. 10. C. 14. D. 15.
Câu 42: X là chất khí, không màu, không mùi, nặng hơn không khí. X là
A. oxi. B. clo. C. nitơ. D. Cacbonic.
Câu 43: Hóa chất cần dùng và cách thu khí để điều chế một lượng nhỏ N2 tinh khiết trong phòng thí nghiệm là?
A. NaNO2, phương pháp đẩy không khí.
B. Không khí, phương pháp chưng cất phân đoạn không khí lỏng.
C. NH4NO3, phương pháp đẩy nước.
D. NH4NO2, phương pháp đẩy nước.
Câu 44: Nhỏ dung dịch H2SO4 đặc vào đường saccarozơ (C12H22O11), hỗn hợp khí thu được sau phản ứng là
A. H2S và CO2. B. SO2 và CO2.
C. SO3 và CO2. D. H2S và SO2.
Câu 45: Chất nào dưới đây là chất điện li mạnh?
A. CH3COOH B. H3PO4. C. H2O. D. NaCl.
Câu 46: Nguyên tử X liên kết với nguyên tử Clo trong hợp chất bằng liên kết cộng hóa trị. Hỏi X không thể là nguyên tử nào sau đây?
A. Oxi. B. Kali. C. Hidro. D. Clo.
Câu 47: Đặc điểm chung của các đơn chất halogen (F2, Cl2, Br2, I2) là
A. vừa có tính oxi hóa vừa có tính khử. B. có tính oxi hóa mạnh.
C. tác dụng mạnh với nước. D. chất khí ở điều kiện thường.
Câu 48: Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân nguyên tử
A. tính kim loại tăng, tính phi kim tăng. B. tính kim loại giảm, tính phi kim giảm.
C. tính kim loại tăng, tính phi kim giảm. D. tính kim loại giảm, tính phi kim tăng.
Câu 49: Giá trị pH của dung dịch H2SO4 có [H+] = 0,01M là
A. 12. B. 10. C. 2. D. 4.
Câu 50: Để nhận biết 3 khí đựng trong 3 lọ mất nhãn riêng biêt bằng phương pháp hóa học: CO2, SO2, N2 cần dùng các dung dịch nào?
A. Br2 và NaOH. B. Br2 và Ca(OH)2.
C. NaOH và Ca(OH)2. D. KMnO4 và NaOH.
Câu 51: Cho phản ứng:MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O vai trò của MnO2 là
A. chất oxi hóa. B. chất khử.
C. chất khử và môi trường. D. chất bị oxi hóa.
Câu 52: Dung dịch chất nào sau đây không làm đổi màu quì tím?
A. NaOH. B. HCl. C. KCl. D. HNO3
Câu 53: Thực hiện 2 thí nghiệm theo hình vẽ sau:
.png?enablejsapi=1)
Hiện tượng quan sát được là
A. không có kết tủa xuất hiện. B. thí nghiệm 1 có kết tủa xuất hiện trước.
C. thí nghiệm 2 có kết tủa xuất hiện trước. D. kết tủa xuất hiện đồng thời.
Câu 54: Đun sôi bốn dung dịch, mỗi dung dịch chứa 1 mol mỗi chất sau: Ba(HCO3)2, Ca(HCO3)2, NaHCO3, Ba(HSO4)2 . Khi phản ứng xảy ra hoàn toàn, trường hợp nào khối lượng dung dịch giảm nhiều nhất (Giả sử nước bay hơi không đáng kể)?
A. Ba(HCO3)2. B. Ca(HCO3)2.
C. NaHCO3. D. Ba(HSO4)2.
Câu 55: Dung dịch chất điện li dẫn điện được là do trong dung dịch có chứa:
A. Các ion H+ và OH- chuyển động tự do B. Các electron chuyển động tự do.
C. Các cation và anion chuyển động tự do. D. Các ion được gắn cố định tại các nút mạng.
Câu 56: Sản phẩm của phản ứng Li và N2 là?
A. Li3N2. B. LiN. C. Li3N. D. Li5N.
Câu 57: Ở nhiệt độ thường, nitơ khá trơ về mặt hoạt động hóa học là do
A. nitơ có độ âm điện lớn nhất trong nhóm. B. phân tử nitơ không phân cực.
C. phân tử nitơ có liên kết ba rất bền. D. nitơ có bán kính nguyên tử nhỏ.
Câu 58: Muối nào sau đây là muối axit?
A. NH4NO3. B. CH3COOK.
C. Na3PO4. D. Ba(HCO3)2.
Câu 59: Phản ứng thuận nghịch là phản ứng:
A. chỉ xảy ra theo một chiều từ trái sang phải.
B. xảy ra theo hai chiều trái ngược nhau, trong điều kiện khác nhau.
C. xảy ra theo hai chiều trái ngược nhau, trong cùng điều kiện.
D. chỉ xảy ra theo một chiều từ phải sang trái.
Câu 60: Kim loại M tác dụng với dung dịch HCl loãng và khí Cl2 cho cùng một loại muối clorua. Kim loại M là
A. Fe. B. Ag. C. Mg. D. Cu.
Câu 61: Phản ứng nào sau đây có phương trình ion rút gọn: HCO3- + OH- → CO32- + H2O ?
A. 2NaHCO3 + 2KOH → Na2CO3 + K2CO3 + 2H2O
B. Ca(HCO3) + 2NaOH → CaCO3 + Na2CO3 + 2H2O
C. 2NaHCO3 + Ca(OH)2 → CaCO3 + Na2CO3 + 2H2O
D. NaHCO3 + HCl → NaCl + CO2 + H2O
Câu 62: Phản ứng sau đây thuộc loại nào: Fe + 2HCl → FeCl2 + H2.
A. phản ứng phân hủy. B. phản ứng hóa hợp.
C. phản ứng thế. D. phản ứng trao đổi.
Câu 63: Hiđroxit nào sau đây là chất lưỡng tính ?
A. Al(OH)3. B. Mg(OH)2. C. Fe(OH)3. D. NaOH.
Câu 64: Cho 31,6 gam KMnO4 tác dụng với dung dịch HCl dư tạo ra V lít Cl2 (ở đktc), hiệu suất của phản ứng là 75%. Giá trị của V là
A. 8,4. B. 4,8. C. 2,4. D. 4,2.
Câu 65: Cho sơ đồ phản ứng:
SO2 + KMnO4 + H2O → H2SO4 + K2SO4 + MnSO4
Tổng hệ số cân bằng (số nguyên, tối giản) của tất cả các chất tham gia phản ứng là
A. 14. B. 9. C. 7. D. 16.
Câu 66: Thực hiện các thí nghiệm sau:
(1) Cho dung dịch KI tác dụng với ozon.
(2) Dẫn khí F2 vào nước.
(3) Nhiệt phân amoni nitrit.
(4) Cho mẩu sắt vào dung dịch H2SO4 loãng nguội.
Số thí nghiệm tạo ra đơn chất là
A. 3. B. 2. C. 4. D. 1.
Câu 67: Hòa tan hoàn toàn 2,44 gam hỗn hợp bột X gồm FexOy và Cu bằng dung dịch H2SO4 đặc nóng, dư. Sau phản ứng thu được 0,504 lít khí SO2 (sản phẩm khử duy nhất, ở đktc) và dung dịch chứa 6,6 gam hỗn hợp muối sunfat. Phần trăm khối lượng của Cu trong X là
A. 65,57%. B. 39,34%. C. 13,11%. D. 26,23%.
Câu 68: Cho 200 ml dung dịch X chứa HCl 1M và HNO3 2M tác dụng với 300 ml dung dịch Y chứa NaOH 0,8 M và KOH a M thu được dung dịch Z. Biết rằng để trung hoà 100 ml dung dịch Z cần 60 ml dung dịch HCl 1 M. Tính khối lượng chất rắn thu được khi cô cạn toàn bộ dung dịch Z?
A. 68,26. B. 54,82. C. 63,16. D. 59,12.
Câu 69: Cho m gam hỗn hợp X gồm Fe, Fe3O4 và Fe(NO3)2 tan hết trong 320 ml dung dịch KHSO4 1M. Sau phản ứng thu được dung dịch Y chỉ chứa 61,4 gam muối trung hòa và 0,896 lít NO (đktc, sản phẩm khử duy nhất). Cho dung dịch NaOH dư vào Y thì có 0,46 mol NaOH phản ứng. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của Fe trong X gần giá trị nào nhất sau đây?
A. 5,0%. B. 3,5%. C. 3,0%. D. 2,0%.
Câu 70: Cho các dung dịch riêng biệt: Na2CO3, BaCl2, MgCl2, H2SO4, NaOH được đánh số ngẫu nhiên (1), (2), (3), (4), (5). Tiến hành các thí nghiệm, kết quả được ghi lại trong bảng sau:
|
Dung dịch |
(1) |
(2) |
(4) |
(5) |
|
(1) |
- |
khí thoát ra |
có kết tủa |
- |
|
(2) |
khí thoát ra |
- |
có kết tủa |
có kết tủa |
|
(4) |
có kết tủa |
có kết tủa |
- |
- |
|
(5) |
- |
có kết tủa |
- |
- |
Chú thích: “–“ là không có hiện tượng
Phát biểu nào sau đây là đúng?
A. Các dung dịch (1), (3), (5) lần lượt là H2SO4, MgCl2, BaCl2.
B. Các dung dịch (1), (2), (4) lần lượt là Na2CO3, H2SO4, BaCl2
C. Các dung dịch (2), (3), (4) lần lượt là: BaCl2, NaOH, Na2CO3.
D. Các dung dịch (1), (3), (5) lần lượt là H2SO4, NaOH, MgCl2.
Câu 71: Oxi hoá hoàn toàn a gam hỗn hợp Mg, Zn và Al thu được b gam hỗn hợp oxít. Cho hỗn hợp kim loại trên tác dụng với dung dịch H2SO4 loãng, dư thu được V lít khí (đktc). V có giá trị tính theo a, b là
A. 22,4(b-a)/32. B. 22,4(b-a)/16.
C. 22,4(a-b)/32. D. 11,2(b-a)/16.
Câu 72: Hoà tan hết 9,6 gam kim loại M trong dung dịch H2SO4 đặc, nóng, thu được SO2 (sản phẩm khử duy nhất), dẫn toàn bộ lượng khí SO2 cho hấp thụ hết vào 0,5 lít dung dịch NaOH 0,6 M. Sau phản ứng, đem cô cạn dung dịch được 18,9 gam chất rắn. Kim loại M là
A. Fe. B. Cu. C. Mg. D. Ca.
Câu 73: Cho từ từ đến dư dung dịch NaOH vào dung dịch X chứa hỗn hợp Al(NO3)3, HCl, HNO3. Kết quả thí nghiệm được biểu diễn trên đồ thị sau:
.png)
Giá trị của a là
A. 0,8. B. 1,2. C. 1,5. D. 1,25.
Câu 74: Thổi một luồng CO qua hỗn hợp Fe và Fe2O3 nung nóng được chất khí X và hỗn hợp Y gồm Fe, FeO, Fe2O3, Fe3O4. Cho X lội qua dung dịch nước vôi trong dư thấy tạo 6 gam kết tủa. Hoà tan Y bằng H2SO4 đặc, nóng thấy tạo ra 0,18 mol SO2 còn dung dịch Z. Cô cạn Z thu được 24 gam muối khan. Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là
A. 58,33%. B. 41,67%. C. 50%. D. 40%.
Câu 75: Tiến hành các thí nghiệm sau:
(a) Sục khí Cl2 vào dung dịch NaOH ở nhiệt độ thường.
(b) Cho mẩu Fe vào dung dịch CuSO4 dư.
(c) Cho hỗn hợp NaHSO4 và NaHCO3 (tỉ lệ mol 1 : 1) vào nước.
(d) Cho dung dịch K2Cr2O7 vào dung dịch HCl dư.
(e) Sục khí NO2 vào dung dịch KOH.
(g) Dung dịch Ba(HSO4)2 tác dụng với dung dịch NaOH dư.
Sau khi các phản ứng kết thúc, số thí nghiệm mà dung dịch thu được có hai muối là
A. 4. B. 2. C. 5. D. 3.
Câu 76: Dung dịch X gồm 0,3 mol K+; 0,6 mol Mg2+; 0,3 mol Na+; 0,6 mol Cl- và a mol Y2-. Cô cạn dung dịch X, thu được m gam muối khan. Ion Y2- và giá trị của m là
A. và 169,5. B. và 126,3.
C. và 90,3. D. và 111,9.
Câu 77: Cho m gam kim loại M vào dung dịch NH4NO3 đến khi phản ứng xảy ra hoàn toàn thu được 6,72 lít hỗn hợp khí (đktc) và dung dịch X chứa 26,1 gam một chất tan duy nhất. (coi các khí thoát ra khỏi dung dịch hoàn toàn).Vậy M là
A. Ca. B. Cu. C. Mg. D. Ba.
Câu 78: Đổ 10 ml dung dịch KOH vào 15 ml dung dịch H2SO4 0,5M, dung dịch vẫn dư axit. Thêm 3 ml dung dịch NaOH 1M vào thì dung dịch trung hoà. Nồng độ mol/l của dung dịch KOH là
A. 0,75 M. B. 1,2 M. C. 0,9 M. D. 0,6 M.
Câu 79: Trộn 250 ml dung dịch hỗn hợp HBr 0,5 M và H2SO4 0,1 M với 250 ml dung dịch Ba(OH)2 có nồng độ a M thu được m gam kết tủa và 500 ml dung dịch có pH=11. Giá trị của a và m lần lượt là:
A. 0,5 M; 0,5825 g. B. 0,351 M; 0,5825 g. C. 0,351M; 5,825 g. D. 0,5 M; 5,825g.
Câu 80: Cho 17,04 gam hỗn hợp rắn X gồm Ca, MgO, Na2O tác dụng hết với 720 ml dung dịch HCl 1M (vừa đủ) thu được dung dịch Y. Khối lượng muối NaCl có trong dung dich Y là
A. 15,21 gam. B. 14,04 gam. C. 4,68 gam. D. 8,775 gam.
ĐÁP ÁN ĐỀ SỐ 1
|
41 |
D |
51 |
A |
61 |
A |
71 |
B |
|
42 |
A - D |
52 |
C |
62 |
C |
72 |
B |
|
43 |
D |
53 |
B |
63 |
A |
73 |
D |
|
44 |
B |
54 |
A |
64 |
A |
74 |
A |
|
45 |
D |
55 |
C |
65 |
B |
75 |
A |
|
46 |
B |
56 |
C |
66 |
C |
76 |
D |
|
47 |
B |
57 |
C |
67 |
D |
77 |
D |
|
48 |
D |
58 |
D |
68 |
A |
78 |
B |
|
49 |
C |
59 |
C |
69 |
A |
79 |
C |
|
50 |
B |
60 |
C |
70 |
D |
80 |
B |
ĐỀ SỐ 2
Câu 41: Để nhận biết 3 khí đựng trong 3 lọ mất nhãn riêng biêt bằng phương pháp hóa học: CO2, SO2, N2 cần dùng các dung dịch nào?
A. NaOH và Ca(OH)2. B. Br2 và Ca(OH)2.
C. KMnO4 và NaOH. D. Br2 và NaOH.
Câu 42: Đun sôi bốn dung dịch, mỗi dung dịch chứa 1 mol mỗi chất sau: Ba(HCO3)2, Ca(HCO3)2, NaHCO3, Ba(HSO4)2 . Khi phản ứng xảy ra hoàn toàn, trường hợp nào khối lượng dung dịch giảm nhiều nhất (Giả sử nước bay hơi không đáng kể)?
A. NaHCO3. B. Ca(HCO3)2.
C. Ba(HSO4)2. D. Ba(HCO3)2.
Câu 43: Nhỏ dung dịch H2SO4 đặc vào đường saccarozơ (C12H22O11), hỗn hợp khí thu được sau phản ứng là
A. H2S và SO2. B. SO2 và CO2.
C. SO3 và CO2. D. H2S và CO2.
Câu 44: Các electron của nguyên tử nguyên tố X được phân bố trên 3 lớp, lớp thứ 3 có 5 electron. Số đơn vị điện tích hạt nhân nguyên tử của nguyên tố X là
A. 18. B. 15. C. 10. D. 14.
Câu 45: Thực hiện 2 thí nghiệm theo hình vẽ sau:
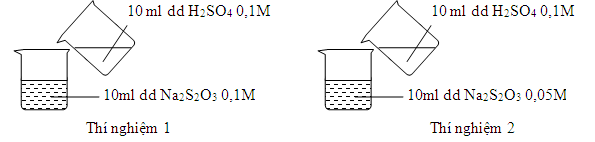
Hiện tượng quan sát được là
A. không có kết tủa xuất hiện. B. thí nghiệm 2 có kết tủa xuất hiện trước.
C. kết tủa xuất hiện đồng thời. D. thí nghiệm 1 có kết tủa xuất hiện trước.
Câu 46: Kim loại M tác dụng với dung dịch HCl loãng và khí Cl2 cho cùng một loại muối clorua. Kim loại M là
A. Fe. B. Ag. C. Mg. D. Cu.
Câu 47: Chất nào dưới đây là chất điện li mạnh?
A. CH3COOH B. H2O. C. NaCl. D. H3PO4.
Câu 48: Cho 31,6 gam KMnO4 tác dụng với dung dịch HCl dư tạo ra V lít Cl2 (ở đktc), hiệu suất của phản ứng là 75%. Giá trị của V là
A. 4,8. B. 8,4. C. 2,4. D. 4,2.
Câu 49: Cho phản ứng:MnO2 + 4HCl MnCl2 + Cl2 + 2H2O vai trò của MnO2 là
A. chất khử. B. chất khử và môi trường.
C. chất oxi hóa. D. chất bị oxi hóa.
Câu 50: Sản phẩm của phản ứng Li và N2 là?
A. Li3N. B. LiN. C. Li5N. D. Li3N2.
---(Để xem đầy đủ, chi tiết của tài liệu vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 2
|
41 |
B |
51 |
D |
61 |
A |
71 |
A |
|
42 |
D |
52 |
D |
62 |
D |
72 |
C |
|
43 |
B |
53 |
B |
63 |
D |
73 |
C |
|
44 |
B |
54 |
D |
64 |
D |
74 |
A |
|
45 |
D |
55 |
A |
65 |
C |
75 |
C |
|
46 |
C |
56 |
C - B |
66 |
B |
76 |
C |
|
47 |
C |
57 |
A |
67 |
C |
77 |
B |
|
48 |
B |
58 |
B |
68 |
A |
78 |
A |
|
49 |
C |
59 |
D |
69 |
B |
79 |
D |
|
50 |
A |
60 |
A |
70 |
A |
80 |
B |
ĐỀ SỐ 3
Câu 41: Đặc điểm chung của các đơn chất halogen (F2, Cl2, Br2, I2) là
A. chất khí ở điều kiện thường. B. tác dụng mạnh với nước.
C. có tính oxi hóa mạnh. D. vừa có tính oxi hóa vừa có tính khử.
Câu 42: Chất nào dưới đây là chất điện li mạnh?
A. CH3COOH B. NaCl. C. H2O. D. H3PO4.
Câu 43: Cho phản ứng:MnO2 + 4HCl MnCl2 + Cl2 + 2H2O vai trò của MnO2 là
A. chất oxi hóa. B. chất khử.
C. chất bị oxi hóa. D. chất khử và môi trường.
Câu 44: Giá trị pH của dung dịch H2SO4 có [H+] = 0,01M là
A. 12. B. 10. C. 2. D. 4.
Câu 45: Thực hiện 2 thí nghiệm theo hình vẽ sau:

Hiện tượng quan sát được là
A. không có kết tủa xuất hiện. B. thí nghiệm 2 có kết tủa xuất hiện trước.
C. kết tủa xuất hiện đồng thời. D. thí nghiệm 1 có kết tủa xuất hiện trước.
Câu 46: Nguyên tử X liên kết với nguyên tử Clo trong hợp chất bằng liên kết cộng hóa trị. Hỏi X không thể là nguyên tử nào sau đây?
A. Oxi. B. Kali. C. Hidro. D. Clo.
Câu 47: Dung dịch chất nào sau đây không làm đổi màu quì tím?
A. NaOH. B. KCl. C. HNO3 D. HCl.
Câu 48: Kim loại M tác dụng với dung dịch HCl loãng và khí Cl2 cho cùng một loại muối clorua. Kim loại M là
A. Fe. B. Ag. C. Cu. D. Mg.
Câu 49: Hiđroxit nào sau đây là chất lưỡng tính ?
A. Al(OH)3. B. Mg(OH)2. C. Fe(OH)3. D. NaOH.
Câu 50: Muối nào sau đây là muối axit?
A. CH3COOK. B. NH4NO3. C. Ba(HCO3)2. D. Na3PO4.
---(Để xem đầy đủ, chi tiết của tài liệu vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 3
|
41 |
C |
51 |
C |
61 |
D |
71 |
B |
|
42 |
B |
52 |
D - C |
62 |
A |
72 |
B |
|
43 |
A |
53 |
C |
63 |
A |
73 |
D |
|
44 |
C |
54 |
D |
64 |
D |
74 |
B |
|
45 |
D |
55 |
A |
65 |
C |
75 |
A |
|
46 |
B |
56 |
C |
66 |
B |
76 |
A |
|
47 |
B |
57 |
C |
67 |
D |
77 |
C |
|
48 |
D |
58 |
A |
68 |
A |
78 |
C |
|
49 |
A |
59 |
D |
69 |
D |
79 |
B |
|
50 |
C |
60 |
B |
70 |
B |
80 |
A |
ĐỀ SỐ 4
Câu 41: Nguyên tử X liên kết với nguyên tử Clo trong hợp chất bằng liên kết cộng hóa trị. Hỏi X không thể là nguyên tử nào sau đây?
A. Oxi. B. Hidro. C. Clo. D. Kali.
Câu 42: Ở nhiệt độ thường, nitơ khá trơ về mặt hoạt động hóa học là do
A. phân tử nitơ có liên kết ba rất bền. B. nitơ có bán kính nguyên tử nhỏ.
C. nitơ có độ âm điện lớn nhất trong nhóm. D. phân tử nitơ không phân cực.
Câu 43: X là chất khí, không màu, không mùi, nặng hơn không khí. X là
A. oxi. B. clo. C. Cacbonic. D. nitơ.
Câu 44: Thực hiện 2 thí nghiệm theo hình vẽ sau:

Hiện tượng quan sát được là
A. không có kết tủa xuất hiện. B. kết tủa xuất hiện đồng thời.
C. thí nghiệm 2 có kết tủa xuất hiện trước. D. thí nghiệm 1 có kết tủa xuất hiện trước.
Câu 45: Để nhận biết 3 khí đựng trong 3 lọ mất nhãn riêng biêt bằng phương pháp hóa học: CO2, SO2, N2 cần dùng các dung dịch nào?
A. Br2 và Ca(OH)2. B. NaOH và Ca(OH)2.
C. Br2 và NaOH. D. KMnO4 và NaOH.
Câu 46: Phản ứng sau đây thuộc loại nào: Fe + 2HCl → FeCl2 + H2.
A. phản ứng trao đổi. B. phản ứng thế.
C. phản ứng hóa hợp. D. phản ứng phân hủy.
Câu 47: Muối nào sau đây là muối axit?
A. Na3PO4. B. NH4NO3.
C. Ba(HCO3)2. D. CH3COOK.
Câu 48: Hiđroxit nào sau đây là chất lưỡng tính ?
A. Mg(OH)2. B. Al(OH)3. C. Fe(OH)3. D. NaOH.
Câu 49: Đun sôi bốn dung dịch, mỗi dung dịch chứa 1 mol mỗi chất sau: Ba(HCO3)2, Ca(HCO3)2, NaHCO3, Ba(HSO4)2 . Khi phản ứng xảy ra hoàn toàn, trường hợp nào khối lượng dung dịch giảm nhiều nhất (Giả sử nước bay hơi không đáng kể)?
A. Ca(HCO3)2. B. NaHCO3.
C. Ba(HSO4)2. D. Ba(HCO3)2.
Câu 50: Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân nguyên tử
A. tính kim loại tăng, tính phi kim giảm. B. tính kim loại tăng, tính phi kim tăng.
C. tính kim loại giảm, tính phi kim tăng. D. tính kim loại giảm, tính phi kim giảm.
---(Để xem đầy đủ, chi tiết của tài liệu vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 4
|
41 |
D |
51 |
A |
61 |
A |
71 |
C |
|
42 |
A |
52 |
A |
62 |
B |
72 |
D |
|
43 |
A- C |
53 |
C |
63 |
A |
73 |
D |
|
44 |
D |
54 |
B |
64 |
B |
74 |
A |
|
45 |
A |
55 |
A |
65 |
A |
75 |
C |
|
46 |
B |
56 |
C |
66 |
C |
76 |
B |
|
47 |
C |
57 |
C |
67 |
D |
77 |
B |
|
48 |
B |
58 |
C |
68 |
C |
78 |
B |
|
49 |
D |
59 |
B |
69 |
D |
79 |
B |
|
50 |
C |
60 |
D |
70 |
D |
80 |
D |
ĐỀ SỐ 5
Câu 41: Đun sôi bốn dung dịch, mỗi dung dịch chứa 1 mol mỗi chất sau: Ba(HCO3)2, Ca(HCO3)2, NaHCO3, Ba(HSO4)2 . Khi phản ứng xảy ra hoàn toàn, trường hợp nào khối lượng dung dịch giảm nhiều nhất (Giả sử nước bay hơi không đáng kể)?
A. Ca(HCO3)2. B. NaHCO3.
C. Ba(HSO4)2. D. Ba(HCO3)2.
Câu 42: Thực hiện 2 thí nghiệm theo hình vẽ sau:

Hiện tượng quan sát được là
A. không có kết tủa xuất hiện. B. kết tủa xuất hiện đồng thời.
C. thí nghiệm 2 có kết tủa xuất hiện trước. D. thí nghiệm 1 có kết tủa xuất hiện trước.
Câu 43: Nhỏ dung dịch H2SO4 đặc vào đường saccarozơ (C12H22O11), hỗn hợp khí thu được sau phản ứng là
A. SO3 và CO2. B. SO2 và CO2.
C. H2S và CO2. D. H2S và SO2.
Câu 44: Hóa chất cần dùng và cách thu khí để điều chế một lượng nhỏ N2 tinh khiết trong phòng thí nghiệm là?
A. Không khí, phương pháp chưng cất phân đoạn không khí lỏng.
B. NaNO2, phương pháp đẩy không khí.
C. NH4NO2, phương pháp đẩy nước.
D. NH4NO3, phương pháp đẩy nước.
Câu 45: Để nhận biết 3 khí đựng trong 3 lọ mất nhãn riêng biêt bằng phương pháp hóa học: CO2, SO2, N2 cần dùng các dung dịch nào?
A. Br2 và Ca(OH)2. B. NaOH và Ca(OH)2.
C. Br2 và NaOH. D. KMnO4 và NaOH.
Câu 46: Cho sơ đồ phản ứng:
SO2 + KMnO4 + H2O → H2SO4 + K2SO4 + MnSO4
Tổng hệ số cân bằng (số nguyên, tối giản) của tất cả các chất tham gia phản ứng là
A. 7. B. 14. C. 16. D. 9.
Câu 47: Nguyên tử X liên kết với nguyên tử Clo trong hợp chất bằng liên kết cộng hóa trị. Hỏi X không thể là nguyên tử nào sau đây?
A. Hidro. B. Kali. C. Clo. D. Oxi.
Câu 48: Muối nào sau đây là muối axit?
A. CH3COOK. B. NH4NO3.
C. Na3PO4. D. Ba(HCO3)2.
Câu 49: Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân nguyên tử
A. tính kim loại tăng, tính phi kim giảm. B. tính kim loại tăng, tính phi kim tăng.
C. tính kim loại giảm, tính phi kim tăng. D. tính kim loại giảm, tính phi kim giảm.
Câu 50: Dung dịch chất điện li dẫn điện được là do trong dung dịch có chứa:
A. Các electron chuyển động tự do.
B. Các ion H+ và OH- chuyển động tự do
C. Các cation và anion chuyển động tự do.
D. Các ion được gắn cố định tại các nút mạng.
---(Để xem đầy đủ, chi tiết của tài liệu vui lòng xem tại online hoặc đăng nhập để tải về máy)---
ĐÁP ÁN ĐỀ SỐ 5
|
41 |
D |
51 |
A |
61 |
A |
71 |
D |
|
42 |
D |
52 |
D |
62 |
B |
72 |
A |
|
43 |
B |
53 |
A |
63 |
B |
73 |
A |
|
44 |
C |
54 |
B |
64 |
B |
74 |
D |
|
45 |
A |
55 |
B |
65 |
C |
75 |
B |
|
46 |
D |
56 |
C |
66 |
C |
76 |
C |
|
47 |
B |
57 |
A |
67 |
B |
77 |
C |
|
48 |
D |
58 |
B |
68 |
A |
78 |
A |
|
49 |
C |
59 |
D-C |
69 |
D |
79 |
D |
|
50 |
C |
60 |
C |
70 |
C |
80 |
A |
Trên đây là một phần trích dẫn nội dung Bộ 5 đề thi giữa HK1 môn Hóa học 11 năm 2021-2022 có đáp án Trường THPT Phụ Dực. Để xem toàn bộ nội dung các em đăng nhập vào trang hoc247.net để tải tài liệu về máy tính.
Hy vọng tài liệu này sẽ giúp các em học sinh ôn tập tốt và đạt thành tích cao trong học tập.
Ngoài ra các em có thể tham khảo thêm một số tư liệu cùng chuyên mục tại đây:
- Bộ 5 đề thi giữa HK1 môn Hóa học 11 có đáp án năm 2021-2022 Trường THPT Nguyễn Thị Định
- Bộ 5 đề thi giữa HK1 môn Hóa học 11 năm 2021 - 2022 có đáp án Trường THPT Lang Chánh
Chúc các em học tốt!
Tài liệu liên quan
Tư liệu nổi bật tuần
-
Đề thi minh họa môn Hóa học tốt nghiệp THPT năm 2025
22/10/20242033 -
Đề thi minh họa môn Tin học tốt nghiệp THPT năm 2025
22/10/2024754 -
Đề thi minh họa môn Toán tốt nghiệp THPT năm 2025
22/10/20241460 - Xem thêm




