HOC247 xin giŠĽõi thiŠĽáu ńĎŠļŅn c√°c em hŠĽćc sinh t√†i liŠĽáu BŠĽô ńĎŠĽĀ kiŠĽÉm tra 1 tiŠļŅt Ch∆į∆°ng 2 m√īn H√≥a hŠĽćc 11 nńÉm hŠĽćc 2019-2020 Tr∆įŠĽĚng THPT Nam S√°ch. ńźŠĽĀ kiŠĽÉm tra bao gŠĽďm 24 c√Ęu hŠĽŹi trŠļĮc nghiŠĽám v√† 3 c√Ęu hŠĽŹi tŠĽĪ luŠļ≠n ho√†n th√†nh trong thŠĽĚi gian 45 ph√ļt. Hy vŠĽćng ńĎŠĽĀ thi n√†y sŠļĹ gi√ļp c√°c em √īn tŠļ≠p hiŠĽáu quŠļ£ h∆°n v√† ńĎŠļ°t kŠļŅt quŠļ£ cao ŠĽü b√†i kiŠĽÉm tra sŠļĮp tŠĽõi.
|
TR∆ĮŠĽúNG THPT NAM S√ĀCH |
ńźŠĽÄ KIŠĽāM TRA 1 TIŠļĺT CH∆Į∆†NG 2 M√ĒN H√ďA HŠĽĆC 11 NńāM HŠĽĆC 2019-2020 |
ńźŠĽÄ 1:
PHŠļ¶N I: TRŠļģC NGHIŠĽÜM
C√Ęu 1: ńźŠĽÉ nhŠļ≠n biŠļŅt dung dŠĽčch amoniac, ng∆įŠĽĚi ta ńĎ∆įa ńĎŠļßu ńĎŇ©a thŠĽßy tinh c√≥ tŠļ©m h√≥a chŠļ•t v√†o miŠĽáng lŠĽć ńĎŠĽĪng dung dŠĽčch amoniac. H√≥a chŠļ•t ńĎ∆įŠĽ£c d√Ļng l√†
A. dung dŠĽčch HCl. B. dung dŠĽčch KOH. C. dung dŠĽčch NaCl. D. dung dŠĽčch KNO3.
C√Ęu 2: NŠļ°p ńĎŠļßy kh√≠ amoniac v√†o b√¨nh thŠĽßy tinh, ńĎŠļ≠y bŠļĪng n√ļt cao su c√≥ ŠĽĎng thŠĽßy tinh vuŠĽĎt nhŠĽćn. Nh√ļng ńĎŠļßu ŠĽĎng thŠĽßy tinh v√†o mŠĽôt chŠļ≠u n∆įŠĽõc c√≥ pha dung dŠĽčch phenolphtalein. HiŠĽán t∆įŠĽ£ng g√¨ sŠļĹ xŠļ£y ra?
A. Kh√≠ trong b√¨nh thŠĽßy tinh chuyŠĽÉn th√†nh m√†u hŠĽďng
B. N∆įŠĽõc trong chŠļ≠u tŠĽę kh√īng m√†u chuyŠĽÉn th√†nh m√†u hŠĽďng
C. N∆įŠĽõc trong chŠļ≠u phun v√†o b√¨nh thŠĽßy tinh th√†nh nhŠĽĮng tia m√†u hŠĽďng
D. N∆įŠĽõc tŠĽę chŠļ≠u tr√†n v√†o b√¨nh thŠĽßy tinh
C√Ęu 3: NhŠļ≠n x√©t n√†o sau ńĎ√Ęy l√† sai?
A. Trong axit nitric, nit∆° h√≥a trŠĽč 4
B. Trong axit nitric, nit∆° h√≥a trŠĽč 5
C. Nit∆° c√≥ sŠĽĎ oxi h√≥a +5 trong axit nitric
D. C√≥ 1 li√™n kŠļŅt cho nhŠļ≠n trong c√īng thŠĽ©c cŠļ•u tŠļ°o cŠĽßa axit nitric
C√Ęu 4: NhŠļ≠n biŠļŅt NH4Cl, (NH4)2SO4, NaNO3
A. BaCl2 B. AgCl C. NaOH D. Ba(OH)2
C√Ęu 5: NhiŠĽát ph√Ęn AgNO3 thu ńĎ∆įŠĽ£c c√°c chŠļ•t thuŠĽôc ph∆į∆°ng √°n n√†o:
A. Ag2O, O2 B. Ag2O, NO2 , O2 C. Ag2O, NO2 D. Ag, NO2 ,O2
C√Ęu 6: Cho 3,2 gam Cu t√°c dŠĽ•ng vŠĽõi 100ml dung dŠĽčch hŠĽón hŠĽ£p HNO3 0,8M v√† H2SO4 0,2M thu ńĎ∆įŠĽ£c V lit (ńĎktc) kh√≠ NO sŠļ£n phŠļ©m khŠĽ≠ duy nhŠļ•t. Gi√° trŠĽč cŠĽßa V l√†
A. 0,672 B. 0,448 C. 0,224 D. 0,336
C√Ęu 7: Cho 38,4 g Cu tan trong 2,4 l√≠t dd HNO3 0,5M thu ńĎ∆įŠĽ£c V l√≠t NO(ńĎktc, sŠļ£n phŠļ©m duy nhŠļ•t). Gi√° trŠĽč cŠĽßa V l√†: A. 4,48 B. 6,72 C. 8,96 D. 5,6
C√Ęu 8:Trong ph∆į∆°ng tr√¨nh h√≥a hŠĽćc cŠĽßa phŠļ£n ŠĽ©ng nhiŠĽát ph√Ęn sŠļĮt (III) nitrat, tŠĽēng c√°c hŠĽá sŠĽĎ bŠļĪng bao nhi√™u?
A. 5 B. 7 C.9 D.2
C√Ęu 9: Kh√≠ nit∆° c√≥ thŠĽÉ ńĎ∆įŠĽ£c tŠļ°o th√†nh phŠļ£n ŠĽ©ng h√≥a hŠĽćc n√†o sau ńĎ√Ęy?
A. ńźŠĽĎt ch√°y NH3 trong Oxi c√≥ chŠļ•t x√ļc t√°c platin B. NhiŠĽát ph√Ęn NH4NO3
C. NhiŠĽát ph√Ęn AgNO3 D. NhiŠĽát ph√Ęn NH4NO2
C√Ęu 10: Ph∆į∆°ng tr√¨nh phŠļ£n ŠĽ©ng giŠĽĮa Ag v√† HNO3 lo√£ng. TŠĽēng c√°c hŠĽá sŠĽĎ trong ph∆į∆°ng tr√¨nh h√≥a hŠĽćc l√†:
A. 12 B. 14 C. 13 D. 15
C√Ęu 11: ńźŠĽĎt ch√°y ho√†n to√†n 6,2 gam photpho trong oxi d∆į. Cho sŠļ£n phŠļ©m tŠļ°o th√†nh t√°c dŠĽ•ng vŠĽęa ńĎŠĽß vŠĽõi dung dŠĽčch NaOH 32% tŠļ°o th√†nh muŠĽĎi Na2HPO4. T√¨m khŠĽĎi l∆įŠĽ£ng dung dŠĽčch NaOH ńĎ√£ d√Ļng?
A. 24 gam B. 75 gam C. 50 gam D. 16 gam
C√Ęu 12: Cho 3,2 gam Cu t√°c dŠĽ•ng hŠļŅt vŠĽõi dung dŠĽčch HNO3 ńĎŠļ∑c. ThŠĽÉ t√≠ch kh√≠ NO2 (ńĎktc) l√†
A. 1,12 lít B. 3,36 lít C. 4,48 lít D. 2,24 lít
C√Ęu 13: Ph∆į∆°ng ph√°p phŠļ£n ŠĽ©ng n√†o sau d√Ļng ńĎŠĽÉ ńĎiŠĽĀu chŠļŅ nit∆° trong c√īng nghiŠĽáp.
A. TŠļ•t cŠļ£ ńĎŠĽĀu sai.
B. NH4NO3 ‚Üí N2 + 2H2O
C. Ch∆įng ph√Ęn ńĎoŠļ°n kh√īng kh√≠ lŠĽŹng ńĎŠĽÉ t√°ch N2 khŠĽŹi hŠĽón hŠĽ£p kh√īng kh√≠ lŠĽŹng
D. NH3 ‚Üí N2 + H2
C√Ęu 14: PhŠļ£i d√Ļng bao nhi√™u l√≠t kh√≠ nit∆° v√† bao nhi√™u l√≠t kh√≠ hidro ńĎŠĽÉ ńĎiŠĽĀu chŠļŅ 8,5 g NH3? BiŠļŅt rŠļĪng hiŠĽáu suŠļ•t chuyŠĽÉn h√≥a th√†nh amoniac l√† 25%. C√°c thŠĽÉ t√≠ch ńĎ∆įŠĽ£c ńĎo ŠĽü ńĎktc.
A. 22,4 lít N2 và 67,2 lít H2 B. 44,8 lít N2 và 134,4 lít H2
C. 22,4 lít N2 và 134,4 lít H2 D. 44,8 lít N2 và 67,2 lít H2
C√Ęu 15: Kim loŠļ°i M phŠļ£n ŠĽ©ng dd HCl, dd Cu(NO¬≠3)2,dd HNO3 ńĎŠļ∑c nguŠĽôi. Kim loŠļ°i M l√†:
A. Al B. Ag C. Fe D. Zn
C√Ęu 16: CŠļ∑p c√īng thŠĽ©c cŠĽßa liti nitrua v√† nh√īm nitrua l√†
A. Li3N, AlN B. Li2N3, Al2N3 C. Li3N2, Al3N2 D. LiN3, Al3N.
C√Ęu 17: Trong nhŠĽĮng nhŠļ≠n x√©t d∆įŠĽõi ńĎ√Ęy, nhŠļ≠n x√©t n√†o l√† kh√īngńĎ√ļng?
A. SŠĽĎ hiŠĽáu nguy√™n tŠĽ≠ cŠĽßa nito bŠļĪng 7.
B. CŠļ•u h√¨nh e cŠĽßa N l√†: 1s22s22p3
C. Ba electron ŠĽü ph√Ęn lŠĽõp 2p cŠĽßa N c√≥ thŠĽÉ tŠļ°o ńĎ∆įŠĽ£c 3 li√™n kŠļŅt cŠĽông h√≥a trŠĽč vŠĽõi c√°c nguy√™n tŠĽ≠ kh√°c.
D. Nguy√™n tŠĽ≠ N c√≥ hai lŠĽõp electron v√† lŠĽõp ngo√†i c√Ļng c√≥ 3 electron.
C√Ęu 18: Trong hŠĽ£p chŠļ•t n√†o sau ńĎ√Ęy nit∆° c√≥ sŠĽĎ oxi h√≥a cao nhŠļ•t?
A. NH4Cl B. N2O5 C. NO2 D. Mg3N2
C√Ęu 19: D√£y n√†o d∆įŠĽõi ńĎ√Ęy gŠĽďm c√°c chŠļ•t m√† nguy√™n tŠĽĎ nit∆° c√≥ khŠļ£ nńÉng vŠĽęa thŠĽÉ hiŠĽán t√≠nh khŠĽ≠ vŠĽęa thŠĽÉ hiŠĽán t√≠nh oxi h√≥a khi tham gia phŠļ£n ŠĽ©ng?
A. NH3, N2O5, N2, NO2 B. NH3, NO, HNO3, N2O5
C. NO2, N2, NO, N2O3 D. N2, NO, N2O, N2O5
C√Ęu 20: ChŠļ•t c√≥ thŠĽÉ d√Ļng ńĎŠĽÉ l√†m kh√ī kh√≠ NH3 l√†
A. H2SO4 ńĎŠļ∑c B. P2O5 C. CuSO4 khan D. KOH rŠļĮn
C√Ęu 21: Cho Cu v√†o dung dŠĽčch H2SO4 lo√£ng. Cu sŠļĹ tan nŠļŅu th√™m v√†o ńĎ√≥.
A. MuŠĽĎi KNO3 B. Kh√≠ O2
C. Dung dŠĽčch HNO3 D. TŠļ•t cŠļ£ ńĎŠĽĀu ńĎ√ļng
C√Ęu 22: H√≤a tan 12,8g kim loŠļ°i h√≥a trŠĽč II trong 1 l∆įŠĽ£ng vŠĽęa ńĎŠĽß dung dŠĽčch HNO3 60% (D = 1,365g/ml), thu ńĎ∆įŠĽ£c 8,96 l√≠t (ńĎktc) mŠĽôt kh√≠ duy nhŠļ•t m√†u n√Ęu ńĎŠĽŹ. T√™n cŠĽßa kim loŠļ°i v√† thŠĽÉ t√≠ch dung dŠĽčch HNO3 ńĎ√£ phŠļ£n ŠĽ©ng l√†:
A. ńĎŠĽďng; 61,5ml B. ch√¨; 65,1 ml C. thŠĽßy ng√Ęn;125,6 ml D. sŠļĮt; 82,3 ml
C√Ęu 23: Th√™m 0,15 mol KOH v√†o dung dŠĽčch chŠĽ©a 0,1 mol H3PO4. sau phŠļ£n ŠĽ©ng dung dŠĽčch c√≥ c√°c muŠĽĎi:
A.KH2PO4 và K2HPO4 B. K2HPO4 và K3PO4
C. KH2PO4 và K3PO4 D. KH2PO4, K2HPO4 và K3PO4
C√Ęu 24: ńźŠĽÉ m gam Fe ngo√†i kh√īng kh√≠ sau thŠĽĚi gian ńĎ∆įŠĽ£c 12g hŠĽón hŠĽ£p B gŠĽďm Fe, FeO, Fe2O3, Fe3O4. Cho hŠĽón hŠĽ£p B t√°c dŠĽ•ng vŠĽõi HNO3 th√¨ ńĎ∆įŠĽ£c 2,24 l√≠t NO (ńĎktc). Gi√° trŠĽč cŠĽßa m l√†
A. 11,8 B. 10,08 C. 9,8 D. 8,8
----(ńźŠĽÉ xem nŠĽôi dung phŠļßn tŠĽĪ luŠļ≠n ńĎŠĽĀ sŠĽĎ 1 vui l√≤ng xem tŠļ°i online hoŠļ∑c ńĎńÉng nhŠļ≠p ńĎŠĽÉ tŠļ£i vŠĽĀ m√°y)----
ńźŠĽÄ 2:
PHŠļ¶N I: TRŠļģC NGHIŠĽÜM
C√Ęu 1: CŠļ•u h√¨nh ngo√†i c√Ļng cŠĽßa c√°c nguy√™n tŠĽĎ nh√≥m Nit∆° (nh√≥m VA) l√†
A. ns2 np5 B. ns2 np3
C. (n-1)s2 np3 C. (n-1)d10 ns2 np3
C√Ęu 2: Trong nh√≥m N, ńĎi tŠĽę N ńĎŠļŅn Bi, ńĎiŠĽĀu khŠļ≥ng ńĎŠĽčnh n√†o sau ńĎ√Ęy l√† sai?
A. NńÉng l∆įŠĽ£ng ion ho√° giŠļ£m
B. ńźŠĽô √Ęm ńĎiŠĽán c√°c nguy√™n tŠĽĎ giŠļ£m
C. B√°n k√≠nh nguy√™n tŠĽ≠ cŠĽßa c√°c nguy√™n tŠĽĎ tńÉng
D. TŠļ•t cŠļ£ c√°c nguy√™n tŠĽĎ ńĎŠĽĀu thŠĽÉ hiŠĽán t√≠nh phi kim
C√Ęu 3: HiŠĽán t∆įŠĽ£ng quan s√°t ńĎ∆įŠĽ£c dŠļęn NH3 qua CuO ńĎun n√≥ng l√†
A. CuO kh√īng ńĎŠĽēi m√†u.
B. CuO chuyŠĽÉn tŠĽę ńĎen sang v√†ng.
C. CuO chuyŠĽÉn tŠĽę ńĎen sang m√†u xanh.
D. CuO chuyŠĽÉn tŠĽę ńĎen sang m√†u ńĎŠĽŹ, c√≥ h∆°i H2O ng∆įng tŠĽ•.
C√Ęu 4: Kim loŠļ°i t√°c dŠĽ•ng HNO3 kh√īng tŠļ°o chŠļ•t n√†o sau ńĎ√Ęy
A. NH4NO3 B. NO C. NO2 D. N2O5
C√Ęu 5: HNO3 kh√īng thŠĽÉ hiŠĽán t√≠nh oxi ho√° mŠļ°nh vŠĽõi chŠļ•t n√†o sau ńĎ√Ęy
A. Fe3O4 B. Fe(OH)2 C. Fe2O3 D. FeO
C√Ęu 6: Cho FeCO3 t√°c dŠĽ•ng HNO3. SŠļ£n phŠļ©m kh√≠ ho√° n√Ęu mŠĽôt phŠļßn ngo√†i kh√īng kh√≠ v√† mŠĽôt muŠĽĎi kim loŠļ°i l√†:
A. CO, NO2, Fe(NO3)2 B. CO2, NO, Fe(NO3)3
C. CO2, NO2, Fe(NO3)2 D. CO2, NO2, Fe(NO3)3
C√Ęu 7: Trong dung dŠĽčch H3PO4 c√≥ c√°c ion sau
A. H+, HPO , PO B. H+, PO
C. H+, HPO , H2PO D. H+, HPO , H2PO , PO
C√Ęu8: Th√™m 0,15 mol KOH v√†o dung dŠĽčch chŠĽ©a 0,1 mol H3PO4. sau phŠļ£n ŠĽ©ng dung dŠĽčch c√≥ c√°c muŠĽĎi:
A.KH2PO4 và K2HPO4 B. K2HPO4 và K3PO4
C. KH2PO4 và K3PO4 D. KH2PO4, K2HPO4 và K3PO4
C√Ęu 9: ChŠĽćn c√īng thŠĽ©c ńĎ√ļng cŠĽßa apatit
A. Ca3(PO4)2 B. Ca(PO3)2 C. 3Ca3(PO4)2CaF2 D. CaP2O7
C√Ęu 10: H√≤a tan 1,2 g kim loŠļ°i X v√†o dung dŠĽčch HNO3 d∆į thu ńĎ∆įŠĽ£c 0,224 l√≠t kh√≠ nit∆° ŠĽü ńĎktc (giŠļ£ thiŠļŅt phŠļ£n ŠĽ©ng chŠĽČ tŠļ°o ra kh√≠ N2). VŠļ≠y X l√†:
A. Zn B. Cu C. Mg D. Al
C√Ęu11: Khi c√≥ sŠļ•m chŠĽõp kh√≠ quyŠĽÉn sinh ra chŠļ•t:
A. Oxit cacbon B. Oxit nit∆°.
C. N∆įŠĽõc. D. Kh√īng c√≥ kh√≠ g√¨ sinh ra
C√Ęu 12: Ph∆į∆°ng ph√°p chŠĽß yŠļŅu sŠļ£n xuŠļ•t N2 trong c√īng nghiŠĽáp
A. Ch∆įng cŠļ•t ph√Ęn ńĎoŠļ°n kh√īng kh√≠ lŠĽŹng B. NhiŠĽát ph√Ęn muŠĽĎi NH4NO3
C. Ph√Ęn hŠĽßy Protein D. TŠļ•t cŠļ£ ńĎŠĽĀu ńĎ√ļng
C√Ęu 13: HŠĽón hŠĽ£p A gŠĽďm N2 v√† H2 theo tŠĽČ lŠĽá 1 : 3 vŠĽĀ thŠĽÉ t√≠ch. TŠļ°o ńĎiŠĽĀu kiŠĽán cho phŠļ£n ŠĽ©ng xŠļ£y ra. TŠĽČ khŠĽĎi cŠĽßa A ńĎŠĽĎi vŠĽõi hŠĽón hŠĽ£p B sau phŠļ£n ŠĽ©ng l√† 0,6. HiŠĽáu suŠļ•t cŠĽßa phŠļ£n ŠĽ©ng l√†
A. 80% B. 50% C. 70% D. 85%
C√Ęu 14: ThuŠĽĎc nŠĽē ńĎen l√† hŠĽón hŠĽ£p n√†o sau ńĎ√Ęy?
A. KNO3 + S B. KClO3 + C C. KClO3 + C + S D. KNO3 + C + S
C√Ęu 15: Trong phŠļ£n ŠĽ©ng: KClO3 + NH3 ‚Üí KNO3 + KCl + Cl2 + H2O. HŠĽá sŠĽĎ c√Ęn bŠļĪng tŠĽĎi giŠļ£n cŠĽßa NH3 trong ph∆į∆°ng tr√¨nh l√†:
A. 10 B. 1 C. 2 D. 6
C√Ęu 16: ńźŠĽÉ ph√Ęn biŠĽát 3 lŠĽć HCl, H3PO4, HNO3 ng∆įŠĽĚi ta d√Ļng
A. QuŠĽ≥ t√≠m B. BaCl2 C. AgNO3 D. Ph√™noltal√™in
C√Ęu 17: Ho√° chŠļ•t c√≥ thŠĽÉ ho√† tan ho√†n to√†n hŠĽón hŠĽ£p 4 kim loŠļ°i: Ag, Zn, Fe, Cu l√†
A. Dung dŠĽčch NaOH B. Dung dŠĽčch H2SO4 ńĎŠļ∑c, nguŠĽôi
C. Dung dŠĽčch H2SO4 lo√£ng D. Dung dŠĽčch HNO3 lo√£ng
C√Ęu 18: Khi cho Cu t√°c dŠĽ•ng vŠĽõi dung dŠĽčch chŠĽ©a H2SO4 lo√£ng v√† NaNO3. Vai tr√≤ cŠĽßa NaNO3 trong phŠļ£n ŠĽ©ng l√†
A. ChŠļ•t x√ļc t√°c B. ChŠļ•t oxi h√≥a C. M√īi tr∆įŠĽĚng D. ChŠļ•t khŠĽ≠
C√Ęu 19: Cho m (g) Cu t√°c dŠĽ•ng HNO3 d∆į ńĎ∆įŠĽ£c 8,96 l√≠t (ńĎktc) hŠĽón hŠĽ£p NO v√† NO2 c√≥ khŠĽĎi l∆įŠĽ£ng l√† 15,2 gam. Gi√° trŠĽč cŠĽßa m l√†
A. 25,6 B. 16 C. 2,56 D. 8
C√Ęu 20: Ho√† tan ho√†n to√†n 11,68g Cu v√† CuO trong 2 lit dung dŠĽčch HNO3 0,25M thu ńĎ∆įŠĽ£c 1,792 lit kh√≠ NO (ńĎktc). PhŠļßn trńÉm khŠĽĎi l∆įŠĽ£ng CuO trong hŠĽóm hŠĽ£p ban ńĎŠļßu l√†
A. 61,64% B. 34,25% C. 39,36% D. 65,80%
C√Ęu 21: ńźŠĽÉ m gam Fe ngo√†i kh√īng kh√≠ sau thŠĽĚi gian ńĎ∆įŠĽ£c 12g hŠĽón hŠĽ£p B gŠĽďm Fe, FeO, Fe2O3, Fe3O4. Cho hŠĽón hŠĽ£p B t√°c dŠĽ•ng vŠĽõi HNO3 th√¨ ńĎ∆įŠĽ£c 2,24 l√≠t NO (ńĎktc). Gi√° trŠĽč cŠĽßa m l√†
A. 11,8 B. 10,08 C. 9,8 D. 8,8
C√Ęu 22: Nung 7,28g bŠĽôt Fe trong oxi, thu ńĎ∆įŠĽ£c m gam hŠĽón hŠĽ£p chŠļ•t rŠļĮn X. H√≤a tan hŠĽón hŠĽ£p X trong HNO3 ńĎŠļ∑c, n√≥ng thu ńĎ∆įŠĽ£c 1,568 lit kh√≠ (ńĎktc) l√† sŠļ£n phŠļ©m khŠĽ≠ duy nhŠļ•t. Gi√° trŠĽč m
A. 9,84 B. 9,65 C. 10,0 D. 8,72
C√Ęu 23: Ho√† tan ho√†n to√†n hŠĽón hŠĽ£p Fe, FeO, Fe2O3 v√† Fe3O4 v√†o dung dŠĽčch HNO3 ńĎŠļ∑c, n√≥ng (d∆į) thu ńĎ∆įŠĽ£c 4,48 l√≠t kh√≠ NO duy nhŠļ•t (ńĎktc) v√† 96,8 gam Fe(NO3)3. SŠĽĎ mol HNO3 ńĎ√£ tham gia phŠļ£n ŠĽ©ng
A. 1 B. 1,2 C. 1,4 D. 1,6
C√Ęu 24: Ho√† tan 20,8 gam hŠĽón hŠĽ£p bŠĽôt gŠĽďm FeS, FeS2, S bŠļĪng dung dŠĽčch HNO3 ńĎŠļ∑c n√≥ng d∆į thu ńĎ∆įŠĽ£c 53,76 l√≠t NO2 (sŠļ£n phŠļ©m khŠĽ≠ duy nhŠļ•t, ŠĽü ńĎkc) v√† dung dŠĽčch A. Cho dung dŠĽčch A t√°c dŠĽ•ng vŠĽõi dung dŠĽčch NaOH d∆į, lŠĽćc lŠļ•y to√†n bŠĽô kŠļŅt tŠĽßa nung trong kh√īng kh√≠ ńĎŠļŅn khŠĽĎi l∆įŠĽ£ng kh√īng ńĎŠĽēi th√¨ khŠĽĎi l∆įŠĽ£ng chŠļ•t rŠļĮn thu ńĎ∆įŠĽ£c l√†
A. 16 gam B. 9 gam C. 8,2 gam D. 10,7 gam
----(ńźŠĽÉ xem nŠĽôi dung phŠļßn tŠĽĪ luŠļ≠n ńĎŠĽĀ sŠĽĎ 2 vui l√≤ng xem tŠļ°i online hoŠļ∑c ńĎńÉng nhŠļ≠p ńĎŠĽÉ tŠļ£i vŠĽĀ m√°y)----
ńźŠĽÄ 3:
I. PHŠļ¶N TRŠļģC NGHIŠĽÜM:
C√Ęu 1: CŠļ∑p c√īng thŠĽ©c cŠĽßa liti nitrua v√† nh√īm nitrua l√†
A. LiN3, Al3N. B. Li2N3, Al2N3 C. Li3N2, Al3N2 D. Li3N, AlN
C√Ęu 2: ńźŠĽÉ nhŠļ≠n biŠļŅt dung dŠĽčch amoniac, ng∆įŠĽĚi ta ńĎ∆įa ńĎŠļßu ńĎŇ©a thŠĽßy tinh c√≥ tŠļ©m h√≥a chŠļ•t v√†o miŠĽáng lŠĽć ńĎŠĽĪng dung dŠĽčch amoniac. H√≥a chŠļ•t ńĎ∆įŠĽ£c d√Ļng l√†
A. dung dŠĽčch KOH. B. dung dŠĽčch NaCl.
C. dung dŠĽčch HCl. D. dung dŠĽčch KNO3.
C√Ęu 3: NhiŠĽát ph√Ęn AgNO3 thu ńĎ∆įŠĽ£c c√°c chŠļ•t thuŠĽôc ph∆į∆°ng √°n n√†o:
A. Ag2O, NO2 B. Ag2O, O2 C. Ag, NO2 ,O2 D. Ag2O, NO2 , O2
C√Ęu 4: NhŠļ≠n x√©t n√†o sau ńĎ√Ęy l√† sai?
A. Trong axit nitric, nit∆° h√≥a trŠĽč 5
B. Nit∆° c√≥ sŠĽĎ oxi h√≥a +5 trong axit nitric
C. Trong axit nitric, nit∆° h√≥a trŠĽč 4
D. C√≥ 1 li√™n kŠļŅt cho nhŠļ≠n trong c√īng thŠĽ©c cŠļ•u tŠļ°o cŠĽßa axit nitric
C√Ęu 5: ChŠļ•t c√≥ thŠĽÉ d√Ļng ńĎŠĽÉ l√†m kh√ī kh√≠ NH3 l√†
A. H2SO4 ńĎŠļ∑c B. P2O5 C. CuSO4 khan D. KOH rŠļĮn
C√Ęu 6: H√≤a tan 12,8g kim loŠļ°i h√≥a trŠĽč II trong 1 l∆įŠĽ£ng vŠĽęa ńĎŠĽß dung dŠĽčch HNO3 60% (D = 1,365g/ml), thu ńĎ∆įŠĽ£c 8,96 l√≠t (ńĎktc) mŠĽôt kh√≠ duy nhŠļ•t m√†u n√Ęu ńĎŠĽŹ. T√™n cŠĽßa kim loŠļ°i v√† thŠĽÉ t√≠ch dung dŠĽčch HNO3 ńĎ√£ phŠļ£n ŠĽ©ng l√†:
A. sŠļĮt; 82,3 ml B. ch√¨; 65,1 ml C. thŠĽßy ng√Ęn;125,6 ml D. ńĎŠĽďng; 61,5ml
C√Ęu 7: ńźŠĽÉ m gam Fe ngo√†i kh√īng kh√≠ sau thŠĽĚi gian ńĎ∆įŠĽ£c 12g hŠĽón hŠĽ£p B gŠĽďm Fe, FeO, Fe2O3, Fe3O4. Cho hŠĽón hŠĽ£p B t√°c dŠĽ•ng vŠĽõi HNO3 th√¨ ńĎ∆įŠĽ£c 2,24 l√≠t NO (ńĎktc). Gi√° trŠĽč cŠĽßa m l√†
A. 11,8 B. 10,08 C. 9,8 D. 8,8
C√Ęu 8: Ph∆į∆°ng ph√°p phŠļ£n ŠĽ©ng n√†o sau d√Ļng ńĎŠĽÉ ńĎiŠĽĀu chŠļŅ nit∆° trong c√īng nghiŠĽáp.
A. Ch∆įng ph√Ęn ńĎoŠļ°n kh√īng kh√≠ lŠĽŹng ńĎŠĽÉ t√°ch N2 khŠĽŹi hŠĽón hŠĽ£p kh√īng kh√≠ lŠĽŹng
B. NH4NO3 N2 + 2H2O
C. TŠļ•t cŠļ£ ńĎŠĽĀu sai.
D. NH3 N2 + H2
C√Ęu 9: Trong ph∆į∆°ng tr√¨nh h√≥a hŠĽćc cŠĽßa phŠļ£n ŠĽ©ng nhiŠĽát ph√Ęn sŠļĮt (III) nitrat, tŠĽēng c√°c hŠĽá sŠĽĎ bŠļĪng bao nhi√™u?
A. 9 B. 5 C. 7 D. 2
C√Ęu 10: ńźŠĽĎt ch√°y ho√†n to√†n 6,2 gam photpho trong oxi d∆į. Cho sŠļ£n phŠļ©m tŠļ°o th√†nh t√°c dŠĽ•ng vŠĽęa ńĎŠĽß vŠĽõi dung dŠĽčch NaOH 32% tŠļ°o th√†nh muŠĽĎi Na2HPO4. T√¨m khŠĽĎi l∆įŠĽ£ng dung dŠĽčch NaOH ńĎ√£ d√Ļng?
A. 75 gam B. 24 gam
C. 16 gam D. 50 gam
C√Ęu 11: Cho 3,2 gam Cu t√°c dŠĽ•ng vŠĽõi 100ml dung dŠĽčch hŠĽón hŠĽ£p HNO3 0,8M v√† H2SO4 0,2M thu ńĎ∆įŠĽ£c V lit (ńĎktc) kh√≠ NO sŠļ£n phŠļ©m khŠĽ≠ duy nhŠļ•t. Gi√° trŠĽč cŠĽßa V l√†
A. 0,336 B. 0,448 C. 0,672 D. 0,224
C√Ęu 12: Kh√≠ nit∆° c√≥ thŠĽÉ ńĎ∆įŠĽ£c tŠļ°o th√†nh phŠļ£n ŠĽ©ng h√≥a hŠĽćc n√†o sau ńĎ√Ęy?
A. NhiŠĽát ph√Ęn AgNO3 B. NhiŠĽát ph√Ęn NH4NO2
C. NhiŠĽát ph√Ęn NH4NO3 D. ńźŠĽĎt ch√°y NH3 trong Oxi c√≥ chŠļ•t x√ļc t√°c platin
C√Ęu 13: PhŠļ£i d√Ļng bao nhi√™u l√≠t kh√≠ nit∆° v√† bao nhi√™u l√≠t kh√≠ hidro ńĎŠĽÉ ńĎiŠĽĀu chŠļŅ 8,5 g NH3? BiŠļŅt rŠļĪng hiŠĽáu suŠļ•t chuyŠĽÉn h√≥a th√†nh amoniac l√† 25%. C√°c thŠĽÉ t√≠ch ńĎ∆įŠĽ£c ńĎo ŠĽü ńĎktc.
A. 22,4 lít N2 và 67,2 lít H2 B. 44,8 lít N2 và 134,4 lít H2
C. 22,4 lít N2 và 134,4 lít H2 D. 44,8 lít N2 và 67,2 lít H2
C√Ęu 14: Cho 3,2 gam Cu t√°c dŠĽ•ng hŠļŅt vŠĽõi dung dŠĽčch HNO3 ńĎŠļ∑c. ThŠĽÉ t√≠ch kh√≠ NO2 (ńĎktc) l√†
A. 2,24 lít B. 4,48 lít C. 3,36 lít D. 1,12 lít
C√Ęu 15: NŠļ°p ńĎŠļßy kh√≠ amoniac v√†o b√¨nh thŠĽßy tinh, ńĎŠļ≠y bŠļĪng n√ļt cao su c√≥ ŠĽĎng thŠĽßy tinh vuŠĽĎt nhŠĽćn. Nh√ļng ńĎŠļßu ŠĽĎng thŠĽßy tinh v√†o mŠĽôt chŠļ≠u n∆įŠĽõc c√≥ pha dung dŠĽčch phenolphtalein. HiŠĽán t∆įŠĽ£ng g√¨ sŠļĹ xŠļ£y ra?
A. N∆įŠĽõc trong chŠļ≠u phun v√†o b√¨nh thŠĽßy tinh th√†nh nhŠĽĮng tia m√†u hŠĽďng
B. Kh√≠ trong b√¨nh thŠĽßy tinh chuyŠĽÉn th√†nh m√†u hŠĽďng
C. N∆įŠĽõc tŠĽę chŠļ≠u tr√†n v√†o b√¨nh thŠĽßy tinh
D. N∆įŠĽõc trong chŠļ≠u tŠĽę kh√īng m√†u chuyŠĽÉn th√†nh m√†u hŠĽďng
C√Ęu 16: NhŠļ≠n biŠļŅt NH4Cl, (NH4)2SO4, NaNO3
A. NaOH B. AgCl C. Ba(OH)2 D. BaCl2
C√Ęu 17: Cho 38,4 g Cu tan trong 2,4 l√≠t dd HNO3 0,5M thu ńĎ∆įŠĽ£c V l√≠t NO(ńĎktc, sŠļ£n phŠļ©m duy nhŠļ•t). Gi√° trŠĽč cŠĽßa V l√†:
A. 8,96 B. 5,6 C. 4,48 D.6,72
C√Ęu 18: Cho Cu v√†o dung dŠĽčch H2SO4 lo√£ng. Cu sŠļĹ tan nŠļŅu th√™m v√†o ńĎ√≥.
A. TŠļ•t cŠļ£ ńĎŠĽĀu ńĎ√ļng B. Kh√≠ O2 C. Dung dŠĽčch HNO3 D. MuŠĽĎi KNO3
C√Ęu 19: Trong nhŠĽĮng nhŠļ≠n x√©t d∆įŠĽõi ńĎ√Ęy, nhŠļ≠n x√©t n√†o l√† kh√īngńĎ√ļng?
A. CŠļ•u h√¨nh e cŠĽßa N l√†: 1s22s22p3
B. SŠĽĎ hiŠĽáu nguy√™n tŠĽ≠ cŠĽßa nito bŠļĪng 7.
C. Ba electron ŠĽü ph√Ęn lŠĽõp 2p cŠĽßa N c√≥ thŠĽÉ tŠļ°o ńĎ∆įŠĽ£c 3 li√™n kŠļŅt cŠĽông h√≥a trŠĽč vŠĽõi c√°c nguy√™n tŠĽ≠ kh√°c.
D. Nguy√™n tŠĽ≠ N c√≥ hai lŠĽõp electron v√† lŠĽõp ngo√†i c√Ļng c√≥ 3 electron.
C√Ęu 20: Ph∆į∆°ng tr√¨nh phŠļ£n ŠĽ©ng giŠĽĮa Ag v√† HNO3 lo√£ng. TŠĽēng c√°c hŠĽá sŠĽĎ trong ph∆į∆°ng tr√¨nh h√≥a hŠĽćc l√†:
A. 13 B. 15 C. 12 D. 14
C√Ęu 21: D√£y n√†o d∆įŠĽõi ńĎ√Ęy gŠĽďm c√°c chŠļ•t m√† nguy√™n tŠĽĎ nit∆° c√≥ khŠļ£ nńÉng vŠĽęa thŠĽÉ hiŠĽán t√≠nh khŠĽ≠ vŠĽęa thŠĽÉ hiŠĽán t√≠nh oxi h√≥a khi tham gia phŠļ£n ŠĽ©ng?
A. NH3, NO, HNO3, N2O5 B. NH3, N2O5, N2, NO2
C. N2, NO, N2O, N2O5 D. NO2, N2, NO, N2O3
C√Ęu 22: Th√™m 0,15 mol KOH v√†o dung dŠĽčch chŠĽ©a 0,1 mol H3PO4. sau phŠļ£n ŠĽ©ng dung dŠĽčch c√≥ c√°c muŠĽĎi: A. KH2PO4 v√† K2HPO4 B. K2HPO4 v√† K3PO4
C. KH2PO4 và K3PO4 D. KH2PO4, K2HPO4 và K3PO4
C√Ęu 23: Kim loŠļ°i M phŠļ£n ŠĽ©ng dd HCl, dd Cu(NO¬≠3)2,dd HNO3 ńĎŠļ∑c nguŠĽôi. Kim loŠļ°i M l√†:
A. Al B. Zn C. Ag D. Fe
C√Ęu 24: Trong hŠĽ£p chŠļ•t n√†o sau ńĎ√Ęy nit∆° c√≥ sŠĽĎ oxi h√≥a cao nhŠļ•t?
A. NH4Cl B. N2O5 C. NO2 D. Mg3N2
----(ńźŠĽÉ xem nŠĽôi dung phŠļßn tŠĽĪ luŠļ≠n ńĎŠĽĀ sŠĽĎ 3 vui l√≤ng xem tŠļ°i online hoŠļ∑c ńĎńÉng nhŠļ≠p ńĎŠĽÉ tŠļ£i vŠĽĀ m√°y)----
ńźŠĽÄ 4:
I. PHŠļ¶N TRŠļģC NGHIŠĽÜM:
C√Ęu 1: D√£y n√†o d∆įŠĽõi ńĎ√Ęy gŠĽďm c√°c chŠļ•t m√† nguy√™n tŠĽĎ nit∆° c√≥ khŠļ£ nńÉng vŠĽęa thŠĽÉ hiŠĽán t√≠nh khŠĽ≠ vŠĽęa thŠĽÉ hiŠĽán t√≠nh oxi h√≥a khi tham gia phŠļ£n ŠĽ©ng?
A. NH3, N2O5, N2, NO2 B. NH3, NO, HNO3, N2O5
C. NO2, N2, NO, N2O3 D. N2, NO, N2O, N2O5
C√Ęu 2: ChŠļ•t c√≥ thŠĽÉ d√Ļng ńĎŠĽÉ l√†m kh√ī kh√≠ NH3 l√†
A. CuSO4 khan B. KOH rŠļĮn C. H2SO4 ńĎŠļ∑c D. P2O5
C√Ęu 3: Ph∆į∆°ng ph√°p phŠļ£n ŠĽ©ng n√†o sau d√Ļng ńĎŠĽÉ ńĎiŠĽĀu chŠļŅ nit∆° trong c√īng nghiŠĽáp.
A. Ch∆įng ph√Ęn ńĎoŠļ°n kh√īng kh√≠ lŠĽŹng ńĎŠĽÉ t√°ch N2 khŠĽŹi hŠĽón hŠĽ£p kh√īng kh√≠ lŠĽŹng
B. TŠļ•t cŠļ£ ńĎŠĽĀu sai.
C. NH4NO3 N2 + 2H2O
D. NH3 N2 + H2
C√Ęu 4: Kh√≠ nit∆° c√≥ thŠĽÉ ńĎ∆įŠĽ£c tŠļ°o th√†nh phŠļ£n ŠĽ©ng h√≥a hŠĽćc n√†o sau ńĎ√Ęy?
A. NhiŠĽát ph√Ęn AgNO3 B. ńźŠĽĎt ch√°y NH3 trong Oxi c√≥ chŠļ•t x√ļc t√°c platin
C. NhiŠĽát ph√Ęn NH4NO2 D. NhiŠĽát ph√Ęn NH4NO3
C√Ęu 5: ńźŠĽÉ m gam Fe ngo√†i kh√īng kh√≠ sau thŠĽĚi gian ńĎ∆įŠĽ£c 12g hŠĽón hŠĽ£p B gŠĽďm Fe, FeO, Fe2O3, Fe3O4. Cho hŠĽón hŠĽ£p B t√°c dŠĽ•ng vŠĽõi HNO3 th√¨ ńĎ∆įŠĽ£c 2,24 l√≠t NO (ńĎktc). Gi√° trŠĽč cŠĽßa m l√†
A. 10,08 B. 11,8 C. 8,8 D. 9,8
C√Ęu 6: Cho 3,2 gam Cu t√°c dŠĽ•ng hŠļŅt vŠĽõi dung dŠĽčch HNO3 ńĎŠļ∑c. ThŠĽÉ t√≠ch kh√≠ NO2 (ńĎktc) l√†
A. 2,24 lít B. 4,48 lít C. 3,36 lít D. 1,12 lít
C√Ęu 7: NhŠļ≠n biŠļŅt NH4Cl, (NH4)2SO4, NaNO3
A. AgCl B. NaOH C. Ba(OH)2 D. BaCl2
C√Ęu 8: PhŠļ£i d√Ļng bao nhi√™u l√≠t kh√≠ nit∆° v√† bao nhi√™u l√≠t kh√≠ hidro ńĎŠĽÉ ńĎiŠĽĀu chŠļŅ 8,5 g NH3? BiŠļŅt rŠļĪng hiŠĽáu suŠļ•t chuyŠĽÉn h√≥a th√†nh amoniac l√† 25%. C√°c thŠĽÉ t√≠ch ńĎ∆įŠĽ£c ńĎo ŠĽü ńĎktc.
A. 22,4 lít N2 và 67,2 lít H2 B. 44,8 lít N2 và 134,4 lít H2
C. 22,4 lít N2 và 134,4 lít H2 D. 44,8 lít N2 và 67,2 lít H2
C√Ęu 9: Trong ph∆į∆°ng tr√¨nh h√≥a hŠĽćc cŠĽßa phŠļ£n ŠĽ©ng nhiŠĽát ph√Ęn sŠļĮt (III) nitrat, tŠĽēng c√°c hŠĽá sŠĽĎ bŠļĪng bao nhi√™u?
A. 5 B. 9 C. 7 D. 2
C√Ęu 10: Trong hŠĽ£p chŠļ•t n√†o sau ńĎ√Ęy nit∆° c√≥ sŠĽĎ oxi h√≥a cao nhŠļ•t?
A. N2O5 B. Mg3N2 C. NO2 D. NH4Cl
C√Ęu 11: H√≤a tan 12,8g kim loŠļ°i h√≥a trŠĽč II trong 1 l∆įŠĽ£ng vŠĽęa ńĎŠĽß dung dŠĽčch HNO3 60% (D = 1,365g/ml), thu ńĎ∆įŠĽ£c 8,96 l√≠t (ńĎktc) mŠĽôt kh√≠ duy nhŠļ•t m√†u n√Ęu ńĎŠĽŹ. T√™n cŠĽßa kim loŠļ°i v√† thŠĽÉ t√≠ch dung dŠĽčch HNO3 ńĎ√£ phŠļ£n ŠĽ©ng l√†:
A. sŠļĮt; 82,3 ml B. ńĎŠĽďng; 61,5ml C. thŠĽßy ng√Ęn;125,6 ml D. ch√¨; 65,1 ml
C√Ęu 12: ńźŠĽÉ nhŠļ≠n biŠļŅt dung dŠĽčch amoniac, ng∆įŠĽĚi ta ńĎ∆įa ńĎŠļßu ńĎŇ©a thŠĽßy tinh c√≥ tŠļ©m h√≥a chŠļ•t v√†o miŠĽáng lŠĽć ńĎŠĽĪng dung dŠĽčch amoniac. H√≥a chŠļ•t ńĎ∆įŠĽ£c d√Ļng l√†
A. dung dŠĽčch HCl. B. dung dŠĽčch KOH.
C. dung dŠĽčch KNO3. D. dung dŠĽčch NaCl.
C√Ęu 13: NhiŠĽát ph√Ęn AgNO3 thu ńĎ∆įŠĽ£c c√°c chŠļ•t thuŠĽôc ph∆į∆°ng √°n n√†o:
A. Ag2O, NO2 B. Ag, NO2 ,O2 C. Ag2O, NO2 , O2 D. Ag2O, O2
C√Ęu 14: NŠļ°p ńĎŠļßy kh√≠ amoniac v√†o b√¨nh thŠĽßy tinh, ńĎŠļ≠y bŠļĪng n√ļt cao su c√≥ ŠĽĎng thŠĽßy tinh vuŠĽĎt nhŠĽćn. Nh√ļng ńĎŠļßu ŠĽĎng thŠĽßy tinh v√†o mŠĽôt chŠļ≠u n∆įŠĽõc c√≥ pha dung dŠĽčch phenolphtalein. HiŠĽán t∆įŠĽ£ng g√¨ sŠļĹ xŠļ£y ra?
A. N∆įŠĽõc trong chŠļ≠u phun v√†o b√¨nh thŠĽßy tinh th√†nh nhŠĽĮng tia m√†u hŠĽďng
B. Kh√≠ trong b√¨nh thŠĽßy tinh chuyŠĽÉn th√†nh m√†u hŠĽďng
C. N∆įŠĽõc tŠĽę chŠļ≠u tr√†n v√†o b√¨nh thŠĽßy tinh
D. N∆įŠĽõc trong chŠļ≠u tŠĽę kh√īng m√†u chuyŠĽÉn th√†nh m√†u hŠĽďng
C√Ęu 15: Cho s∆° ńĎŠĽď ńĎiŠĽĀu chŠļŅ HNO3 trong ph√≤ng th√≠ nghiŠĽám.
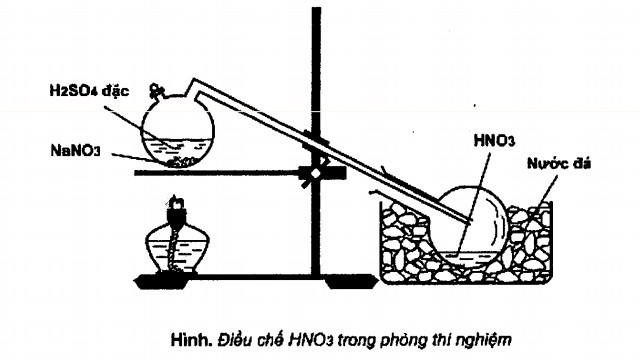
Ph√°t biŠĽÉu n√†o sau ńĎ√Ęy l√† sai khi n√≥i vŠĽĀ qu√° tr√¨nh ńĎiŠĽĀu chŠļŅ HNO3?
A. ńźŠĽĎt n√≥ng b√¨nh cŠļßu bŠļĪng ńĎ√®n cŠĽďn ńĎŠĽÉ phŠļ£n ŠĽ©ng xŠļ£y ra nhanh h∆°n.
B.HNO3 sinh ra d∆įŠĽõi dŠļ°ng h∆°i n√™n cŠļßn l√†m lŠļ°nh ńĎŠĽÉ ng∆įng tŠĽ•.
C.HNO3 c√≥ nhiŠĽát ńĎŠĽô s√īi thŠļ•p (-830C) n√™n dŠĽÖ bŠĽč bay h∆°i khi ńĎun n√≥ng.
D.HNO3 l√† axit yŠļŅu h∆°n H2SO4 n√™n bŠĽč ńĎŠļ©y ra khŠĽŹi muŠĽĎi.
C√Ęu 16: Cho 38,4 g Cu tan trong 2,4 l√≠t dd HNO3 0,5M thu ńĎ∆įŠĽ£c V l√≠t NO(ńĎktc, sŠļ£n phŠļ©m duy nhŠļ•t). Gi√° trŠĽč cŠĽßa V l√†: A. 8,96 B. 5,6 C. 4,48 D. 6,72
C√Ęu 17: Cho Cu v√†o dung dŠĽčch H2SO4 lo√£ng. Cu sŠļĹ tan nŠļŅu th√™m v√†o ńĎ√≥.
A. TŠļ•t cŠļ£ ńĎŠĽĀu ńĎ√ļng B. Kh√≠ O2 C. Dung dŠĽčch HNO3 D. MuŠĽĎi KNO3
C√Ęu 18: Trong nhŠĽĮng nhŠļ≠n x√©t d∆įŠĽõi ńĎ√Ęy, nhŠļ≠n x√©t n√†o l√† kh√īngńĎ√ļng?
A. CŠļ•u h√¨nh e cŠĽßa N l√†: 1s22s22p3
B. Ba electron ŠĽü ph√Ęn lŠĽõp 2p cŠĽßa N c√≥ thŠĽÉ tŠļ°o ńĎ∆įŠĽ£c 3 li√™n kŠļŅt cŠĽông h√≥a trŠĽč vŠĽõi c√°c nguy√™n tŠĽ≠ kh√°c.
C. SŠĽĎ hiŠĽáu nguy√™n tŠĽ≠ cŠĽßa nito bŠļĪng 7.
D. Nguy√™n tŠĽ≠ N c√≥ hai lŠĽõp electron v√† lŠĽõp ngo√†i c√Ļng c√≥ 3 electron.
C√Ęu 19: Ph∆į∆°ng tr√¨nh phŠļ£n ŠĽ©ng giŠĽĮa Ag v√† HNO3 lo√£ng. TŠĽēng c√°c hŠĽá sŠĽĎ trong ph∆į∆°ng tr√¨nh h√≥a hŠĽćc l√†:
A. 13 B. 15 C. 12 D. 14
C√Ęu 20: ńźŠĽĎt ch√°y ho√†n to√†n 6,2 gam photpho trong oxi d∆į. Cho sŠļ£n phŠļ©m tŠļ°o th√†nh t√°c dŠĽ•ng vŠĽęa ńĎŠĽß vŠĽõi dung dŠĽčch NaOH 32% tŠļ°o th√†nh muŠĽĎi Na2HPO4. T√¨m khŠĽĎi l∆įŠĽ£ng dung dŠĽčch NaOH ńĎ√£ d√Ļng?
A. 50 gam B. 24 gam C. 16 gam D. 75 gam
C√Ęu 21: Cho 3,2 gam Cu t√°c dŠĽ•ng vŠĽõi 100ml dung dŠĽčch hŠĽón hŠĽ£p HNO3 0,8M v√† H2SO4 0,2M thu ńĎ∆įŠĽ£c V lit (ńĎktc) kh√≠ NO sŠļ£n phŠļ©m khŠĽ≠ duy nhŠļ•t. Gi√° trŠĽč cŠĽßa V l√†
A. 0,336 B. 0,224 C. 0,672 D. 0,448
C√Ęu 22: Kim loŠļ°i M phŠļ£n ŠĽ©ng dd HCl, dd Cu(NO¬≠3)2,dd HNO3 ńĎŠļ∑c nguŠĽôi. Kim loŠļ°i M l√†:
A. Al B. Zn C. Ag D. Fe
C√Ęu 23: NhŠļ≠n x√©t n√†o sau ńĎ√Ęy l√† sai?
A. Trong axit nitric, nit∆° h√≥a trŠĽč 5
B. C√≥ 1 li√™n kŠļŅt cho nhŠļ≠n trong c√īng thŠĽ©c cŠļ•u tŠļ°o cŠĽßa axit nitric
C. Trong axit nitric, nit∆° h√≥a trŠĽč 4
D. Nit∆° c√≥ sŠĽĎ oxi h√≥a +5 trong axit nitric
C√Ęu 24: CŠļ∑p c√īng thŠĽ©c cŠĽßa liti nitrua v√† nh√īm nitrua l√†
A. LiN3, Al3N. B. Li3N2, Al3N2 C. Li2N3, Al2N3 D. Li3N, AlN
----(ńźŠĽÉ xem nŠĽôi dung phŠļßn tŠĽĪ luŠļ≠n ńĎŠĽĀ sŠĽĎ 4 vui l√≤ng xem tŠļ°i online hoŠļ∑c ńĎńÉng nhŠļ≠p ńĎŠĽÉ tŠļ£i vŠĽĀ m√°y)----
Tr√™n ńĎ√Ęy l√† mŠĽôt phŠļßn tr√≠ch ńĎoŠļ°n nŠĽôi dung BŠĽô ńĎŠĽĀ kiŠĽÉm tra 1 tiŠļŅt Ch∆į∆°ng 2 m√īn H√≥a hŠĽćc 11 nńÉm hŠĽćc 2019-2020 Tr∆įŠĽĚng THPT Nam S√°ch. ńźŠĽÉ xem to√†n bŠĽô nŠĽôi dung v√† ńĎ√°p √°n ńĎŠĽĀ kiŠĽÉm tra c√°c em chŠĽćn chŠĽ©c nńÉng xem online hoŠļ∑c ńĎńÉng nhŠļ≠p v√†o trang hoc247.net ńĎŠĽÉ tŠļ£i t√†i liŠĽáu vŠĽĀ m√°y t√≠nh.
Hy vŠĽćng ńĎŠĽĀ thi n√†y sŠļĹ gi√ļp c√°c em hŠĽćc sinh lŠĽõp 11 √īn tŠļ≠p tŠĽĎt v√† ńĎŠļ°t th√†nh t√≠ch cao trong b√†i kiŠĽÉm tra sŠļĮp tŠĽõi.
T∆į liŠĽáu nŠĽēi bŠļ≠t tuŠļßn
-
ńźŠĽĀ thi minh hŠĽća m√īn To√°n tŠĽĎt nghiŠĽáp THPT nńÉm 2025
22/10/20241478 - Xem thêm
ERROR:connection to 10.20.1.101:9312 failed (errno=111, msg=Connection refused)
ERROR:connection to 10.20.1.101:9312 failed (errno=111, msg=Connection refused)




